Në fushën e kimisë kemi reaksionet kimike që ndodhin midis molekulave dhe atomeve. Sot ne do të flasim për hidrolizë. Hidroliza është një lloj i reaksionit kimik që mund të ndodhë midis molekulave ose joneve inorganike dhe organike. Karakteristika kryesore e hidrolizës është se ajo përfshin pjesëmarrjen e ujit në mënyrë që lidhjet të mund të prishen.
Në këtë artikull ne do t'ju tregojmë për të gjitha karakteristikat dhe rëndësinë e hidrolizës në fushën e kimisë.
Çfarë është hidroliza
Po flasim për një lloj reaksioni kimik që mund të ndodhë si midis molekulave organike ashtu edhe atyre inorganike. Kushti thelbësor është që uji duhet të përfshihet në mënyrë që të mundet thyejnë lidhjet e këtyre molekulave. Fjala hidrolizë vjen nga greqishtja hydro, që do të thotë ujë dhe nga lysis, që do të thotë këputje. Përkthyer në formë, hidroliza mund të njihet si prishja e ujit. Në këtë rast, ne po flasim për thyerjen e lidhjeve të disa reaktantëve përmes pjesëmarrjes së ujit.
Molekula e ujit përbëhet nga dy atome hidrogjeni dhe një atome oksigjeni. Falë këtij kombinimi të atomeve, formohet një ekuilibër midis joneve të kripërave të acideve dhe bazave të dobëta. Acidet dhe bazat janë koncepte që paraqiten në studimet e përgjithshme të kimisë dhe kimisë analitike. Hidroliza mund të thuhet se është një nga reagimet më të thjeshta kimike atje. Ekuacioni i përgjithshëm për një hidrolizë është si më poshtë:
AB + H2O = AH + B-OH
Ka disa shembuj të hidrolizës ku uji ose në vetvete nuk mund të thyejë një lidhje të caktuar kovalente. Ne kujtojmë se një lidhje kovalente është ajo në të cilën disa molekula me karakteristika jometalike bashkohen së bashku për të formuar një molekulë tjetër të re. Lidhja që bashkohet me ta njihet si lidhje kovalente. Kur vetëm uji nuk është në gjendje ta thyejë këtë lidhje, procesi përshpejtohet ose katalizohet nga acidifikimi ose alkalizimi i mjedisit. Kjo është, në prani të joneve, hidroliza mund të katalizohet. Dhe ka enzima që janë të afta të katalizojnë reaksionin kimik të hidrolizës.
tipare kryesore

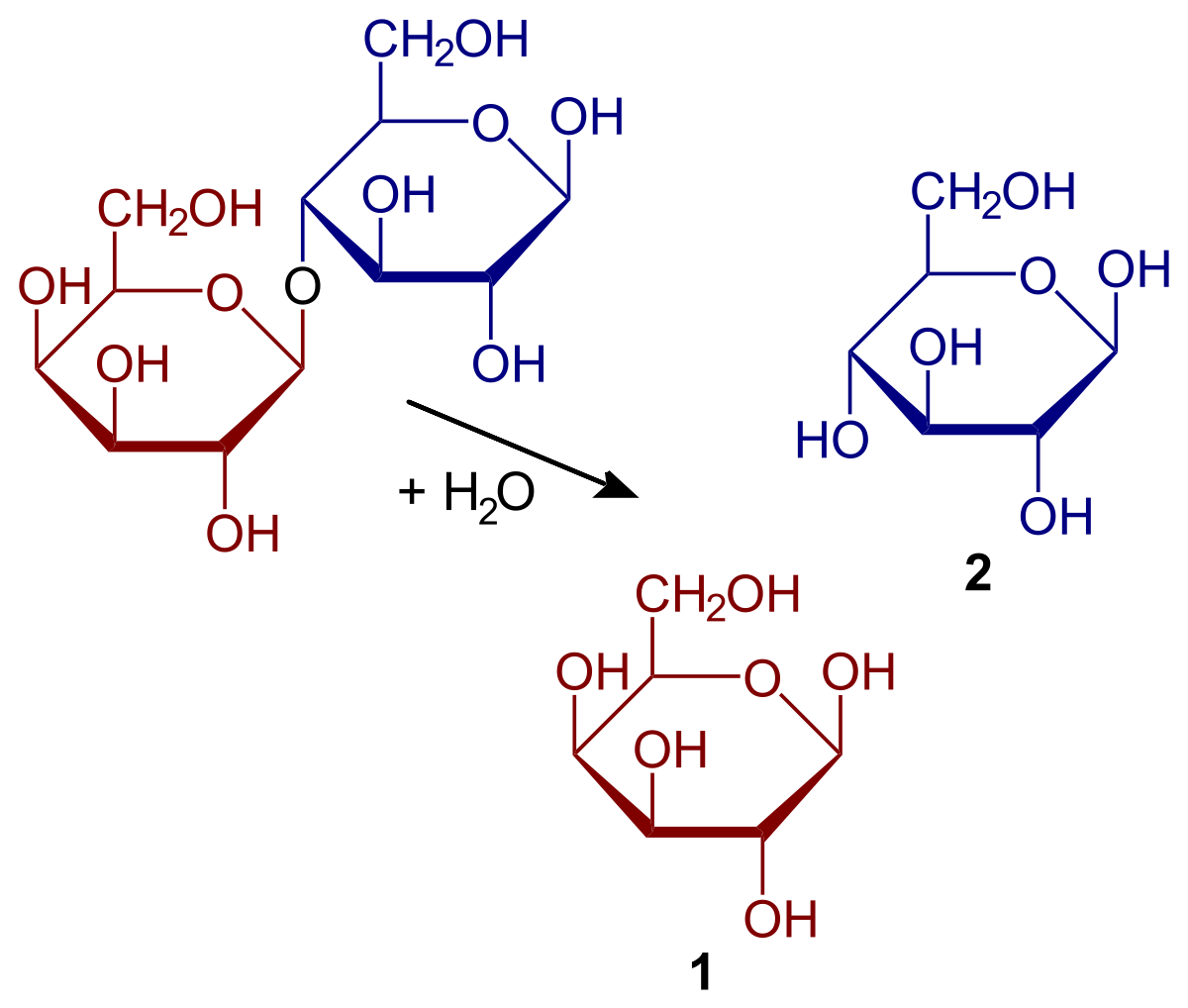
Le të shohim cilat janë karakteristikat dhe nga çfarë përbëhet hidroliza. Ky lloj i reaksionit zë një vend të veçantë kur bëhet fjalë për biomolekulat. Dhe është se lidhjet që mbajnë monomeret e molekulave së bashku janë të ndjeshme ndaj hidrolizimit në kushte të caktuara. Kjo është, lidhjet kovalente me të cilat janë të bashkuara molekulat mund të prishen në prani të ujit. Një shembull i kësaj janë sheqernat. Sheqernat janë të afta të hidrolizojnë për të zbërthyer polisakaridet në monosakaride. Kjo ndodh falë veprimit të enzimave të njohura si glukozidaza.
Duhet të kihet parasysh se nuk është vetëm molekula një substrat që prish lidhjen. Vetë uji gjithashtu thyhet dhe eventualisht ndan jonet. Thyerjet e ujit në H + dhe OH–, ku H + përfundon me A, dhe OH– me B. AB kështu reagon me një molekulë uji, duke prodhuar dy produkte, AH dhe B-OH.
Prandaj, mund të themi se hidroliza është një reaksion kimik në kundërshtim me kondensimin. Nga kondensimi, bashkohen dy produkte duke lëshuar një molekulë të vogël. Kjo molekulë e vogël është uji. Përkundrazi, në hidrolizë konsumohet një molekulë, ndërsa në kondensim kjo molekulë e elektrolizës konsumohet, lirohet ose prodhohet.
Për ta bërë më të lehtë për t'u kuptuar, ne do të shpjegojmë përsëri shembullin e sheqernave. Le të supozojmë se AB është një dimer saharoze. Në këtë rast A përfaqëson glukozën dhe B përfaqëson fruktozën. Kjo lidhje në, e cila njihet me emrin glikozidik, mund të hidrolizohet për të dhënë dy monosakaride të ndara dhe tretësirën. E njëjta gjë ndodh me oligosakaridet dhe polisakaridet nëse enzimat janë ato që veprojnë në reaksione.
Ne e dimë që ky reaksion kimik ka vetëm një drejtim. Kjo do të thotë se është një lloj hidrolize e pakthyeshme. Nga ana tjetër, ka reaksione të hidrolizës që janë të kthyeshme pasi të arrihet ekuilibri.
Shembuj të reaksioneve të hidrolizës
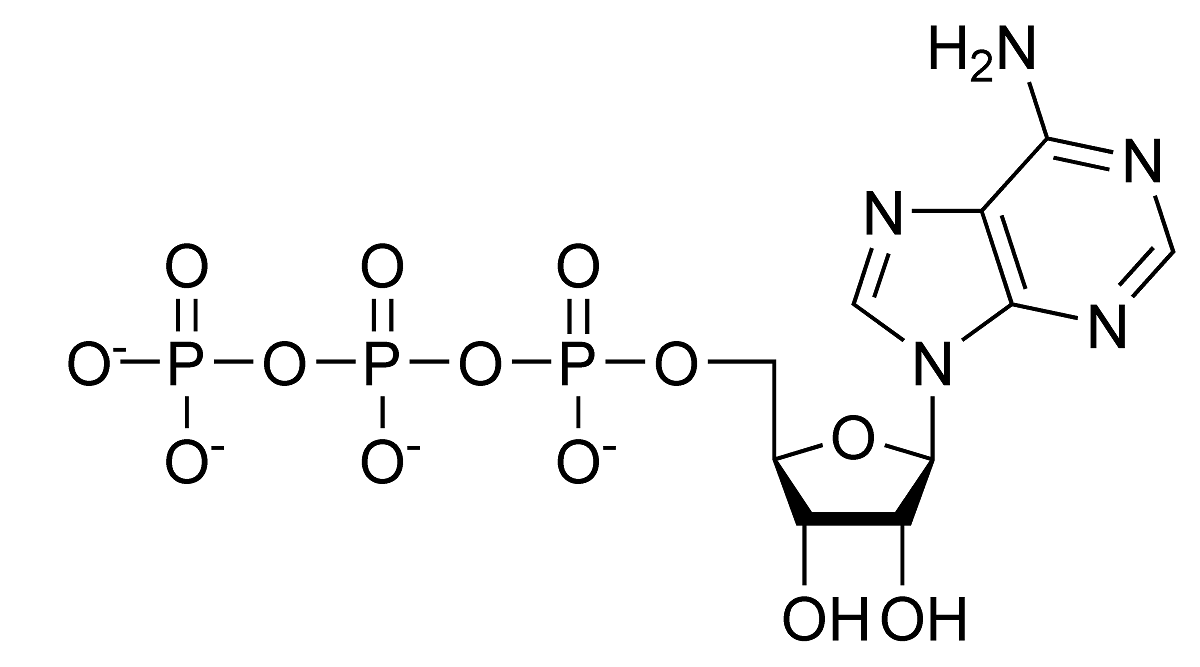
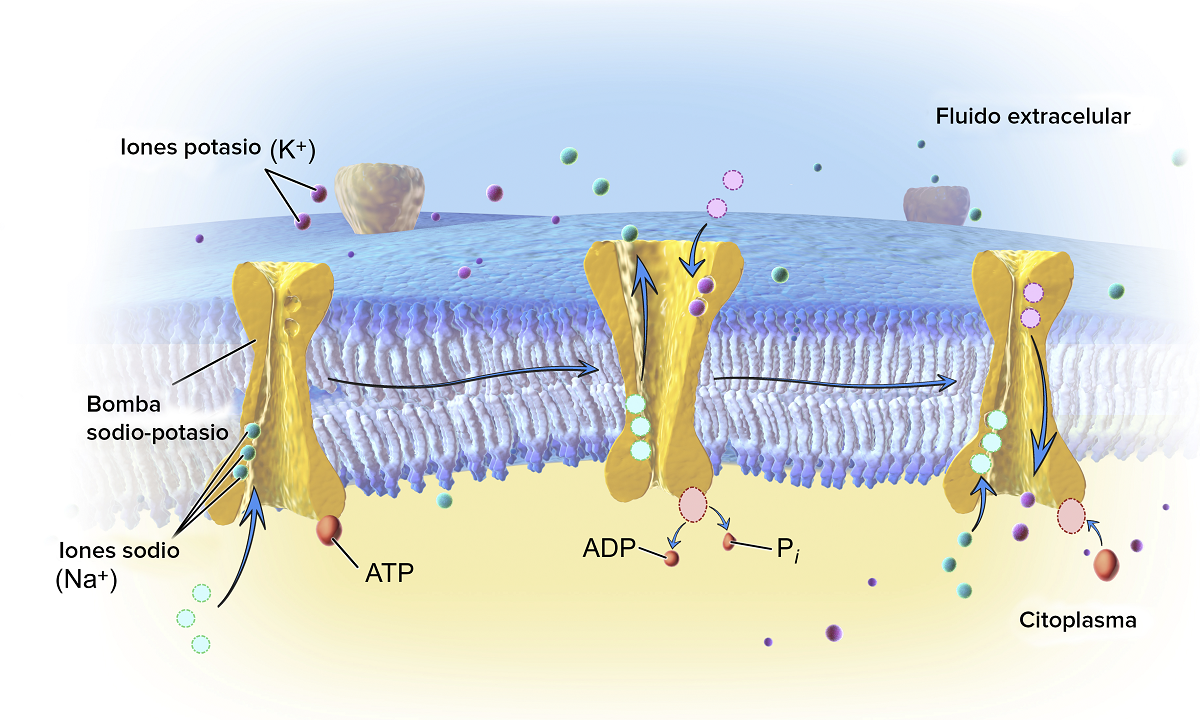
Le të shohim cilët janë shembujt kryesorë të hidrolizës që ndodhin natyrshëm. Para së gjithash, shihni reagimin e hidrolizës së ATP. Ne e dimë që kjo molekulë ka vlera të qëndrueshme të pH midis 6.8 dhe 7.4. Sidoqoftë, nëse vlerat e pH rriten për tu bërë shumë më alkaline, ajo mund të hidrolizohet në mënyrë spontane. Në qeniet e gjalla, hidroliza katalizohet nga enzimat e njohura me emrin e ATPazave. Isshtë një lloj i reaksionit kimik ekzergonik. Kjo do të thotë që entropia e ADP është më e madhe se ajo e ATP, kështu që variacioni i energjisë së lirë ndodh nga hidroliza e ATP. Ky lloj i hidrolizës përdor reagime të shumta endergonike.
Reaksionet e bashkuara janë një lloj tjetër i reaksionit ku ndodh hidroliza. Në disa raste përdoret për shndërrimin e një përbërjeje A në një përbërje B. Shembulli më i njohur i hidrolizës ndodh natyrshëm në ujë. Asshtë sikur një nga molekulat e ujit të mund të copëtohet në jone dhe lidhjet e protonit të hidrogjenit me atomin e oksigjenit të molekulës tjetër të ujit. Kjo krijon jon hidron. Mund të quhet më shumë sesa një hidrolizë si një automionizim ose autoprotolizë e ujit.
Më në fund, një tjetër nga pjesët ku këto reaksione gjenerohen në një mënyrë të përbashkët në proteina. Ne e dimë që proteinat janë molekula të qëndrueshme dhe për të arritur hidrolizën e tyre të plotë, kërkohen kushte ekstreme. Kujtojmë që proteinat përbëhen nga aminoacide. Sidoqoftë, qeniet e gjalla janë të pajisura me një arsenal enzimash që lejojnë hidrolizën e proteinave në aminoacide në duodenum.
Shpresoj që me këtë informacion të mësoni më shumë rreth hidrolizës dhe karakteristikave të saj.