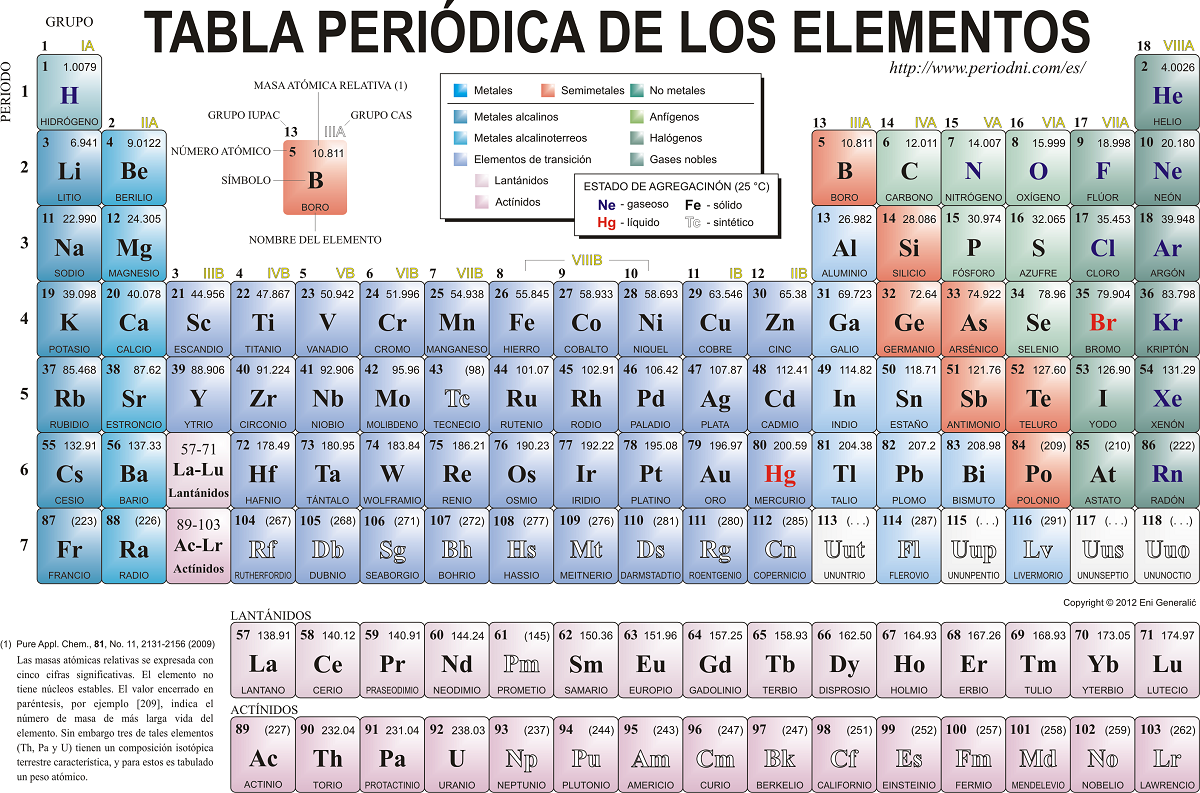
Ο περιοδικός πίνακας είναι ένα γραφικό και εννοιολογικό εργαλείο που οργανώνει όλα τα χημικά στοιχεία που είναι γνωστά στον άνθρωπο σύμφωνα με τον ατομικό τους αριθμό (δηλαδή τον αριθμό των πρωτονίων στον πυρήνα) και άλλες θεμελιώδεις χημικές ιδιότητες. Πολλοί άνθρωποι δεν γνωρίζουν καλά το προέλευση του περιοδικού πίνακα.
Ως εκ τούτου, θα σας πούμε για την προέλευση του περιοδικού πίνακα, την ιστορία του και τη σημασία που έχει για τη χημεία.
Προέλευση του περιοδικού πίνακα

Η πρώτη έκδοση αυτού του εννοιολογικού μοντέλου δημοσιεύτηκε στη Γερμανία το 1869 από τον ρωσικής καταγωγής χημικό Dimitri Mendeleev (1834-1907), ο οποίος ανακάλυψε ένα αναγνωρίσιμο σχήμα για να βοηθήσει στην κατηγοριοποίηση και την γραφική τους οργάνωση. Το όνομά του προέρχεται από την υπόθεση του Mendeleev ότι το ατομικό βάρος καθορίζει τις περιοδικές ιδιότητες των στοιχείων.
Ο πρώτος περιοδικός πίνακας στοιχείων τακτοποίησε τα 63 στοιχεία που ανακαλύφθηκαν εκείνη την εποχή σε έξι στήλες, κάτι που είναι γενικά αποδεκτό και σεβαστό από τους μελετητές αυτού του κλάδου. Θεωρείται η πρώτη προσπάθεια συστηματοποίησης των στοιχείων που πρότεινε ο Antoine Lavoisier ή ο André-Emile Bégueille de Champs Courtois Σημαντική βελτίωση σε σχέση με τα πρώτα τραπέζια που δημιουργήθηκαν από τον Béguyer de Chancourtois (μια «επίγεια προπέλα») το 1862 και τον Julius Lothar Meyer το 1864.
Εκτός από τη δημιουργία του περιοδικού πίνακα, ο Mendeleev το χρησιμοποίησε ως εργαλείο για να συμπεράνει την αναπόφευκτη ύπαρξη στοιχείων που δεν έχουν ακόμη ανακαλυφθεί, μια πρόβλεψη που εκπληρώθηκε αργότερα όταν άρχισαν να ανακαλύπτονται πολλά από τα στοιχεία που κάλυπταν τα κενά του τραπεζιού του.
Από τότε, ωστόσο, ο περιοδικός πίνακας έχει επανεφευρεθεί και επαναδιατυπωθεί αρκετές φορές, επεκτείνοντας τα άτομα που ανακαλύφθηκαν ή συντέθηκαν αργότερα. Ο ίδιος ο Mendeleev δημιούργησε μια δεύτερη έκδοση το 1871. Η σημερινή δομή επινοήθηκε από τον Ελβετό χημικό Alfred Werner (1866-1919) από τον αρχικό πίνακα και το σχέδιο της τυπικής φιγούρας αποδίδεται στον Αμερικανό χημικό Horace Groves Deming.
Μια νέα έκδοση του πίνακα, που προτάθηκε από τον Κοσταρικανό Gil Chaverri (1921-2005), λαμβάνει υπόψη τις ηλεκτρονικές δομές των στοιχείων παρά τους αριθμούς πρωτονίων τους. Η σημερινή αποδοχή όμως της παραδοσιακής εκδοχής είναι απόλυτη.
Ιστορία του περιοδικού πίνακα

Τον XNUMXο αιώνα, οι χημικοί άρχισαν να ταξινομούν τα γνωστά στοιχεία με βάση την ομοιότητα τους στις φυσικές και χημικές ιδιότητες. Το τέλος αυτών των μελετών παρήγαγε τον σύγχρονο περιοδικό πίνακα στοιχείων όπως τον ξέρουμε.
Μεταξύ του 1817 και του 1829, ο Γερμανός χημικός Johan Dobereiner ομαδοποίησε ορισμένα στοιχεία σε ομάδες των τριών, που ονομάζονται τρίδυμα, επειδή μοιράζονταν παρόμοιες χημικές ιδιότητες. Για παράδειγμα, στην τριάδα χλωρίου (Cl), βρωμίου (Br) και ιωδίου (I), παρατηρήσατε ότι η ατομική μάζα του Br ήταν πολύ κοντά στη μέση μάζα του Cl και του I. Δυστυχώς, δεν ταξινομούνται όλα τα στοιχεία σε τρίδυμα.και οι προσπάθειές του απέτυχαν να καταλήξουν σε ταξινόμηση στοιχείων.
Το 1863, ο Βρετανός χημικός John Newlands χώρισε τα στοιχεία σε ομάδες και πρότεινε τον νόμο των οκτάβων, που αποτελείται από στοιχεία αυξανόμενης ατομικής μάζας στα οποία ορισμένες ιδιότητες επαναλαμβάνονται κάθε 8 στοιχεία.
Το 1869, ο Ρώσος χημικός Dmitri Mendeleev δημοσίευσε τον πρώτο του περιοδικό πίνακα, απαριθμώντας τα στοιχεία κατά σειρά αύξησης της ατομικής μάζας. Την ίδια εποχή, ο Γερμανός χημικός Lothar Meyer δημοσίευσε τον δικό του περιοδικό πίνακα, στον οποίο τα στοιχεία ήταν διατεταγμένα από τη μικρότερη στη μεγαλύτερη ατομική μάζα. Ο Mendeleev τακτοποίησε τα τραπέζια τους σε οριζόντιες διατάξεις, αφήνοντας κενά κενά όπου έπρεπε να προσθέσουν κάτι που δεν είχε ανακαλυφθεί ακόμη. Μέσα στον οργανισμό, ο Mendeleev οραματίστηκε ένα ξεχωριστό μοτίβο: στοιχεία με παρόμοιες χημικές ιδιότητες εμφανίζονται σε τακτά (ή περιοδικά) διαστήματα σε κάθετες στήλες σε έναν πίνακα. Μετά την ανακάλυψη του γαλλίου (Ga), του σκανδίου (Sc) και του γερμανίου (Ge) μεταξύ 1874 και 1885, οι προβλέψεις του Mendeleev υποστηρίχθηκαν τοποθετώντας τις σε αυτά τα κενά, γεγονός που έκανε τον περιοδικό του πίνακα έναν κόσμο που έχει αποκτήσει μεγαλύτερη αξία και αποδοχή.
Το 1913, ο Βρετανός χημικός Henry Moseley προσδιόρισε το πυρηνικό φορτίο (ατομικός αριθμός) των στοιχείων μέσω μελετών ακτίνων Χ και τα ανασυγκρότησε με σειρά αυξανόμενου ατομικού αριθμού όπως τα γνωρίζουμε σήμερα.
Ποιες είναι οι ομάδες του περιοδικού πίνακα στοιχείων;
Στη χημεία, μια ομάδα περιοδικού πίνακα είναι μια στήλη από συστατικά στοιχεία, που αντιστοιχεί σε μια ομάδα χημικών στοιχείων με πολλά ατομικά χαρακτηριστικά. Στην πραγματικότητα, η κύρια συνάρτηση του περιοδικού πίνακα, που δημιουργήθηκε από τον Ρώσο χημικό Dmitri Mendeleev (1834-1907), επρόκειτο ακριβώς να χρησιμεύσει ως διάγραμμα για την ταξινόμηση και την οργάνωση των διαφορετικών ομάδων γνωστών χημικών στοιχείων, για τα οποία ο πληθυσμός του είναι ένα από τα σημαντικότερα συστατικά του.
Οι ομάδες αναπαρίστανται στις στήλες του πίνακα, ενώ οι σειρές σχηματίζουν τις τελείες. Υπάρχουν 18 διαφορετικές ομάδες, αριθμημένες από το 1 έως το 18, καθένα από τα οποία περιέχει μεταβλητό αριθμό χημικών στοιχείων. Κάθε ομάδα στοιχείων έχει τον ίδιο αριθμό ηλεκτρονίων στο τελευταίο ατομικό τους κέλυφος, γι' αυτό έχουν παρόμοιες χημικές ιδιότητες, αφού οι χημικές ιδιότητες των χημικών στοιχείων σχετίζονται στενά με τα ηλεκτρόνια που βρίσκονται στο τελευταίο ατομικό κέλυφος.
Η αρίθμηση των διαφορετικών ομάδων στον πίνακα έχει καθοριστεί από τη Διεθνή Ένωση Καθαρής και Εφαρμοσμένης Χημείας (IUPAC) και αντιστοιχεί στους αραβικούς αριθμούς (1, 2, 3...18) που αντικαθιστούν την παραδοσιακή ευρωπαϊκή μέθοδο που χρησιμοποιούσε λατινικούς αριθμούς και Τα γράμματα (IA, IIA, IIIA…VIIIA) και η αμερικανική μέθοδος χρησιμοποιούν επίσης λατινικούς αριθμούς και γράμματα, αλλά σε διαφορετική διάταξη από την ευρωπαϊκή μέθοδο.
- IUPAC. 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18.
- ευρωπαϊκό σύστημα. ΙΑ, ΙΙΑ, IIIA, IVA, VA, VIA, VIIA, VIIIA, VIIIA, VIIIA, IB, IIB, IIIB, IVB, VB, VIB, VIIB, VIII.
- αμερικανικό σύστημα. ΙΑ, ΙΙΑ, IIIB, IVB, VB, VIB, VIIB, VIII, VIII, VIIIB, IB, IIB, IIIA, IVA, VA, VIA, VIIA, VIIIA.
Με αυτόν τον τρόπο, κάθε στοιχείο που εμφανίζεται στον περιοδικό πίνακα αντιστοιχεί πάντα σε μια συγκεκριμένη ομάδα και περίοδο, αντικατοπτρίζοντας τον τρόπο με τον οποίο αναπτύσσεται η ανθρώπινη επιστήμη για την ταξινόμηση της ύλης.
Όπως μπορείτε να δείτε, ο περιοδικός πίνακας ήταν μια τεράστια πρόοδος στη χημεία σε όλη την ιστορία και σήμερα. Ελπίζω ότι με αυτές τις πληροφορίες μπορείτε να μάθετε περισσότερα για την προέλευση του περιοδικού πίνακα και τα χαρακτηριστικά του.