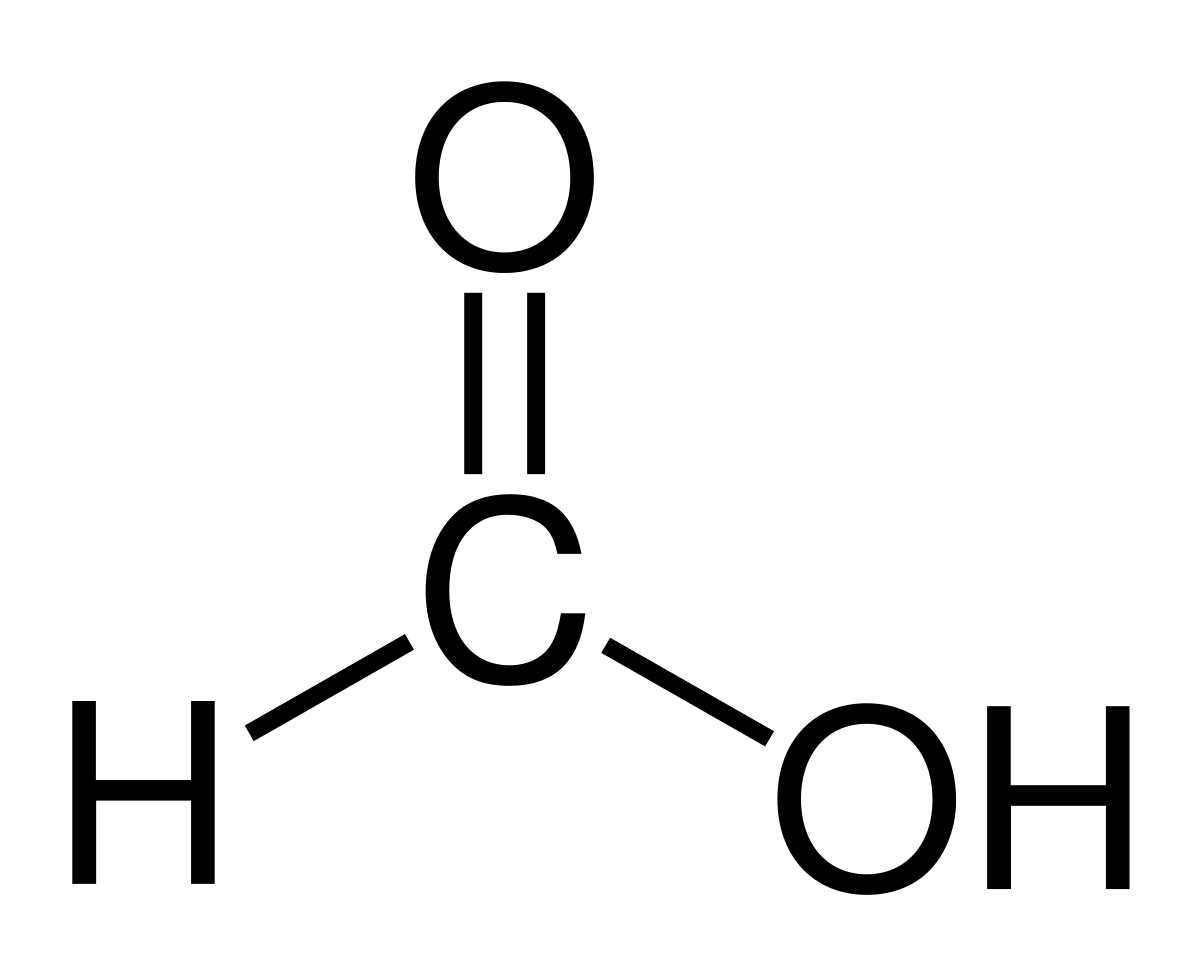
El maursyre o Metansyre er den enkleste og minste forbindelsen av alle organiske syrer. Den har molekylformelen HCOOH med bare ett hydrogenatom bundet til et karbonatom. Navnet kommer fra ordet formica, som betyr maur på latin. Det er en ganske viktig forbindelse i kjemiens verden og mye brukt i dag.
Av denne grunn skal vi dedikere denne artikkelen til å fortelle deg alt du trenger å vite om maursyre, dens egenskaper og viktighet.
Hovedkarakteristikker
Naturforskere fra det XNUMX. århundre oppdaget at visse typer insekter (termicider), som f.eks. maur, termitter, bier og biller, skiller de ut denne forbindelsen som gjør bittene deres smertefulle. I tillegg bruker disse insektene denne forbindelsen som en mekanisme for angrep, forsvar og kjemisk signalering.
De har giftige kjertler som driver ut denne og andre syrer, for eksempel eddiksyre, fra kroppen i form av en tåke. Maursyre er sterkere enn eddiksyre (CH3COOH); derfor vil en lik mengde maursyre oppløst i vann resultere i en løsning med lavere pH.
Den engelske naturforskeren John Ray oppnådde isolasjonen av denne forbindelsen i 1671, utvunnet fra et stort antall maur. På den annen side ble den første vellykkede syntesen av denne forbindelsen utført av den franske kjemikeren og fysikeren Joseph Gay-Lussac ved å bruke blåsyre (HCN) som reagens.
maursyre i naturen

Maursyre kan eksistere på terrestriske nivåer, som en komponent av biomasse eller i atmosfæren, delta i en lang rekke kjemiske reaksjoner, den kan til og med finnes under jorden, i olje eller i gassfasen på overflaten.
Når det gjelder biomasse, er insekter og planter hovedprodusentene av denne syren. Når fossilt brensel brenner, produserer de gassformig maursyre; derfor slipper bilmotorer denne syren ut i atmosfæren.
Imidlertid det bor mange maur på jorden, og produksjonen av maursyre mellom dem er tusenvis av ganger større enn mengden metansyre produsert av menneskelig industri på ett år. Skogbranner er også en gassformig kilde til maursyre.
Høyere oppe, i den komplekse atmosfæriske matrisen, foregår fotokjemiske prosesser for syntese av maursyre. På dette tidspunktet brytes mange flyktige organiske forbindelser (VOC) ned under påvirkning av UV-stråling eller oksideres av OH-radikalmekanismen. Den rike og komplekse atmosfæriske kjemien er langt den viktigste kilden til metansyre på jorden.
Atomstruktur av maursyre
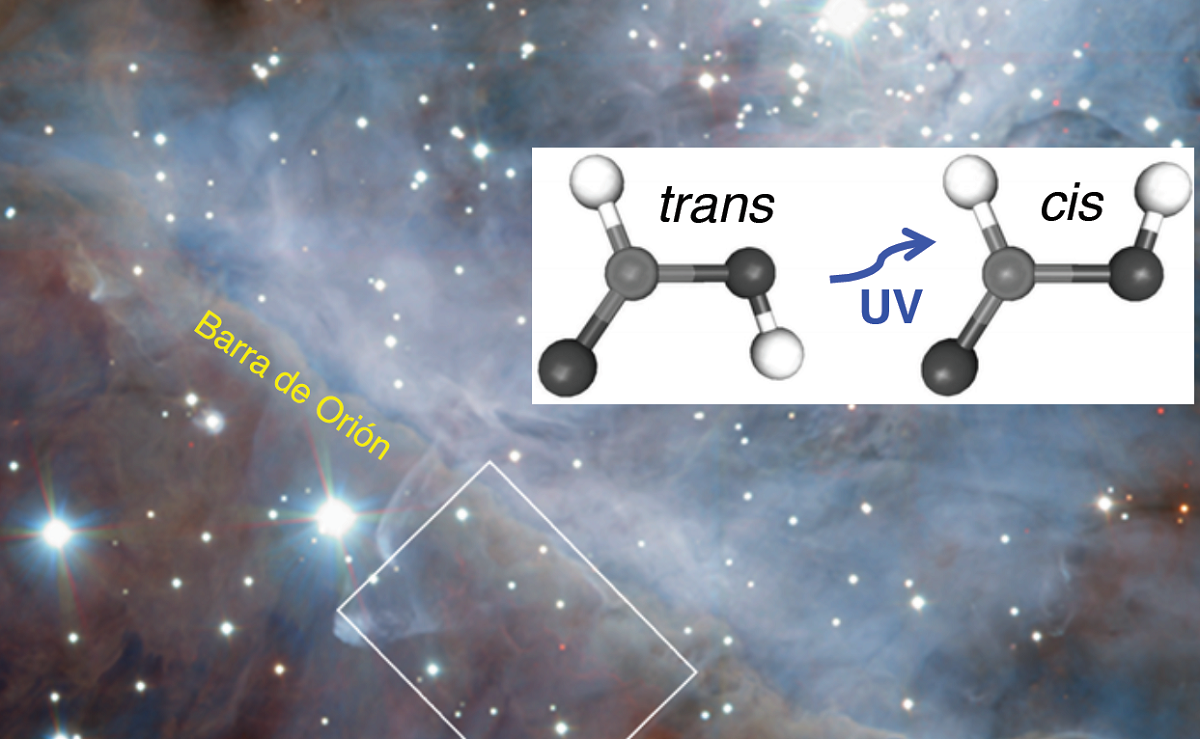
Figuren over viser strukturen til gassfasedimeren av maursyre. De hvite kulene tilsvarer hydrogenatomer, de røde til oksygenatomer og de svarte til karbonatomer.
To grupper kan sees i disse molekylene: hydroksyl (-OH) og formyl (-CH=O), som er i stand til å danne hydrogenbindinger. Disse interaksjonene er av typen OHO, hvor hydroksylgruppen er H-donoren og formylgruppen er O-donoren.
Imidlertid mangler H bundet til karbonatomer denne evnen. Disse interaksjonene er veldig sterke, og hydrogenet i OH-gruppen er surere på grunn av det elektronmangelfulle H-atomet; Og dermed, dette hydrogenet stabiliserer broen ytterligere. Som et resultat av ovenstående eksisterer maursyre som en dimer og ikke som et individuelt molekyl.
Når temperaturen synker, orienterer dimeren sine hydrogenbindinger for å skape den mest stabile strukturen med andre dimerer, noe som resulterer i uendelige alfa- og beta-kjeder av metansyre. Denne krystallstrukturen Det avhenger av de fysiske variablene som virker på det, som trykk og temperatur.. Derfor er strengen konvertibel. Hvis trykket økes til ekstreme nivåer, blir kjedene komprimert nok til å bli betraktet som en krystallinsk polymer av maursyre.
Egenskaper
Vi skal fokusere på å beskrive hovedegenskapene til maursyre:
- metansyre er en fargeløs væske ved romtemperatur med en sterk stikkende lukt. Den har en molekylvekt på 46g/mol, et smeltepunkt på 8,4ºC og et kokepunkt på 100,8ºC, høyere enn vann.
- Blandbar med vann og polare organiske løsemidler som eter, aceton, metanol og etanol.
- Tvert imot, i aromatiske løsningsmidler som benzen og toluen er den dårlig løselig fordi maursyre har få karbonatomer i strukturen.
- Den har en pKa på 3,77, som er surere enn eddiksyre, noe som kan forklares fordi metylgruppen gir elektrontetthet til karbonatomet oksidert av to oksygener. Dette resulterer i en liten reduksjon i surheten til protonene (CH3COOH, HCOOH).
- Når syren er deprotonert, konverteres til formatanionet HCOO-, som delokaliserer den negative ladningen mellom de to oksygenatomene. Derfor er det et stabilt anion og er ansvarlig for den høye surheten til maursyre.
Bruk av maursyre
Mat- og landbruksnæringen
Like skadelig som metansyre, det brukes i tilstrekkelige konsentrasjoner som matkonserveringsmiddel på grunn av dets antibakterielle effekt. Av samme grunn som den brukes i landbruket, har den også insektdrepende egenskaper. Den har også en antiseptisk effekt på gress og bidrar til å forhindre tarmgass hos husdyr.
Tekstil- og fottøyindustrien
Den brukes i tekstilindustrien for å farge og foredle tekstiler og er sannsynligvis den vanligste bruken av denne syren. Maursyre brukes til bearbeiding av lær og depilering av dette materialet ved dens avfettende virkning. Deprotonering av maursyre omdannes til formiatanionet HCOO-, som delokaliserer den negative ladningen mellom de to oksygenatomene. Derfor er det et stabilt anion og er ansvarlig for den høye surheten til maursyre.
Veibeskyttelse
I tillegg til de spesifiserte industrielle bruksområdene, brukes maursyrederivater (format) på vinterveier i Sveits og Østerrike for å redusere risikoen for ulykker. Denne behandlingen er mer effektiv enn å bruke bordsalt.
Jeg håper at du med denne informasjonen kan lære mer om maursyre, dens struktur og bruken.