
Dalam kimia terdapat kiasan yang hebat keseimbangan kimia. Ini adalah keadaan bahawa tindak balas kimia dapat dicapai secara terbalik dan di mana tidak terdapat variasi kepekatan kedua-dua reaktan dan produk yang terlibat dalam tindak balas itu sendiri. Keseimbangan kimia dicirikan oleh dinamik dan tidak statik. Ini bermaksud bahawa semua molekul dan atom terus bertindak balas secara berterusan tetapi mengekalkan kepekatan yang sama.
Dalam artikel ini, kami akan memberitahu anda semua yang perlu anda ketahui mengenai keseimbangan kimia dan kepentingannya.
ciri-ciri utama

Apabila kita bercakap mengenai keseimbangan kimia kita bercakap tentang sesuatu yang serupa dengan apa yang berlaku ketika perubahan lulus berlaku. Bahawa perubahan cendawan mungkin bukan penghentian hubungan. Mari kita beri contoh: kita menggunakan cecair yang boleh berada dalam keseimbangan dengan wapnya sendiri, sama seperti pepejal. Kami mewujudkan keseimbangan apabila pepejal juga dapat berada dalam keseimbangan dengan air di sekitarnya ketika ia telah mendakan atau mengkristal.
Keseimbangan kimia sangat penting dalam industri kimia. Dengan cara ini, penambahbaikan sintesis dan hasil dapat diperoleh. Setelah keseimbangan kimia terjalin, tidak ada perubahan atau tindak balas yang lebih lanjut kecuali keseimbangan ini terganggu. Biasanya, ia terganggu oleh tindakan luar. Ini adalah bagaimana sintesis produk diubahsuai dengan beberapa parameter seperti tekanan, isipadu atau suhu. Sekiranya kita terus menerus bermain dengan nilai-nilai parameter ini pada akhirnya kita mencapai keseimbangan yang dihasilkan apabila dapat mencapai pengeluaran maksimum.
Jika tidak, jika kita tidak mengira dengan baik, keseimbangan kimia anda tidak akan mempunyai jumlah produk yang baik dan produk tersebut tidak memuaskan. Iaitu, ia akan menghasilkan hasil yang lebih rendah dan tidak dapat dilaksanakan secara ekonomi. Semua ini lebih berguna jika kita memperkirakannya ke industri kimia dan untuk sebarang sintesis tanpa mengira skala. Jelas sekali, kita harus mengoptimumkan pengeluaran selagi ada pengeluaran pada skala yang lebih besar.
Dalam keseimbangan kimia mungkin terdapat lebih banyak kuantiti produk atau lebih banyak kuantiti reaktan. Semuanya bergantung pada arah perubahan keseimbangan ini. Sekiranya kita mengambil kira semua faktor, kita dapat mengubah keseimbangan kimia ke kedua arah. Perlu diambil kira bahawa perubahan arah ini boleh berlaku selagi tindak balas kimia dapat dipulihkan.
Penjelasan keseimbangan kimia
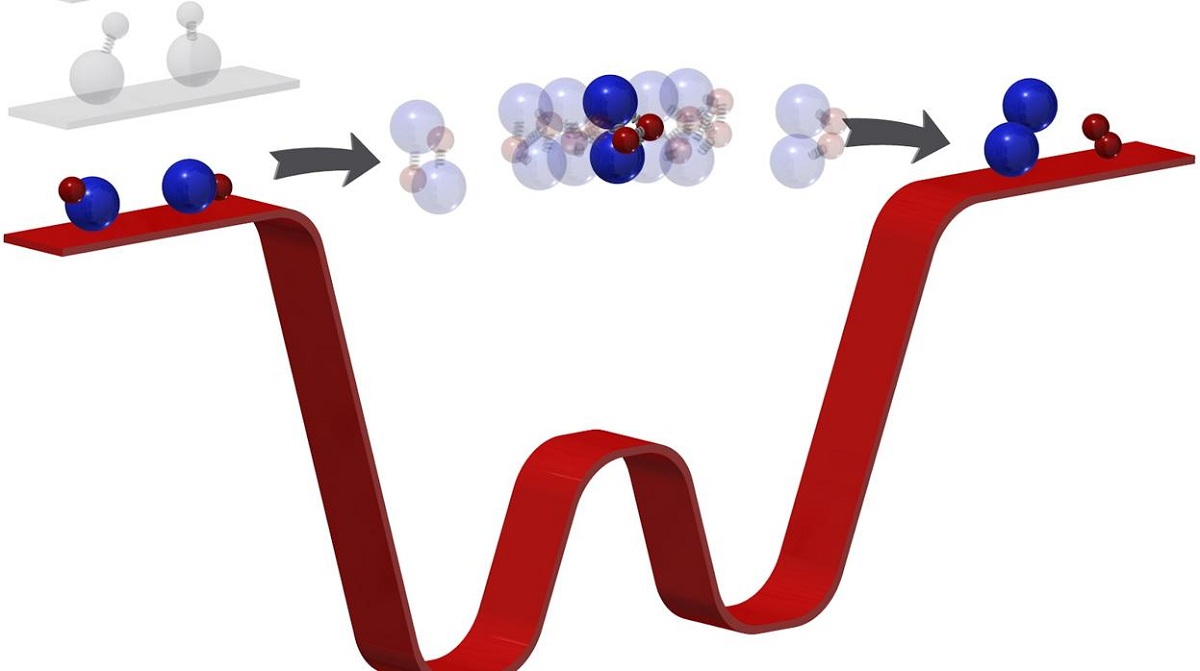
Kami akan menerangkan bagaimana ia berlaku dan apa yang diperlukan untuk mencapai keseimbangan kimia. Perkara pertama adalah melihat apa yang berlaku sebelumnya. Kami akan mempertimbangkan reaksi berikut yang benar-benar boleh dibalikkan. Di sini kita mempunyai nitrogen tetraoksida yang diubah menjadi 2 mol nitrogen dioksida. Mereka berdua adalah gas. Gas pertama yang merupakan reagen tidak berwarna, sementara yang kedua mempunyai warna coklat atau coklat. Sekiranya kita memasukkan sejumlah reagen ke dalam botol atau bekas kecil, Kita akan melihat bahawa ia tidak berwarna sehingga keseimbangan kimia terjalin.
Kepekatan reagen mula menurun secara beransur-ansur apabila tindak balas kimia berlaku dari masa ke masa. Sebahagian daripadanya akhirnya berpisah untuk menghasilkan molekul nitrogen dioksida. Walaupun kepekatannya sama dengan sifar pada awal tindak balas, ia akan mula meningkat ketika reagen mula berasingan.
Walau bagaimanapun, kita bercakap mengenai tindak balas kimia yang boleh diterbalikkan, sehingga sebahagian molekul produk akan bergabung untuk membentuk semula reaktan. Ini bermaksud bahawa kedua-dua reaksi, baik yang langsung dan yang terbalik, akan mempunyai halaju tersendiri.
Kadar tindak balas dalam keseimbangan kimia

Mari kita lihat betapa pentingnya kadar tindak balas dalam keseimbangan kimia. Mula-mula kita mesti tahu bahawa kelajuan penggunaan reagen akan lebih besar daripada kelajuan penggunaan produk. Dengan cara ini, pada mulanya, kerana hanya terdapat tetraoksida nitrogen, beberapa molekul yang terbentuk daripada nitrogen dioksida hampir tidak dapat saling bertemu untuk bertindak balas dengan cara yang berlawanan. Apabila kita telah mencapai saat reaksi, di dalam botol anda dapat melihat bagaimana ia mula berubah menjadi jingga kerana anda mempunyai campuran reaktan dan produk pada masa yang sama.
Sedikit demi sedikit, ketika tindak balas kimia berlangsung, molekul produk akan berada dalam kuantiti yang lebih besar daripada molekul reaktan. Kadar kedua-dua tindak balas, baik langsung dan terbalik, akan terus menyamakan, walaupun kepekatannya berbeza antara satu sama lain semakin banyak. Maksudnya, produk cenderung lebih besar daripada reaktan, jadi kepekatannya akan meningkat sepanjang keseimbangan kimia.
Apabila tindak balas kimia mencapai keseimbangan kimia halaju dan kedua-dua tindak balas sama. Kedua-dua kepekatan juga tetap berterusan kerana kedua-dua tindakan berlaku pada kelajuan yang sama. Sebaik sahaja kuantiti reaktan tertentu dipisahkan, kuantiti yang sama akan dihasilkan semula dengan segera kerana reaksi kuantiti produk yang lain. Inilah sebab mengapa nama keseimbangan kimia diketahui dan benar-benar dinamik. Dan molekul kedua-dua reagen dan produk terus mengambil bahagian dalam tindak balas, walaupun kepekatannya tidak berubah dari masa ke masa.
Sekiranya kita mempunyai kadar tindak balas yang sama tetapi dalam kedua arah, kemungkinan keseimbangan tetap.
Pemalar keseimbangan
Ia tercapai dan selalu sama, selagi faktor seperti suhu stabil. Maksudnya, pemalar keseimbangan kimia akan sama selagi suhunya stabil, tidak kira seberapa banyak nitrogen tetraoxide disuntik ke dalam botol pada mulanya.
Seperti yang anda lihat, keseimbangan kimia cukup penting untuk industri kimia dan untuk pengetahuan penjanaan produk. Saya harap dengan maklumat ini anda dapat mengetahui lebih lanjut mengenai keseimbangan kimia dan kepentingannya.