Dalam bidang kimia kita mempunyai reaksi kimia yang berlaku antara molekul dan atom. Hari ini kita akan membincangkan mengenai hidrolisis. Hidrolisis adalah sejenis tindak balas kimia yang boleh berlaku antara molekul atau ion organik dan organik. Ciri utama hidrolisis adalah bahawa ia melibatkan penyertaan air sehingga ikatan dapat diputuskan.
Dalam artikel ini kami akan memberitahu anda tentang semua ciri dan kepentingan hidrolisis dalam bidang kimia.
Apa itu hidrolisis
Kami bercakap mengenai sejenis tindak balas kimia yang boleh berlaku antara molekul organik dan bukan organik. Syarat penting ialah air mesti dilibatkan sehingga boleh putuskan ikatan molekul ini. Kata hidrolisis berasal dari hidro Yunani, yang bermaksud air dan dari lisis, yang bermaksud pecah. Diterjemahkan dalam bentuk, hidrolisis dapat dikenali sebagai pemecahan air. Dalam kes ini, kita bercakap mengenai pemutusan ikatan beberapa reaktan melalui penyertaan air.
Molekul air terdiri daripada dua atom hidrogen dan satu atom oksigen. Berkat gabungan atom ini, keseimbangan terbentuk antara ion garam asid lemah dan basa. Asid dan basa adalah konsep yang muncul dalam kajian umum kimia dan kimia analitik. Hidrolisis boleh dikatakan sebagai salah satu tindak balas kimia termudah di luar sana. Persamaan umum untuk hidrolisis adalah seperti berikut:
AB + H2O = AH + B-OH
Terdapat beberapa contoh hidrolisis di mana air atau dengan sendirinya tidak dapat memutuskan ikatan kovalen tertentu. Kita ingat bahawa ikatan kovalen adalah ikatan di mana beberapa molekul dengan ciri bukan logam bergabung untuk membentuk molekul baru yang lain. Ikatan yang bergabung dengan mereka dikenali sebagai ikatan kovalen. Apabila air sahaja tidak dapat memutuskan ikatan ini, prosesnya dipercepat atau dikatalisis oleh pengasidan atau alkaliisasi medium. Maksudnya, dengan adanya ion, hidrolisis dapat dikatalisis. Dan ada enzim yang mampu menjadi pemangkin reaksi kimia hidrolisis.
ciri-ciri utama

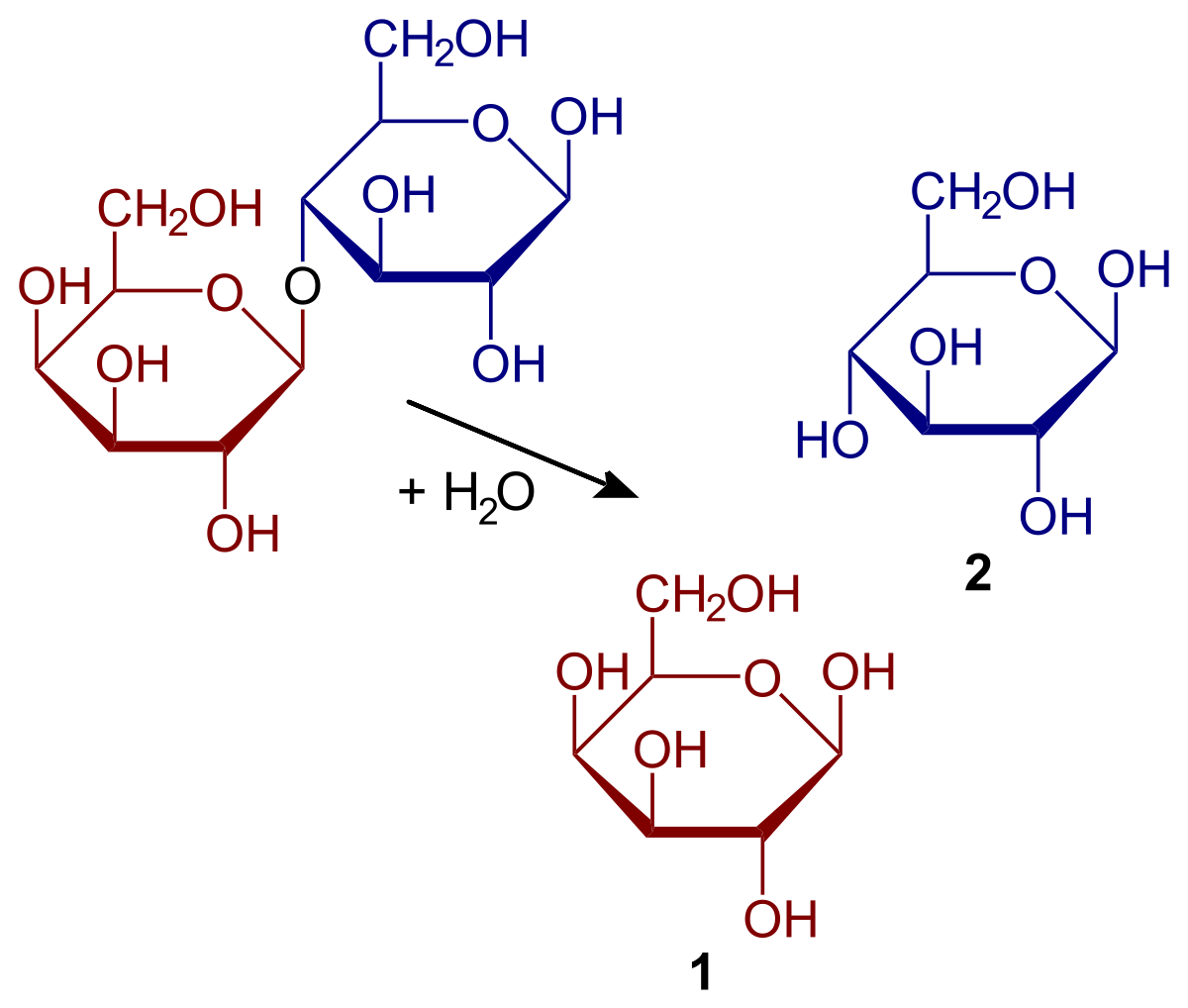
Mari kita lihat apa ciri dan hidrolisis. Jenis tindak balas ini menempati tempat yang istimewa dalam hal biomolekul. Dan ikatan yang menyatukan monomer molekul bersamaan rentan untuk hidrolisis dalam keadaan tertentu. Maksudnya, ikatan kovalen dengan molekul yang dilekatkan dapat diputuskan di hadapan air. Contohnya ialah gula. Gula mampu menghidrolisis untuk memecah polisakarida menjadi monosakarida. Ini berlaku berkat tindakan enzim yang dikenali sebagai glukosidase.
Perlu diingat bahawa bukan sahaja molekul merupakan substrat yang memutuskan ikatan. Air itu sendiri juga retak dan akhirnya memisahkan ion. Air pecah menjadi H + dan OH–, di mana H + berakhir dengan A, dan OH- dengan B. AB dengan itu bertindak balas dengan molekul air, menghasilkan dua produk, AH dan B-OH.
Oleh itu, kita dapat mengatakan bahawa hidrolisis adalah tindak balas kimia yang bertentangan dengan pemeluwapan. Dari pemeluwapan, dua produk bergabung dengan melepaskan molekul kecil. Molekul kecil ini adalah air. Sebaliknya, dalam hidrolisis molekul dimakan, sementara dalam kondensasi molekul elektrolisis ini dimakan, dilepaskan atau dihasilkan.
Untuk menjadikannya lebih mudah difahami, kita akan menerangkan lagi contoh gula. Mari kita anggap bahawa AB adalah sukerosa dimer. Dalam kes ini A mewakili glukosa dan B mewakili fruktosa. Ikatan ini, yang dikenali dengan nama glikosidik, dapat dihidrolisis untuk menghasilkan dua monosakarida yang terpisah dan larutannya. Perkara yang sama berlaku dengan oligosakarida dan polisakarida jika enzim adalah yang bertindak dalam tindak balas.
Kita tahu bahawa tindak balas kimia ini hanya mempunyai satu arah. Ini bermaksud bahawa ia adalah sejenis hidrolisis yang tidak dapat dipulihkan. Sebaliknya, terdapat reaksi hidrolisis yang dapat dipulihkan apabila keseimbangan tercapai.
Contoh tindak balas hidrolisis
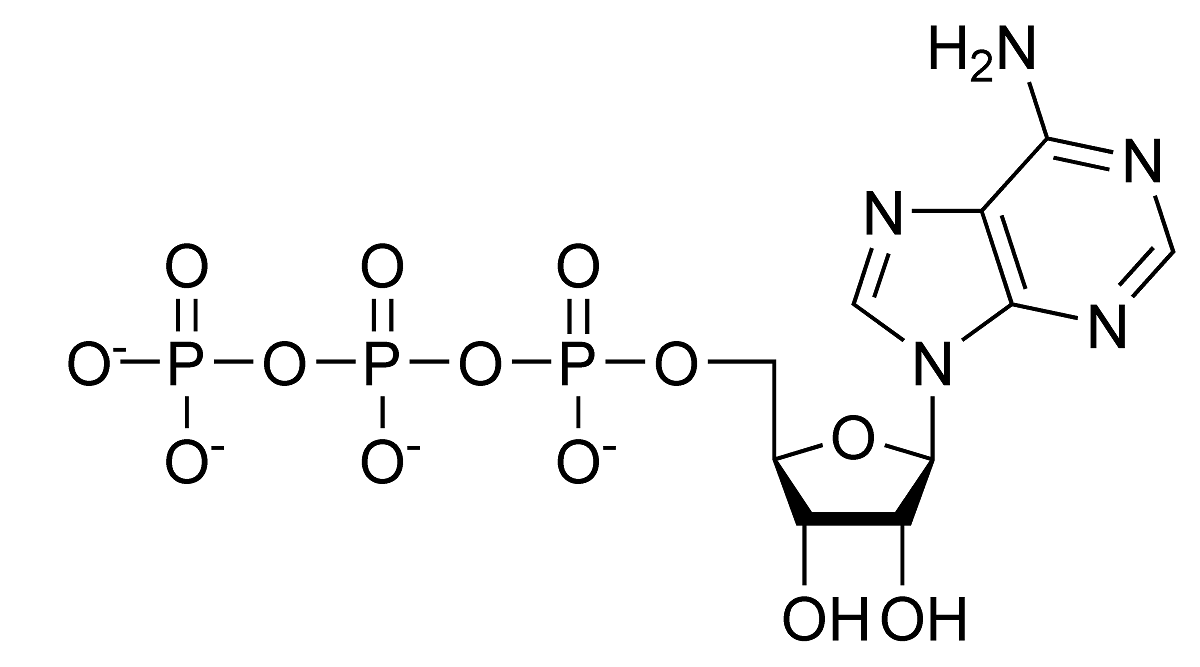
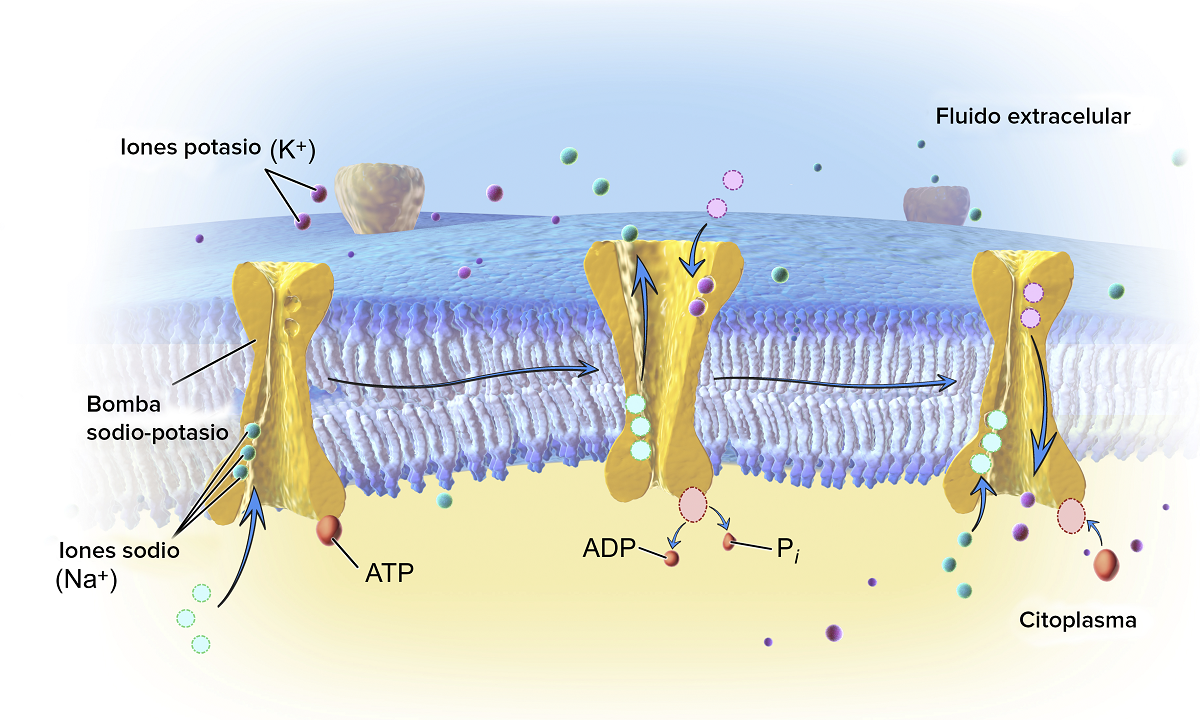
Mari lihat apa contoh utama hidrolisis yang berlaku secara semula jadi. Pertama sekali, lihat reaksi hidrolisis ATP. Kita tahu bahawa molekul ini mempunyai nilai pH yang stabil antara 6.8 dan 7.4. Tetapi, jika nilai pH meningkat menjadi lebih beralkali, ia dapat menghidrolisis secara spontan. Pada makhluk hidup, hidrolisis dikatalisis oleh enzim yang dikenali dengan nama ATPases. Ia adalah sejenis tindak balas kimia eksergonik. Ini bermaksud bahawa entropi ADP lebih besar daripada ATP, jadi variasi tenaga bebas berlaku oleh hidrolisis ATP. Hidrolisis jenis ini menggunakan banyak tindak balas endergonik.
Reaksi berpasangan adalah jenis tindak balas lain di mana hidrolisis berlaku. Dalam beberapa kes, ia digunakan untuk penukaran sebatian A menjadi sebatian B. Contoh hidrolisis yang paling terkenal secara semula jadi berlaku di air. Seolah-olah salah satu molekul air dapat dipecah menjadi ion dan hidrogen proton terikat dengan atom oksigen molekul air yang lain. Ini menimbulkan ion hidronium. Ini dapat disebut lebih dari sekadar hidrolisis sebagai autoionisasi atau autoprotolisis air.
Akhirnya, bahagian lain di mana tindak balas ini dihasilkan dengan cara yang biasa dalam protein. Kita tahu bahawa protein adalah molekul stabil dan untuk mencapai hidrolisis lengkapnya, keadaan ekstrim diperlukan. Kita ingat bahawa protein terdiri daripada asid amino. Walau bagaimanapun, makhluk hidup dikurniakan senjata enzim yang membolehkan hidrolisis protein menjadi asid amino dalam duodenum.
Saya harap dengan maklumat ini anda dapat mengetahui lebih lanjut mengenai hidrolisis dan ciri-cirinya.