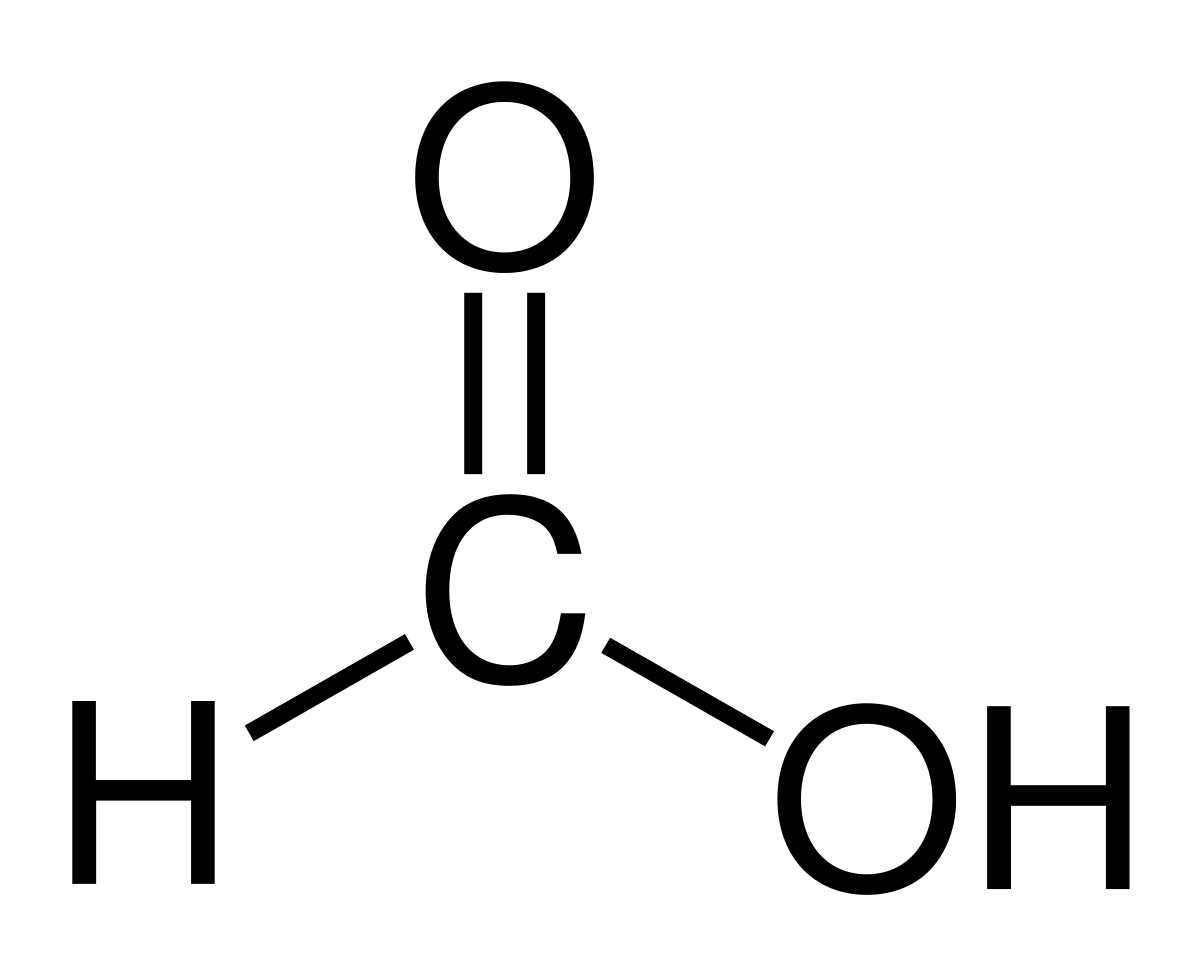
El skudrskābe o Metānskābe ir visvienkāršākais un mazākais savienojums no visām organiskajām skābēm. Tam ir molekulārā formula HCOOH, kurā tikai viens ūdeņraža atoms ir saistīts ar oglekļa atomu. Tās nosaukums cēlies no vārda formica, kas latīņu valodā nozīmē skudra. Tas ir diezgan svarīgs savienojums ķīmijas pasaulē un plaši izmantots mūsdienās.
Šī iemesla dēļ mēs veltīsim šo rakstu, lai pastāstītu jums visu, kas jums jāzina par skudrskābi, tās īpašībām un nozīmi.
galvenās iezīmes
Piecpadsmitā gadsimta dabaszinātnieki atklāja, ka noteikta veida kukaiņi (termicīdi), piemēram, skudras, termīti, bites un vaboles, tie izdala šo savienojumu, kas padara viņu kodumus sāpīgus. Turklāt šie kukaiņi izmanto šo savienojumu kā uzbrukuma, aizsardzības un ķīmisko signālu mehānismu.
Viņiem ir toksiski dziedzeri, kas miglas veidā izvada no organisma šo un citas skābes, piemēram, etiķskābi. Skudrskābe ir stiprāka par etiķskābi (CH3COOH); tādēļ vienāds daudzums skudrskābes, kas izšķīdināts ūdenī, radīs šķīdumu ar zemāku pH līmeni.
Angļu dabaszinātnieks Džons Rejs panāca šī savienojuma izolāciju 1671. gadā, kas iegūts no liela skaita skudru. No otras puses, pirmo veiksmīgo šī savienojuma sintēzi veica franču ķīmiķis un fiziķis Džozefs Gajs-Lussaks, kā reaģentu izmantojot ciānūdeņražskābi (HCN).
skudrskābe dabā

Skudrskābe var pastāvēt sauszemes līmenī, kā biomasas sastāvdaļa vai atmosfērā, piedaloties visdažādākajās ķīmiskajās reakcijās, to var atrast pat pazemē, eļļā vai gāzveida fāzē uz tās virsmas.
Biomasas ziņā kukaiņi un augi ir galvenie šīs skābes ražotāji. Dedzinot fosilo kurināmo, rodas gāzveida skudrskābe; tāpēc automašīnu dzinēji izdala šo skābi atmosfērā.
Tomēr, uz zemes dzīvo daudz skudru, un skudrskābes ražošana starp tām ir tūkstošiem reižu lielāka nekā cilvēka rūpniecībā vienā gadā saražotās metānskābes daudzums. Meža ugunsgrēki ir arī gāzveida skudrskābes avots.
Augstāk, sarežģītajā atmosfēras matricā, notiek fotoķīmiskie procesi skudrskābes sintēzei. Šajā brīdī daudzi gaistošie organiskie savienojumi (GOS) noārdās UV starojuma ietekmē vai tiek oksidēti ar OH radikāļu mehānismu. Bagātīgā un sarežģītā atmosfēras ķīmija ir tālu galvenais metanskābes avots uz Zemes.
Skudrskābes atomu struktūra
Augšējā attēlā parādīta skudrskābes gāzes fāzes dimēra struktūra. Baltās sfēras atbilst ūdeņraža atomiem, sarkanās - skābekļa atomiem, bet melnās - oglekļa atomiem.
Šajās molekulās var redzēt divas grupas: hidroksilgrupa (-OH) un formilgrupa (-CH=O), kas spēj veidot ūdeņraža saites. Šīs mijiedarbības ir OHO tipa, kur hidroksilgrupa ir H donors un formilgrupa ir O donors.
Tomēr H, kas saistīts ar oglekļa atomiem, trūkst šīs spējas. Šīs mijiedarbības ir ļoti spēcīgas, un ūdeņradis OH grupā ir skābāks elektronu deficīta H atoma dēļ; Tādējādi šis ūdeņradis vēl vairāk stabilizē tiltu. Iepriekšminētā rezultātā skudrskābe pastāv kā dimērs, nevis kā atsevišķa molekula.
Temperatūrai pazeminoties, dimērs orientē savas ūdeņraža saites, lai kopā ar citiem dimēriem izveidotu visstabilāko struktūru, kā rezultātā veidojas bezgalīgas metanskābes alfa un beta ķēdes. Šī kristāla struktūra Tas ir atkarīgs no fiziskajiem mainīgajiem lielumiem, kas uz to iedarbojas, piemēram, spiediena un temperatūras.. Tāpēc virkne ir konvertējama. Ja spiediens tiek palielināts līdz galējam līmenim, ķēdes tiek pietiekami saspiestas, lai tās uzskatītu par skudrskābes kristālisku polimēru.
īpašības
Mēs koncentrēsimies uz skudrskābes galveno īpašību aprakstu:
- metānskābe ir bezkrāsains šķidrums istabas temperatūrā ar spēcīgu asu smaku. Tā molekulmasa ir 46 g/mol, kušanas temperatūra ir 8,4ºC un viršanas temperatūra ir 100,8ºC, kas ir augstāka nekā ūdens.
- Sajaucas ar ūdeni un polāriem organiskiem šķīdinātājiem, piemēram, ēteri, acetonu, metanolu un etanolu.
- Gluži pretēji, aromātiskajos šķīdinātājos, piemēram, benzolā un toluolā, tas slikti šķīst, jo skudrskābes struktūrā ir maz oglekļa atomu.
- Tā pKa ir 3,77, kas ir skābāks par etiķskābi, kas izskaidrojams ar to, ka metilgrupa nodrošina elektronu blīvumu oglekļa atomam, ko oksidē divi skābekļa savienojumi. Tā rezultātā nedaudz samazinās protonu skābums (CH3COOH, HCOOH).
- Kad skābe ir deprotonēta, tiek pārveidots par formāta anjonu HCOO-, kas delokalizē negatīvo lādiņu starp diviem skābekļa atomiem. Tāpēc tas ir stabils anjons un ir atbildīgs par skudrskābes augsto skābumu.
Skudrskābes izmantošana
Pārtikas un lauksaimniecības nozare
Tikpat kaitīgs kā metānskābe, to pietiekamā koncentrācijā lieto kā pārtikas konservantu antibakteriālās iedarbības dēļ. Tā paša iemesla dēļ, kā to izmanto lauksaimniecībā, tai ir arī insekticīdas īpašības. Tam ir arī antiseptiska iedarbība uz stiebrzālēm un palīdz novērst gāzu veidošanos lauksaimniecības dzīvniekiem.
Tekstila un apavu rūpniecība
To izmanto tekstilrūpniecībā, lai krāsotu un uzlabotu tekstilizstrādājumus, un tas, iespējams, ir visizplatītākais šīs skābes lietojums. Skudrskābi izmanto ādas apstrādei un šī materiāla depilācijai ar tā attaukošanas darbība. Skudrskābes deprotonēšana pārvēršas par formiāta anjonu HCOO-, kas delokalizē negatīvo lādiņu starp diviem skābekļa atomiem. Tāpēc tas ir stabils anjons un ir atbildīgs par skudrskābes augsto skābumu.
Ceļu satiksmes drošība
Papildus norādītajiem rūpnieciskajiem lietojumiem uz ziemas ceļiem Šveicē un Austrijā tiek izmantoti skudrskābes atvasinājumi (formāts). lai samazinātu negadījumu risku. Šī ārstēšana ir efektīvāka nekā galda sāls lietošana.
Es ceru, ka, izmantojot šo informāciju, jūs varat uzzināt vairāk par skudrskābi, tās struktūru un lietojumiem.