
Ūdens, kam ir dažādi parametri un īpašības, kas ir vairāk vai mazāk svarīgi atkarībā no izmantotā veida. Viens no vissvarīgākajiem ķīmiskajiem parametriem, klasificējot tā kvalitāti, ir ūdens cietība. Lai gan likums neprasa ūdens cietības un tā vērtību lietošanai pārtikā ierobežojumus, šoreiz dažas netiešas attiecības. Iespējams, ka ūdens, kam mums jābūt ar augstu cietību, un norma nenosaka tā vērtību.
Šo iemeslu dēļ mēs veltīsim šo rakstu, lai pastāstītu jums visu, kas jums jāzina par ūdens cietību.
Kāda ir ūdens cietība

Tā kā likums neierobežo dzeramā ūdens cietību, tieši zinātniekiem ir jānovērtē, kādas ir sekas, dzerot ūdeni ar lielu cietību. Šis ūdens parametrs ir dažādas sekas daudzos ikdienas procesos tāpat kā to izmanto personīgai mazgāšanai vai veļas mazgāšanai. Viena no īpašībām, pēc kuras var klasificēt ūdens kvalitāti, ir tās cietība. Ja mēs izmantosim ūdeni apūdeņošanai, jūs noteikti esat vairākkārt redzējis, ka dažiem augiem nepieciešama īpaša ūdens cietība.
Ūdens cietība tiek definēta kā kopējā tajā esošo kalcija un magnija jonu koncentrācija. Šie divi joni ir dzīvi katijoni, un tie visbiežāk sastopami dabiskajā ūdenī. Tas ir, ūdens cietību varētu definēt kā visu tajā esošo daudzvērtīgo katjonu summa, lai gan magnija plakātam ir daudz svarīgāka ūdens globālā cietība.
Mēs bieži konstatējam, ka ūdens cietību nosaka kā kalcija karbonāta masu un mēra miligramos uz litru šķīduma. Tas nenozīmē, ka viss cietajā ūdenī esošais kalcijs nāk no kalcija karbonāta. Vienkārši ar līgumu parasti izturas tā, it kā tas būtu. Lai aprēķinātu ūdens cietību, koeficientus izmanto attiecībā uz kalcija masu un mg ar kalcija karbonāta masu. Ja dalām attiecības starp tām ar 10, mums var būt ļoti izmantota vienība. Tā ir vienība, kurā mēra ūdens cietību. Tos sauc Francijas hidrimetriskie grādi, kas pazīstami kā GHF vai ºfH. Ir arī citas vienības, kas norāda ūdens cietību, taču tās ir mazāk izplatītas.
Ūdens cietības vērtības
Ja ūdens ir ļoti salds vai ļoti mīksts, tā cietības vērtības būs zemākas par 7ºfH. Šī vērtība norāda, ka katrā litrā ūdens to koncentrācija ir 70 miligrami kalcija karbonāta. No otras puses, mums būs ļoti ciets ūdens, ja tā daudzums būs lielāks par 54ºfH vai kāds ir bijis 540 miligramu kalcija karbonāta koncentrācija uz katru litru ūdens.
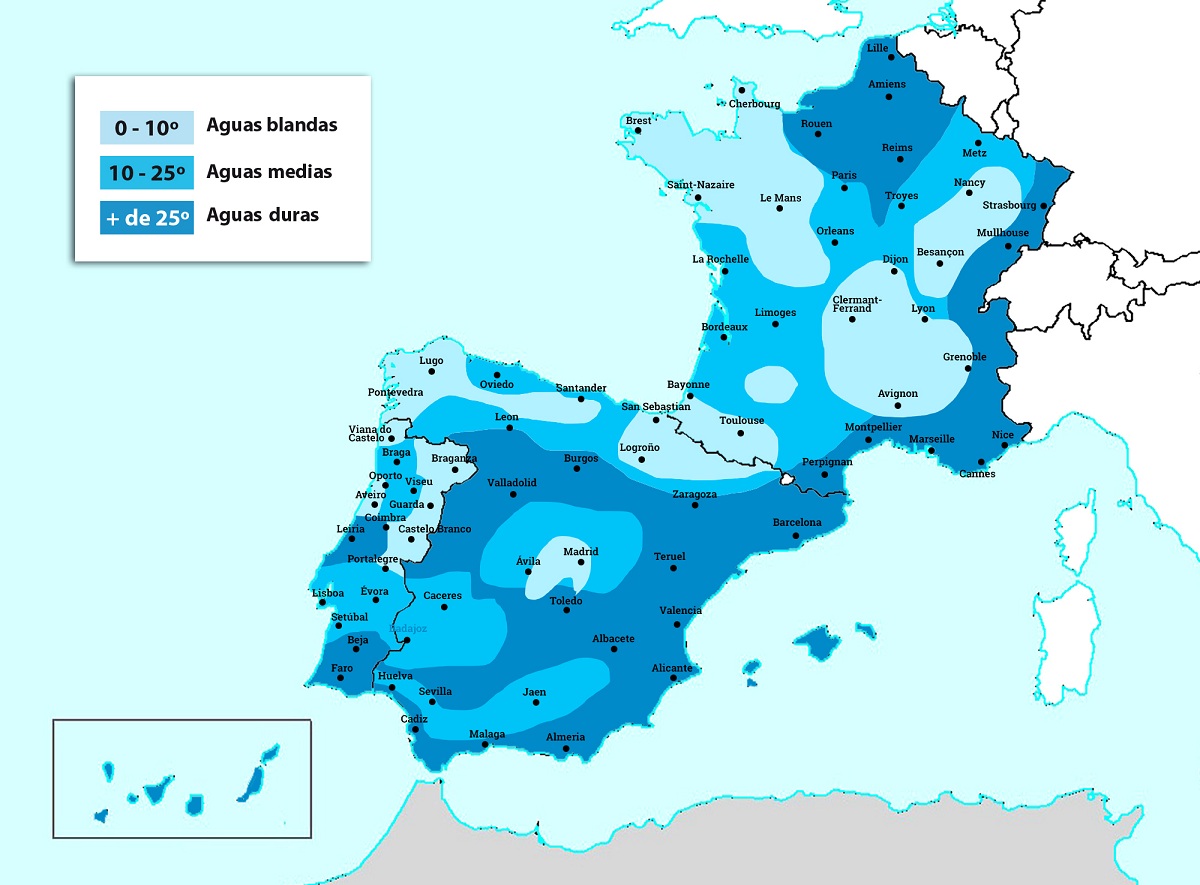
Ja analizējam Spānijas ūdeņus, redzam, ka cietība ir ļoti dažāda. Ūdeņos, kuru galvenais mērķis ir cilvēku patēriņš, mēs atrodam lielu daudzumu cietības. Piemēram, dažās provincēs, piemēram, Segovijā vai Madridē, cietības vērtības ir aptuveni 5ºH, savukārt citās vietās, piemēram, Almerijā, tā var sasniegt 60. Svarīgi ir zināt, kāda negatīva ietekme uz ķermeni var būt cietajam ūdenim.
Bikarbonātu klātbūtne ūdenī nozīmē, ka karsējot var veidoties kalcija karbonāta nogulsnes. Tā rezultātā veidojas kaļķainas garozas. Protams, jūs jau to parasti zināt kā kaļķi. Sarunvalodā kaļķi lieto, lai apzīmētu šos baltos plankumus, kas veidojas izlietņu tuvumā vai uz dušas ekrāna. Šis kaļķis nenozīmē, ka tas nāk tieši no padeves ūdens, bet tā ir ķīmiska reakcija, kas notiek starp kalciju un ziepēm. Ūdens cietība ne tikai ietekmē tīrīšanas problēmas, bet arī rūpnieciskajā vidē rada cietas nogulsnes, kas var radīt problēmas un bojājumus katlos, dzesēšanas torņos un citā aprīkojumā.
Kaļķainas garozas parasti tiek noņemtas, izraisot pretēju ķīmisko reakciju uz iepriekšējo. Tas nozīmē, ka tā atkal veidojas šķīstošā kalcijā un bikarbonātā. Jūs varat izmantot vāju skābi, piemēram, etiķskābe (mēs to varam atrast etiķī) vai citronskābe (mēs to varam atrast citronu sulā). Šī iemesla dēļ lielākās daļas kaļķiem izmantoto tīrīšanas līdzekļu pamatā ir produkts ar nedaudz skābu pH.
Cietā ūdens negatīvā ietekme un kā to novērst
Ja mēs ejam uz sadzīves vidi, mēs redzam, ka cietajam ūdenim ir tādas negatīvas sekas kā kraupu uzkrāšanās katlos, kafejnīcās, ūdensvados un sildītājos. Tāpēc šo atlikumu noņemšanai ir nepieciešams izmantot lielāku daudzumu ziepju un mazgāšanas līdzekļu. Ja mēs izmantojam ziepes, lai varētu likvidēt kanāla paliekas, mums tas ir jāzina tie ir taukskābju sārmu metālu karboksilāti. Tas ir tāpēc, ka kalcijs spēj tieši reaģēt ar ziepēm. Jūs varat viegli redzēt reakciju, jo veidojas nešķīstoši gabali.
Kas palīdz iznīcināt ziepju īpašības, ir to spēja putot. Jo cietāks būs ūdens, jo lielāks šampūna vai želejas daudzums mums būs nepieciešams, lai spētu panākt tādas pašas putas. Problēma ar vairāk mazgāšanas līdzekļu lietošanu ir palielināti ekonomiskie izdevumi un ES piesārņojums ūdens Vēl viens cietā ūdens trūkums ir tas, ka drēbju mazgāšanai nepieciešams arī vairāk mazgāšanas līdzekļu.
Lai noņemtu lieko cietību no ūdens, ir nepieciešamas vairākas metodes. Pats vienkāršākais ir ūdens sildīšana. Ūdens cietību var novērst tikai sildot, ja tā ir tā saucamā īslaicīgā cietība. Pagaidu cietība ir tāda, ka kalcija karbonāts ir kalcija bikarbonāta formā. Tomēr šī metode nav laba, jo kaļķi tiek uzglabāti caurulēs un ūdens sildītājos. Atkaļķošanai vislabāk ir izmantot dažādas ķīmiskas vielas. Parasti tie ir sārma metālu karbonāti, kas palīdz radīt ķīmisku reakciju.
Es ceru, ka ar šo informāciju jūs varat uzzināt vairāk par ūdens cietību.
