
L'aigua que tenen diversos paràmetres i característiques que són més o menys importants depenent de l'ús que es elevada. Un dels paràmetres químics més importants a l'hora de classificar la seva qualitat és la duresa de l'aigua. Tot i que la llei no exigeix cap límit per a la duresa de l'aigua i els seus valors en el consum humà, si que aquest cop algunes relacions indirectes. És possible que l'aigua que haguem tingui dureses elevades i la norma no estableix cap valor d'això.
Per aquestes raons, dedicarem aquest article a explicar-tot el que has de saber sobre la duresa de l'aigua és la seva importància.
Què és la duresa de l'aigua

Atès que la llei no limita la duresa en l'aigua potable, són els científics els que han d'avaluar quines són les conseqüències de beure una aigua amb alta duresa. Aquest paràmetre de l'aigua té diverses conseqüències en gran quantitat de processos quotidians com ho és el seu ús per al rentat personal o la bugada. Una de les característiques per la qual es pot classificar la qualitat de l'aigua és la duresa de la mateixa. Si anem a utilitzar l'aigua per a regar, segurament hauràs vist en nombroses ocasions que en determinades plantes necessiten una duresa de l'aigua en concret.
Es defineix la duresa d'l'aigua com a la concentració total d'ions de calci i de magnesi presents. Aquests dos ions són cations visqui lents i són els que més es troben a l'aigua natural. És a dir, es podria definir a la duresa de l'aigua com la suma de tots els cations polivalents que té, Tot i que el cartell magnesi tinguin molta més important la duresa global d'l'aigua.
Freqüentment trobem que la duresa de l'aigua es determina com la massa de carbonat càlcic i es mesura en mil·ligrams per cada litre de dissolució. Això no vol dir que tot el calci presentin una aigua dura provingui de carbonat càlcic. Simplement el conveni se sol tractar com si així fos. Per poder calcular la duresa d'una aigua s'utilitzen els coeficients en relació existent entre la massa de l'calci i de l'mg amb la massa de l'carbonat càlcic. Si dividim per 10 la relació entre ells, podem tenir una unitat molt utilitzada. És la unitat en la qual es mesura la duresa de l'aigua. Se li diuen graus Hidrotimétricos francesos coneguts com GHF o ºfH. També hi ha altres unitats per indicar la duresa de l'aigua però són menys esteses.
Valors de la duresa de l'aigua
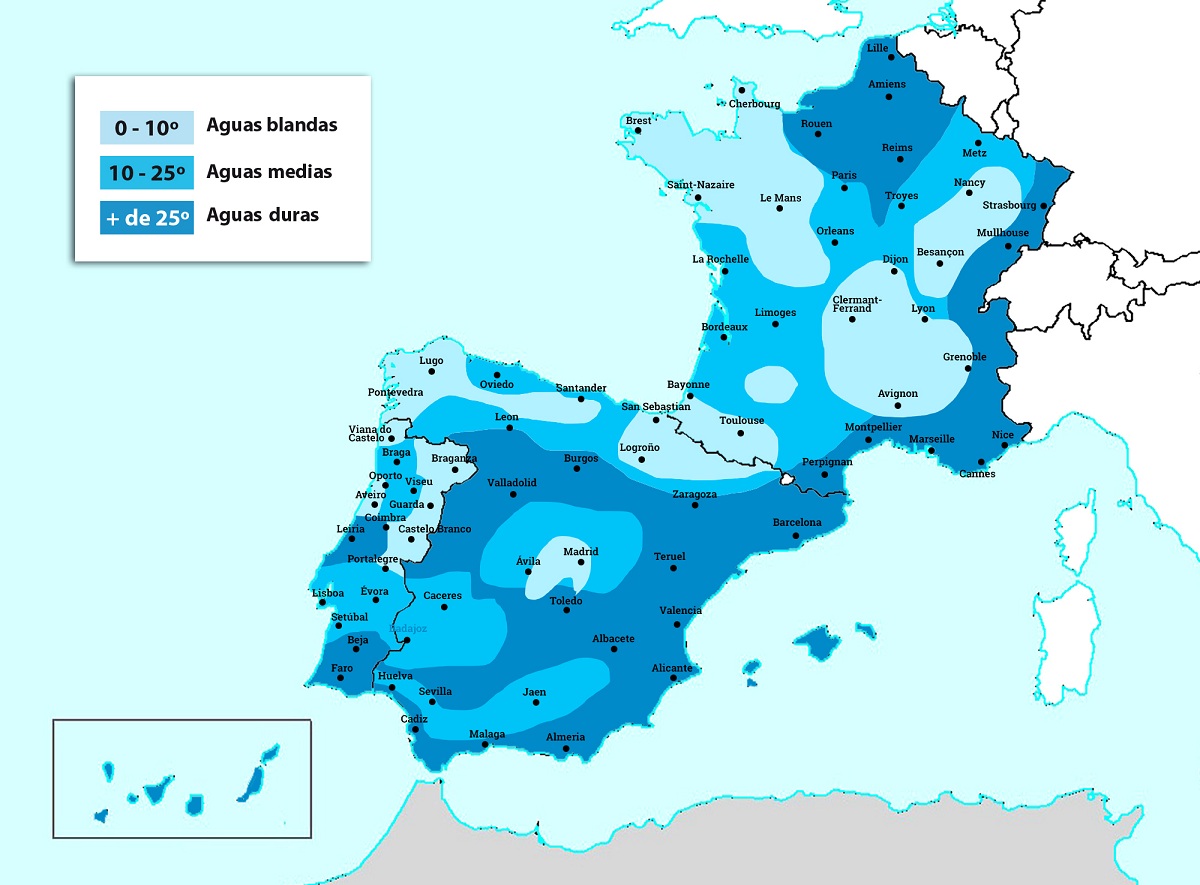
Si una aigua és molt dolça o molt tova tindrà valors de duresa inferior a 7ºfH. Aquest Valor indica que tenen una concentració de 70 mil·ligrams de carbonat càlcic per cada litre d'aigua. D'altra banda, tindrem una aigua molt dura si presenta una quantitat més gran de 54ºfH o el que ve sent una concentració de 540 mil·ligrams de carbonat càlcic per cada litre d'aigua.
Si analitzem les aigües espanyoles veiem que hi ha una gran varietat de dureses. En les aigües que s'administren la destinació principal és el consum humà, trobem gran quantitat de varietat en les dureses. Per exemple, algunes províncies com Segòvia o Madrid tenen valors de duresa al voltant de 5ºfH, mentre que en altres llocs com Almeria pot arribar a assolir els 60. L'important és conèixer quins efectes negatius pot tenir l'aigua dura en l'organisme.
La presència de bicarbonats en l'aigua fa que, quan es calenta, es poden formar precipitats de carbonat càlcic. Això dóna lloc a la formació de crostes calcàries. Segurament ja ho conegueu comunament com la calç. En el llenguatge col·loquial s'utilitza la calç per referir-se a aquestes taques blanques que es formen prop dels lavabos o en la mampara de la dutxa. Aquesta calç no vol dir que provingui directament de l'aigua de l'subministrament, sinó que és una reacció química que es produeix entre el calci i el sabó. La duresa de l'aigua no només té repercussió en problemes de neteja, sinó que també es produeix el dipòsit en sòlid en entorns industrials que pugui arribar a produir problemes i avaries en calderes, torres de refredament i altres equips.
Les crostes calcària se solen eliminar provocat la reacció química inversa l'anterior. És a dir, perquè es formi novament en calci soluble i bicarbonat. Es pot emprar un àcid feble com ho és l'àcid acètic (el podem trobar en el vinagre) o àcid cítric (el podem trobar en el suc de llimona). Per això, la majoria dels productes de neteja que s'utilitzen per a la calç es basen en un producte amb un pH lleugerament àcid.
Efectes negatius de l'aigua dura i com eliminar-la
Si ens anem a l'àmbit domèstic, veiem que l'aigua dura té efectes negatius com ho és l'acumulació de crostes en calderes, cafeteries, conductes d'aigua i escalfadors. Això fa que sigui necessari utilitza una major quantitat de sabó i detergent per eliminar aquestes restes. Si utilitzem sabons per poder eliminar les restes de canal, hem de saber que són carboxilats de metalls alcalins procedents d'àcids grassos. Això és a causa que el calci és capaç de reaccionar directament amb el sabó. Es pot veure fàcilment la reacció ja que es formen uns grumolls insolubles.
El que ajuda a destruir les propietats de l'sabó és la seva capacitat per poder formar escumes. Mentre més dura serà l'aigua, més quantitat de xampú o gel necessitarem per poder aconseguir la mateixa escuma. El problema a utilitzar més de detergent és el major despesa econòmica i la contaminació de l' aigua. Una altra dels desavantatges de l'aigua dura és que també cal major quantitat de detergent per rentar la roba.
Per eliminar l'excés de la duresa de l'aigua es necessiten diversos mètodes. El més bàsic és escalfar l'aigua. La duresa d'una aigua només es pot eliminar per escalfament si es tracta de l'anomenada duresa temporal. La duresa temporal és aquella en aquell carbonat càlcic es troba en forma de bicarbonat càlcic. No obstant això, aquest mètode no és bo ja que s'emmagatzema la calç en els conductes i escalfadors d'aigua. El millor és utilitzar diversos productes químics per a la descalcificació. Aquests solen ser els carbonats d'un metall alcalí que ajuda a produir una reacció química.
Espero que amb aquesta informació puguin conèixer més sobre la duresa de l'aigua.
