水是我們賴以生存的要素,要讓地球上的生命如今天所知。 這 水分子 它由兩個氫原子和一個氧原子通過共價鍵連接而成。 這意味著氫的兩個原子和氧的一個原子相互結合,這是因為它們之間共享電子。 水分子的分子式為H2O。 水分子具有許多特徵,而且由於它,許多過程才引起了生命的發展。
因此,我們將專門為您介紹有關水分子的所有知識。
水分子分析
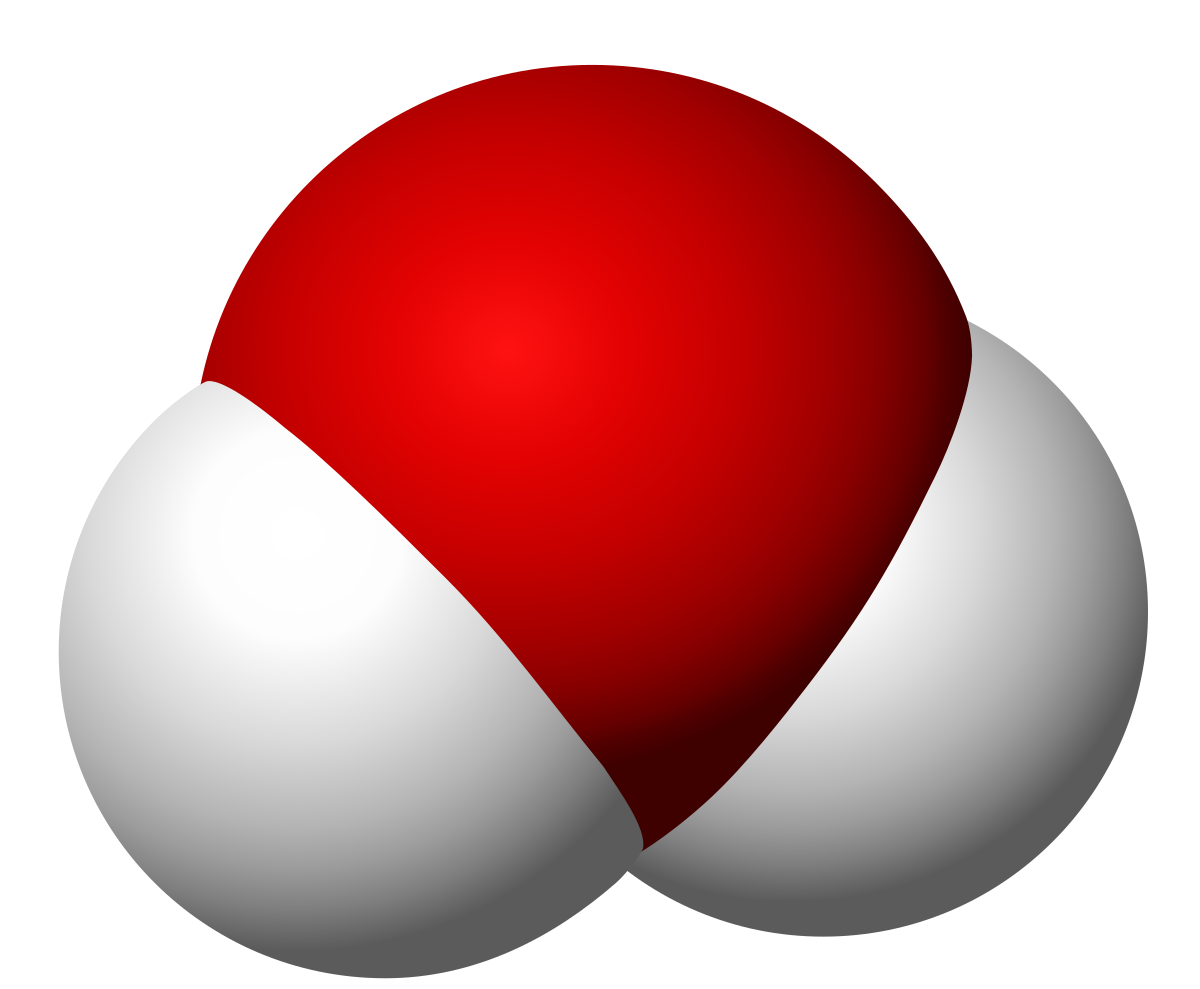
如果我們分析這個分子,我們可以看到氫和氧之間的共價鍵的連接角從104.5度開始。 這可以通過光譜分析和X射線分析來實現,氫和氧原子之間的平均距離為 是96.5 pm,或者說是9.65•10-8毫米。
這些距離無法與人眼看到的任何東西相比。 水分子中電子的排列傳達了電氣不對稱性,因為氫和氧之間存在不同程度的電負性。 我們稱電負性為 原子吸引共價鍵共享電子的能力。 我們記得,共價鍵是在兩個非金屬原子之間建立的。
由於氧比氫具有更大的電負性,因此電子比氫原子更可能靠近氧原子。 這是因為電子帶負電。 電子主要到達氧原子的事實使氫原子具有一定的正電荷。 該電荷稱為正偏電荷。 氧的負電荷稱為負部分電荷。
靠近兩個原子的正負電子之間的差異使水分子成為極性分子。 即,該分子的一部分具有負極,另一部分具有正極。 儘管整個分子是中性的,但其所有的理化和生物學特性都是通過這種極性特性獲得的。
分子之間的相互作用
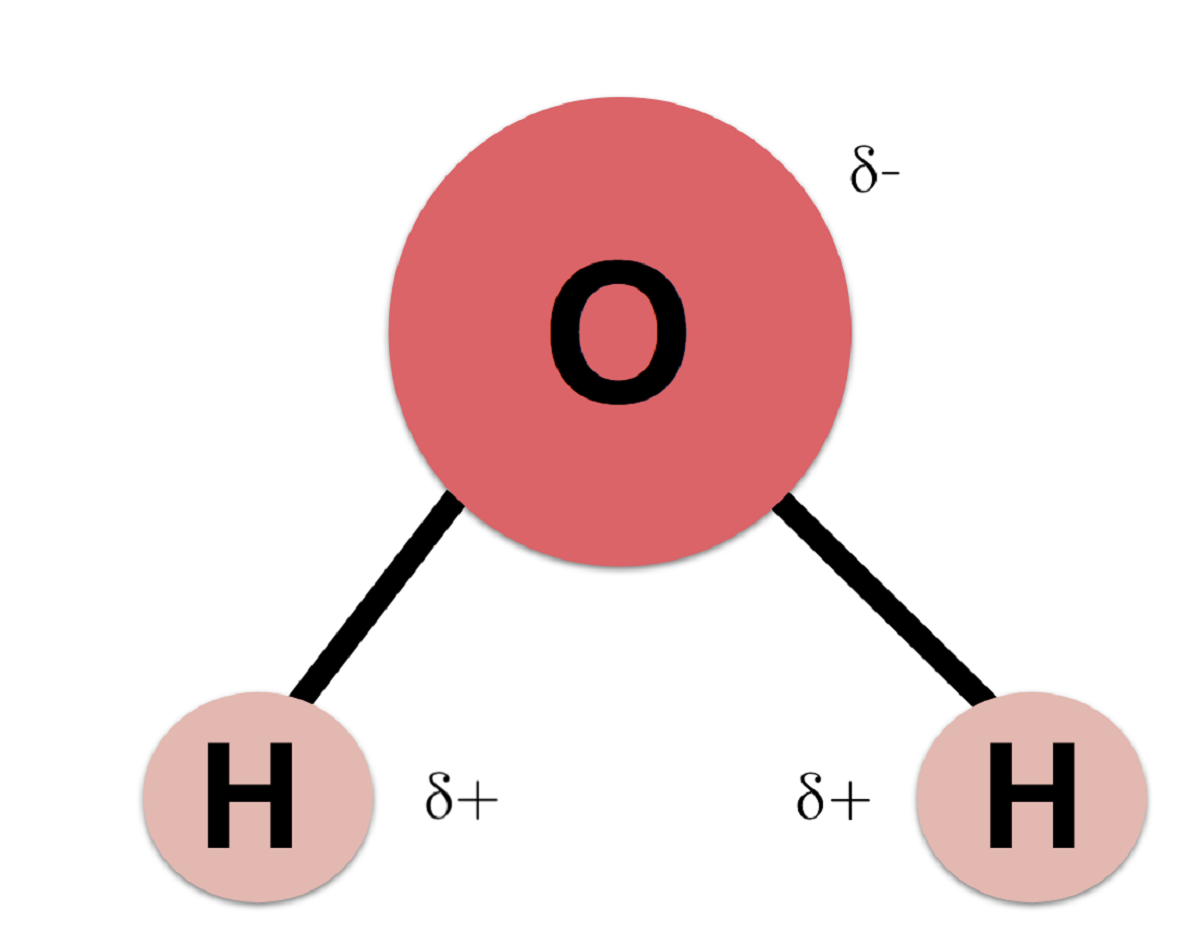
當幾個水分子彼此非常接近時,它們能夠分別在分子的氧原子之間建立牽引力。 這是因為氧具有負的部分電荷,而氫之一具有正的部分電荷。 因此,一個水分子的正部分被另一水分子的負部分吸引。 分子之間的這種相互作用稱為氫源。 這些分子發生很多變化,因為它們的排列方式 每個水分子能夠與另外4個分子締合。 這種相互作用與冰發生。
氫之間的鍵是由於存在一個帶有負部分電荷的原子和一個帶有正部分電荷的氫的事實而發生的。 這使得鏈接不是水獨有的。 這些相互作用鍵還存在於其他含有蛋白質和DNA的分子中的氮,氟和氫中。
讓我們看看水分子的物理化學特性是什麼。 在這些特性和特徵中,我們可以強調容量和溶劑。 我們一定不能忘記,水被認為是通用溶劑。 水分子的另一個特徵是其高比熱和汽化熱。 它也具有很大的內聚力和粘附力,異常密度,並且起化學試劑的作用。
如果我們利用水的特性,我們會發現由於其極性特性,它能夠在其中分散大量化合物。 正如我們之前提到的,儘管整個分子是中性的,但實際上它有一個正部分和一個負部分 它提供了生命所必需的水的理化特性。 因此,它可與鹽和其他離子物質(水分子在其中定向其極性)一起使用。 極的方向是兩個離子的電荷的函數,負極位於一側,正極位於另一側。 例如,對於極性物質(例如乙醇),水以類似的方式起作用。 它與具有相反符號的另一極相對。
水分子的性質
水分子具有高的比熱。 該比熱僅是需要管理的熱量 一克水可以將其溫度升高一度。 另一方面,我們有汽化熱。 這是必須施加到一克液體中的蒸汽量,這樣它才能轉化成一克蒸汽。 我們知道,由於連接氫原子的鍵,水分子具有很高的比熱和汽化率。 也就是說,為了將水的溫度升高一度,所有分子都需要增加其振動。 為此,它們會破壞氫鍵,使它們可以將一克液態水傳遞到一克蒸汽水中。
它具有高的汽化熱值的事實是由於它能夠通過。 水分子的另一個特徵是內聚力。 問題是兩個分子必須結合在一起的趨勢。 再次由於水分子的氫鍵,內聚力很高。 加入是 兩個不同分子相互結合的趨勢。 這使得水分子對離子和極性化合物具有高附著力。 這是當水粘在不同表面上時發生的應用程序。
我希望藉助這些信息,您可以了解有關水分子的更多信息。