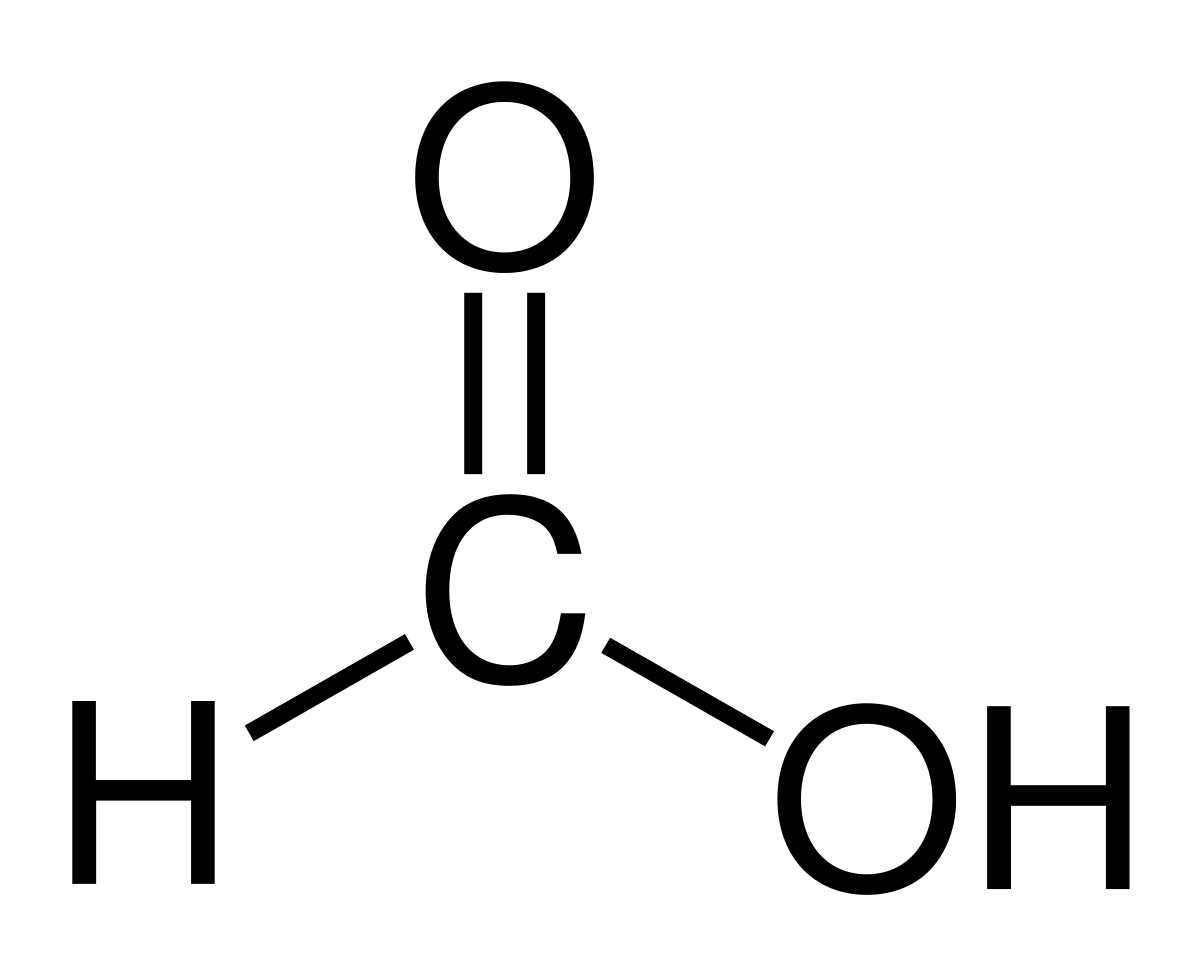
El Мурашина кислота o Метанова кислота — найпростіша і найменша сполука з усіх органічних кислот. Він має молекулярну формулу HCOOH з лише одним атомом водню, зв’язаним з атомом вуглецю. Його назва походить від слова formica, що на латині означає мураха. Це досить важлива сполука у світі хімії і широко використовується сьогодні.
З цієї причини ми збираємося присвятити цю статтю тому, щоб розповісти вам все, що вам потрібно знати про мурашину кислоту, її характеристики та важливість.
ключові особливості
Натуралісти XV століття виявили, що деякі види комах (терміциди), такі як мурахи, терміти, бджоли та жуки, вони виділяють цю сполуку, яка робить їхні укуси болючими. Крім того, ці комахи використовують цю сполуку як механізм атаки, захисту та хімічної сигналізації.
У них є токсичні залози, які виганяють цю та інші кислоти, наприклад, оцтову, з організму у вигляді туману. Мурашина кислота сильніша за оцтову кислоту (CH3COOH); тому однакова кількість мурашиної кислоти, розчиненої у воді, призведе до отримання розчину з нижчим pH.
Англійський натураліст Джон Рей досягнув виділення цієї сполуки в 1671 році, видобуваються з великої кількості мурах. З іншого боку, перший успішний синтез цієї сполуки здійснив французький хімік і фізик Жозеф Гей-Люссак з використанням синильної кислоти (HCN) як реагенту.
мурашина кислота в природі

Мурашина кислота може існувати на земних рівнях, як компонент біомаси або в атмосфері, беручи участь у широкому спектрі хімічних реакцій, її навіть можна знайти під землею, в нафті або в газоподібній фазі на її поверхні.
За біомасою комахи та рослини є основними виробниками цієї кислоти. При горінні викопного палива утворюється газоподібна мурашина кислота; тому автомобільні двигуни викидають цю кислоту в атмосферу.
Проте, на землі живе багато мурах, а виробництво мурашиної кислоти між ними в тисячі разів перевищує кількість метанової кислоти, виробленої промисловістю людини за один рік. Лісові пожежі також є газоподібним джерелом мурашиної кислоти.
Вище, в складній атмосферній матриці, відбуваються фотохімічні процеси синтезу мурашиної кислоти. У цей момент багато леткі органічні сполуки (ЛОС) розкладаються під дією УФ-випромінювання або окислюються за механізмом радикалів ОН. Багата і складна хімія атмосфери безсумнівно головне джерело метанової кислоти на Землі.
Будова атома мурашиної кислоти
На малюнку вище показана структура газофазного димеру мурашиної кислоти. Білі кулі відповідають атомам водню, червоні — атомам кисню, а чорні — атомам вуглецю.
У цих молекулах можна побачити дві групи: гідроксил (-OH) і формил (-CH=O), які здатні утворювати водневі зв’язки. Ці взаємодії відносяться до типу OHO, де гідроксильна група є донором H, а формильна група є донором O.
Однак Н, зв’язаний з атомами вуглецю, не має цієї здатності. Ці взаємодії дуже сильні, і водень у групі ОН є більш кислим через електронодефіцитний атом Н; таким чином, цей водень додатково стабілізує міст. У результаті вищесказаного мурашина кислота існує як димер, а не як окрема молекула.
При зниженні температури димер орієнтує свої водневі зв’язки, щоб створити найбільш стабільну структуру з іншими димерами, в результаті чого утворюються нескінченні альфа- та бета-ланцюги метанової кислоти. Це кристалічна структура Це залежить від фізичних змінних, які діють на нього, таких як тиск і температура.. Тому ланцюг конвертований. Якщо тиск збільшується до екстремальних рівнів, ланцюги стискаються достатньо, щоб вважатися кристалічним полімером мурашиної кислоти.
Властивості
Ми зосередимося на описі основних властивостей мурашиної кислоти:
- метанова кислота безбарвна рідина кімнатної температури з сильним різким запахом. Він має молекулярну масу 46 г/моль, температуру плавлення 8,4ºC і температуру кипіння 100,8ºC, що вище, ніж у води.
- Змішується з водою та полярними органічними розчинниками, такими як ефір, ацетон, метанол та етанол.
- Навпаки, в ароматичних розчинниках, таких як бензол і толуол, він погано розчиняється, оскільки мурашина кислота має в своїй структурі мало атомів вуглецю.
- Він має рКа 3,77, яка більш кисла, ніж оцтова кислота, що можна пояснити тим, що метильна група забезпечує електронну густину атому вуглецю, окисленому двома киснями. Це призводить до незначного зниження кислотності протонів (CH3COOH, HCOOH).
- Після депротонування кислоти, перетворюється на формиат-аніон HCOO-, що делокалізує негативний заряд між двома атомами кисню. Тому він є стабільним аніоном і відповідає за високу кислотність мурашиної кислоти.
Використання мурашиної кислоти
Харчова та сільськогосподарська промисловість
Так само шкідливо, як метанова кислота, його використовують у достатніх концентраціях як харчовий консервант завдяки його антибактеріальній дії. З тієї ж причини, по якій він використовується в сільському господарстві, він також володіє інсектицидними властивостями. Він також має антисептичну дію на трави та допомагає запобігти кишковим газам у сільськогосподарських тварин.
Текстильна та взуттєва промисловість
Вона використовується в текстильній промисловості для фарбування та очищення текстилю і, ймовірно, є найпоширенішим використанням цієї кислоти. Мурашину кислоту використовують для обробки шкіри та депіляції цього матеріалу його знежирюючу дію. Депротонування мурашиної кислоти перетворюється на формуат-аніон HCOO-, який делокалізує негативний заряд між двома атомами кисню. Тому він є стабільним аніоном і відповідає за високу кислотність мурашиної кислоти.
Безпека дорожнього руху
Крім зазначеного промислового використання, похідні мурашиної кислоти (формат) використовуються на зимових дорогах у Швейцарії та Австрії щоб зменшити ризик нещасних випадків. Таке лікування більш ефективне, ніж використання кухонної солі.
Я сподіваюся, що завдяки цій інформації ви зможете дізнатися більше про мурашину кислоту, її структуру та використання.