Ang tubig ay isang sangkap na kailangan nating mabuhay at upang magkaroon ng buhay sa mundo tulad ng alam natin ngayon. Ang Molekyul ng tubig Ito ay binubuo ng dalawang hydrogen atoms at isang oxygen atoms na sumali sa isang covalent bond. Nangangahulugan ito na ang dalawang atomo ng hydrogen at ang isa sa oxygen ay nagkakaisa salamat sa pagbabahagi nila ng mga electron sa pagitan nila. Ang formula para sa Molekyul ng tubig ay H2O. Maraming mga katangian na mayroon ang water Molekul at ito ay salamat dito na maraming mga proseso na nagbibigay ng pag-unlad ng buhay.
Samakatuwid, ilalaan namin ang artikulong ito upang sabihin sa iyo ang lahat ng kailangan mong malaman tungkol sa Molekyul ng tubig.
Pagsusuri ng Molekyul ng tubig
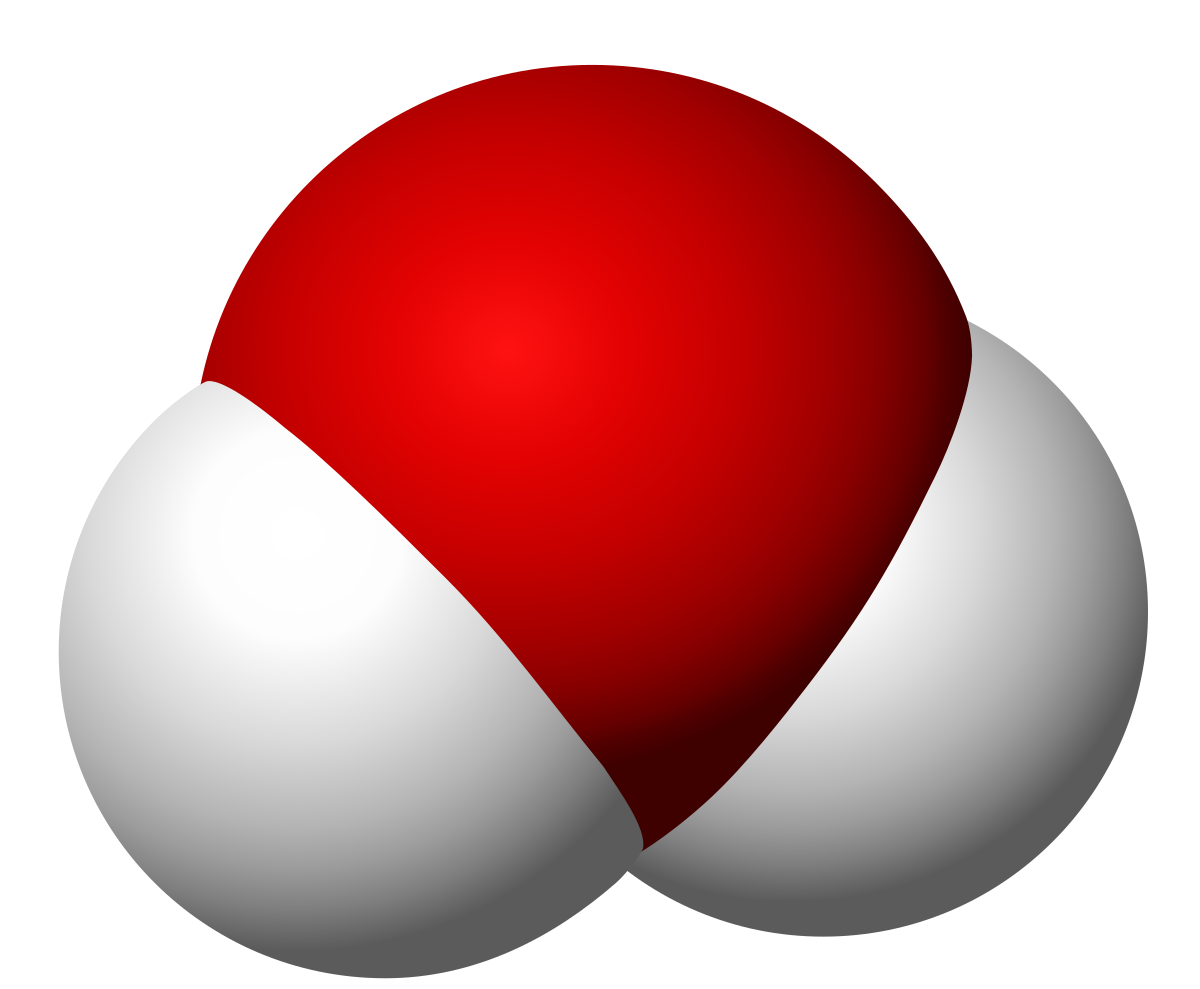
Kung pag-aralan natin ang Molekyul na ito maaari nating makita na ang anggulo ng pagkakabit ng covalent bond sa pagitan ng hydrogen at oxygen mula 104.5 degree. Maaari itong makamit sa pamamagitan ng pagsusuri ng spectroscopic at X-ray. Ang average na distansya sa pagitan ng hydrogen at oxygen atoms ay ng 96.5 pm o, ano ang pareho, 9.65 • 10-8 millimeter.
Ang mga distansya na ito ay hindi maikukumpara sa anumang nakikita ng mata ng tao. Ang pag-aayos ng mga electron sa Molekyul ng tubig ay kung ano ang nakikipag-usap sa electrical asymmetry dahil mayroong iba't ibang antas ng electronegativity sa pagitan ng hydrogen at oxygen. Tinatawag namin ang electronegativity sa ang kakayahan ng isang atom na akitin ang mga electron na ibinabahagi sa isang covalent bond. Naaalala namin na ang isang covalent bond ay isa na itinatag sa pagitan ng dalawang mga hindi-metal na atomo.
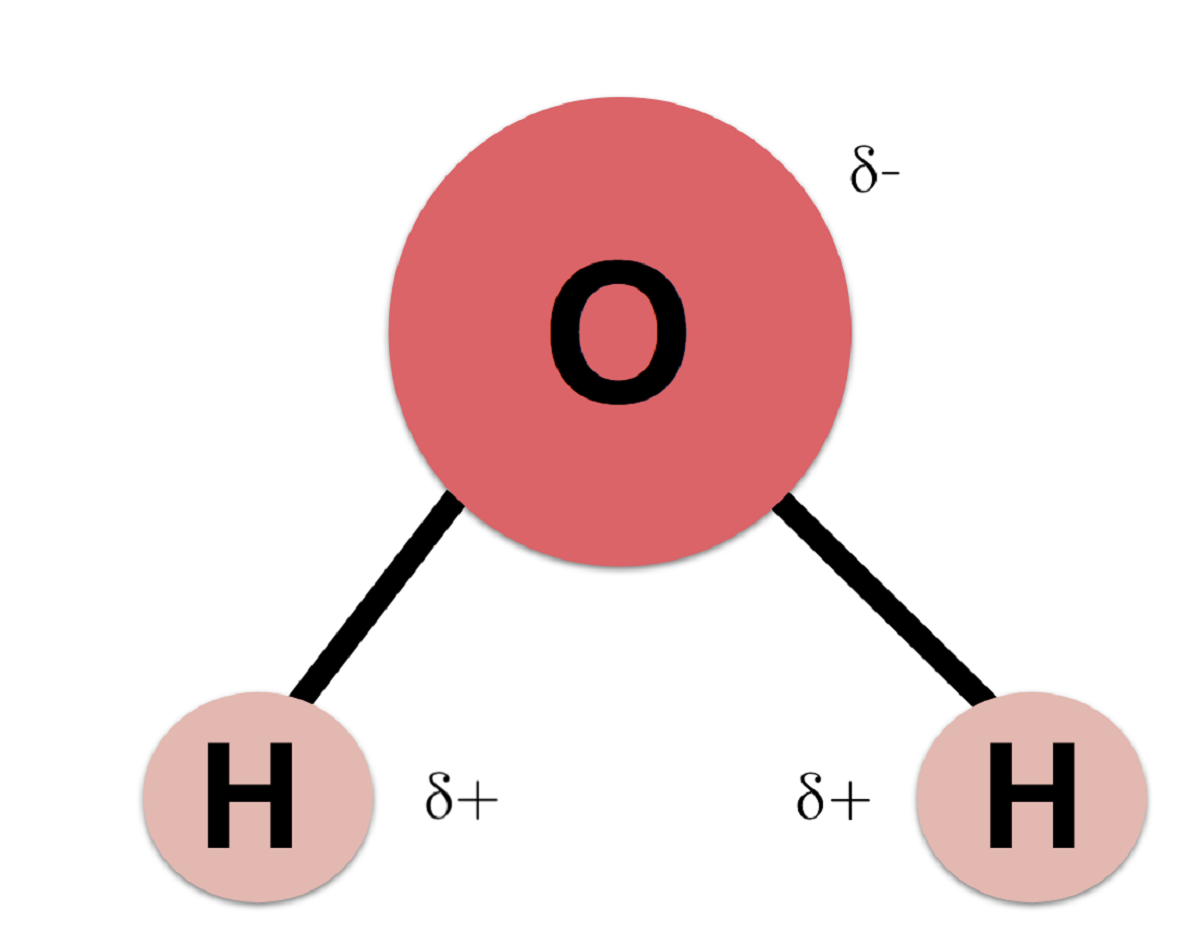
Dahil ang oxygen ay may higit na electronegativity kaysa sa hydrogen, ang mga electron ay mas malamang na mas malapit sa oxygen atom kaysa sa hydrogen. Ito ay sapagkat ang mga electron ay negatibong sisingilin. Ang katotohanan na ang mga electron ay pumupunta sa karamihan sa mga atomo ng oxygen na gumagawa ng hydrogen atom na may tiyak na positibong singil. Ang singil na ito ay tinawag na positibong bahagyang pagsingil. Ang oxygen na iyon ay tinatawag na negatibong bahagyang pagsingil.
Ang pagkakaiba sa pagitan ng positibo at negatibong mga electron na malapit sa parehong mga atomo ay gumagawa ng Molekyul ng tubig na isang polar Molekyul. Iyon ay, ang Molekyul ay may bahagi na may isang negatibong poste at isa pang bahagi na may isang positibong poste. Bagaman ang buong Molekyul ay walang kinikilingan, mula sa polar character na ito na nakukuha ang lahat ng mga physicochemical at biological na katangian.
Pakikipag-ugnayan sa pagitan ng mga molekula
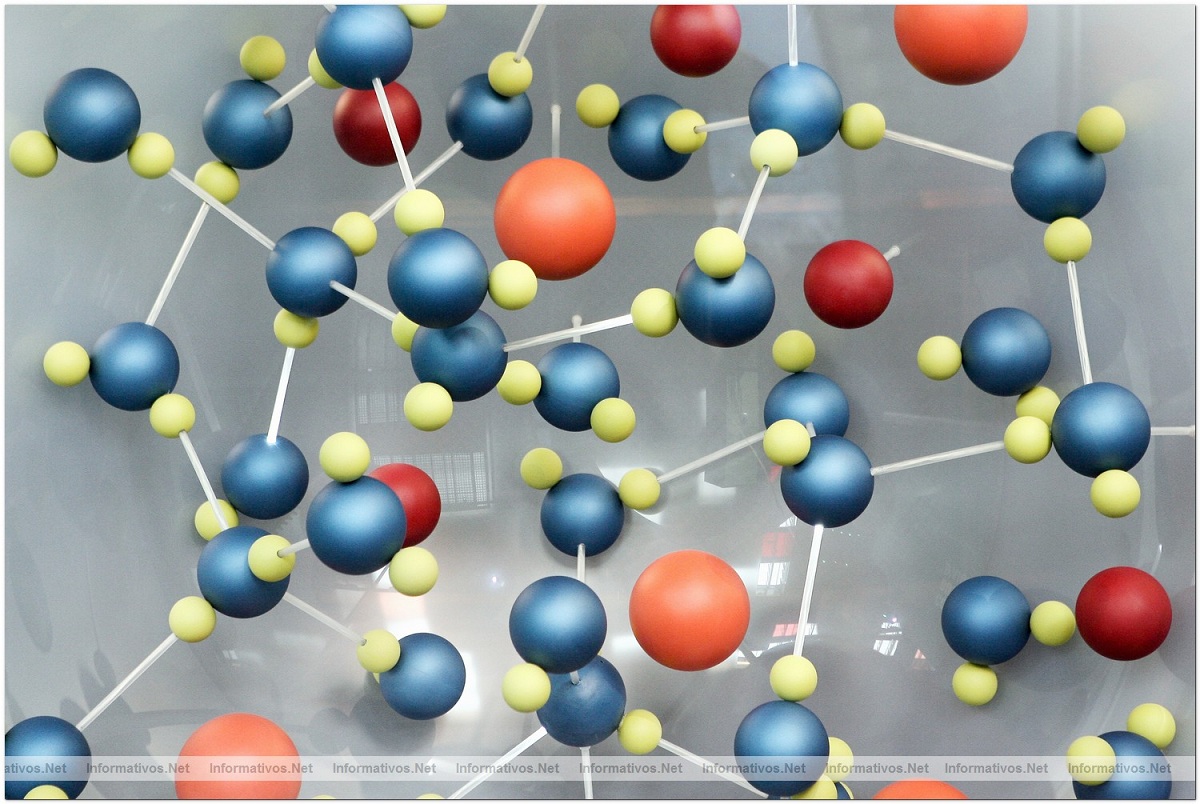
Kapag maraming mga molekula ng tubig ang napakalapit sa bawat isa ay nakapagtatag sila ng isang lakas sa pagitan ng mga atomo ng oxygen ng mga molekula nang magkahiwalay. Ito ay dahil ang oxygen ay may negatibong bahagyang singil at ang isa sa mga hydrogens ay may positibong bahagyang singil. Samakatuwid, ang positibong bahagi ng isang molekula ng tubig ay naaakit sa negatibong bahagi ng iba pang Molekyul ng tubig. Ang ganitong uri ng pakikipag-ugnayan sa pagitan ng mga molekula ay tinatawag bilang isang mapagkukunan ng hydrogen. Marami itong nangyayari sa mga molekulang ito dahil iniutos sila sa paraang ganoon ang bawat Molekyul ng tubig ay may kakayahang maiugnay sa 4 pang mga molekula. Ang ganitong uri ng pakikipag-ugnayan ay nangyayari sa yelo.
Ang mga bono sa pagitan ng mga hydrogens ay nagaganap salamat sa ang katunayan na mayroong isang atom na may negatibong bahagyang singil at isang hydrogen na may positibong bahagyang singil. Ginagawa nitong hindi kakaiba ang tubig sa mga link. Ang mga pakikipag-ugnayan na bono ay nagaganap din sa nitrogen, fluorine, at hydrogen sa iba pang mga molekula na naglalaman ng mga protina at DNA.
Tingnan natin kung ano ang mga katangian ng physicochemical ng Molekyul ng tubig. Kabilang sa mga pag-aari at katangiang ito maaari nating mai-highlight ang kakayahan at pantunaw. Hindi natin dapat kalimutan na ang tubig ay itinuturing na unibersal na pantunaw. Ang isa pang katangian ng Molekyul ng tubig ay ang mataas na tiyak na init at ang init ng vaporization. Mayroon din itong mahusay na pagkakaisa at pagdirikit, isang abnormal na density, at gumagana bilang isang kemikal na reagent.
Kung gagamitin namin ang mga katangian ng tubig nakikita namin na may kakayahang ipakalat ang isang malaking bilang ng mga compound sa loob nito salamat sa polar character nito. Tulad ng nabanggit na namin dati, kahit na ang buong Molekyul ay walang kinikilingan, ang katotohanan na ito ay may positibong bahagi at isang negatibong bahagi Nagbibigay ito ng mga katangiang physicochemical kung saan kinakailangan ang tubig sa buhay. Sa gayon, gumagana ito sa mga asing-gamot at iba pang mga sangkap na ionic kung saan binibigkas ng Molekyul ng tubig ang mga poste nito. Ang oryentasyong ito ng mga poste ay ibinibigay bilang isang pag-andar ng mga singil ng dalawang ions, inilalagay ang negatibong poste sa isang gilid at ang positibong poste sa kabilang panig. Halimbawa, sa mga polar na sangkap tulad ng ethanol, kumikilos ang tubig sa katulad na paraan. Kinokontra nito ang isang poste laban sa isa pa na may kabaligtaran na palatandaan ng sangkap.
Mga pag-aari ng Molekyul ng tubig
Ang Molekyul ng tubig ay may mataas na tiyak na init. Ang tukoy na init na ito ay hindi hihigit sa dami ng init na kailangang ibigay isang gramo ng tubig upang maiangat ang temperatura nito ng isang degree. Sa kabilang banda, mayroon kaming init ng vaporization. Ito ang halaga ng singaw na dapat ilapat sa isang gramo ng likido upang maaari itong pumasa sa isang gramo ng singaw. Alam namin na ang Molekyul ng tubig ay may mataas na tiyak na init at pag-singaw salamat sa mga tulay na sumali sa mga hydrogen atoms. Iyon ay, upang itaas ang temperatura ng tubig sa isang degree, ang lahat ng mga molekula ay kailangang dagdagan ang kanilang panginginig. Upang magawa ito, sinisira nila ang mga bono ng hydrogen upang mapasa nila ang isang gramo ng likidong tubig sa isang gramo ng singaw na tubig.
Ang katotohanan na ito ay may isang mataas na halaga ng init ng vaporization ay dahil sa ito ay maaaring pumasa. Ang isa pang katangian ng molekula ng tubig ay ang pagkakaisa. Ang tanong ay ang ugali na kailangang magkaisa ang dalawang mga molekula. Salamat muli sa mga bond ng hydrogen ng Molekyul ng tubig, mataas ang koheyon. Ang accession ay ang ugali ng dalawang magkakaibang mga molekula na magkabuklod sa bawat isa. Ginagawa nitong ang Molekyul ng tubig ay may mataas na pagdirikit sa mga compound na ionic at polar. Ito ang application na nagaganap kapag nangyari na dumidikit ang tubig sa iba't ibang mga ibabaw.
Inaasahan ko na sa impormasyong ito maaari kang matuto nang higit pa tungkol sa Molekyul ng tubig.