Na področju kemije imamo kemijske reakcije, ki se pojavljajo med molekulami in atomi. Danes se bomo pogovorili o hidroliza. Hidroliza je vrsta kemične reakcije, ki se lahko pojavi med anorganskimi in organskimi molekulami ali ioni. Glavna značilnost hidrolize je, da vključuje sodelovanje vode, da se vezi lahko pretrgajo.
V tem članku vam bomo predstavili vse značilnosti in pomen hidrolize na področju kemije.
Kaj je hidroliza
Govorimo o vrsti kemijske reakcije, ki se lahko pojavi med organskimi in anorganskimi molekulami. Bistveni pogoj je, da mora biti voda vključena, da lahko pretrgajo vezi teh molekul. Beseda hidroliza izhaja iz grškega hydro, kar pomeni vodo, in iz lize, kar pomeni ruptura. Prevedeno v obliki bi hidrolizo lahko poznali kot razgradnjo vode. V tem primeru govorimo o pretrganju vezi nekaterih reaktantov s sodelovanjem vode.
Molekula vode je sestavljena iz dveh atomov vodika in enega atoma kisika. Zahvaljujoč tej kombinaciji atomov nastane ravnovesje med ioni soli šibkih kislin in baz. Kisline in baze so koncepti, ki se pojavljajo v splošnih študijah kemije in analitične kemije. Za hidrolizo lahko rečemo, da je ena najpreprostejših kemičnih reakcij tam zunaj. Splošna enačba za hidrolizo je naslednja:
AB + H2O = AH + B-OH
Obstaja več primerov hidrolize, ko voda ali sama po sebi ne more pretrgati določene kovalentne vezi. Spomnimo se, da je kovalentna vez tista, v kateri več molekul z nekovinskimi značilnostmi se združi in tvori novo molekulo. Vez, ki se jim pridruži, je znana kot kovalentna vez. Kadar voda sama ne more pretrgati te vezi, postopek pospešimo ali kataliziramo z nakisanjem ali alkalizacijo medija. To pomeni, da lahko v prisotnosti ionov kataliziramo hidrolizo. In obstajajo encimi, ki lahko katalizirajo kemično reakcijo hidrolize.
Glavne značilnosti

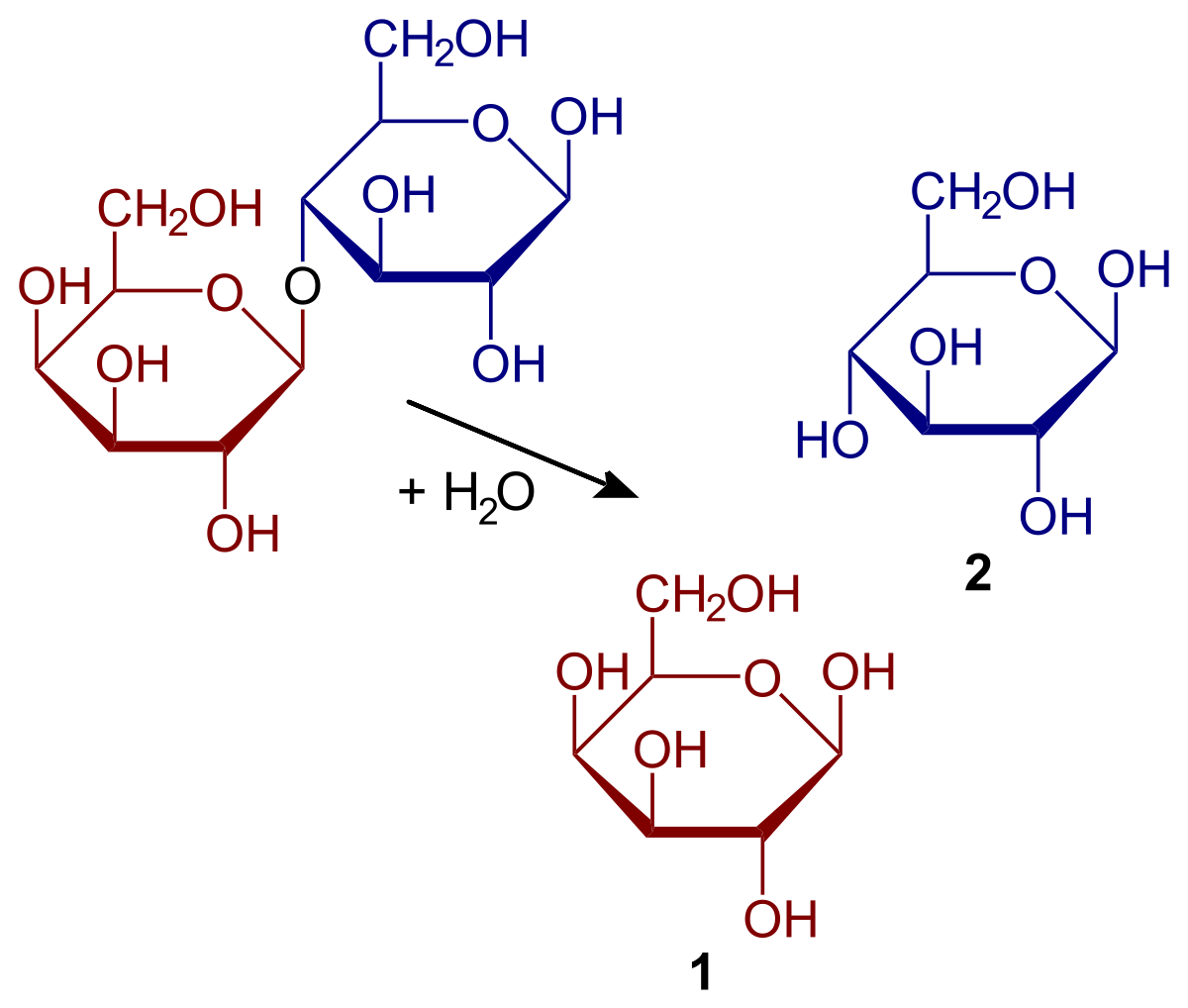
Poglejmo, kakšne so značilnosti in iz česa je sestavljena hidroliza. Ta vrsta reakcije zavzema posebno mesto, ko gre za biomolekule. In to je, da so vezi, ki držijo monomere molekul skupaj, pod določenimi pogoji dovzetne za hidrolizo. Se pravi, kovalentne vezi, s katerimi so molekule pritrjene, se lahko v prisotnosti vode pretrgajo. Primer tega so sladkorji. Sladkorji so sposobni hidrolize, da razgradijo polisaharide v monosaharide. To se zgodi zaradi delovanja encimov, znanih kot glukozidaze.
Upoštevati je treba, da vez ni le tista, ki prekine molekulo. Tudi sama voda se zlomi in sčasoma loči ione. Voda se zlomi v H + in OH–, kjer se H + konča z A, OH - z B. AB tako reagira z molekulo vode, pri čemer nastaneta dva produkta, AH in B-OH.
Zato lahko rečemo, da je hidroliza kemična reakcija v nasprotju s kondenzacijo. Od kondenzacije, dva izdelka se združita tako, da sprostita majhno molekulo. Ta majhna molekula je voda. Nasprotno, pri hidrolizi se molekula porabi, pri kondenzaciji pa se ta molekula za elektrolizo porabi, sprosti ali proizvede.
Za lažje razumevanje bomo znova razložili primer sladkorjev. Predpostavimo, da je AB saharozni dimer. V tem primeru A predstavlja glukozo, B pa fruktozo. Ta vez, ki je znana pod glikozidnim imenom, se lahko hidrolizira, da nastaneta dva ločena monosaharida in raztopina. Enako se zgodi z oligosaharidi in polisaharidi, če encimi delujejo v reakcijah.
Vemo, da ima ta kemijska reakcija le eno smer. To pomeni, da gre za vrsto ireverzibilne hidrolize. Po drugi strani pa obstajajo reakcije hidrolize, ki so reverzibilne, ko se doseže ravnotežje.
Primeri reakcij hidrolize
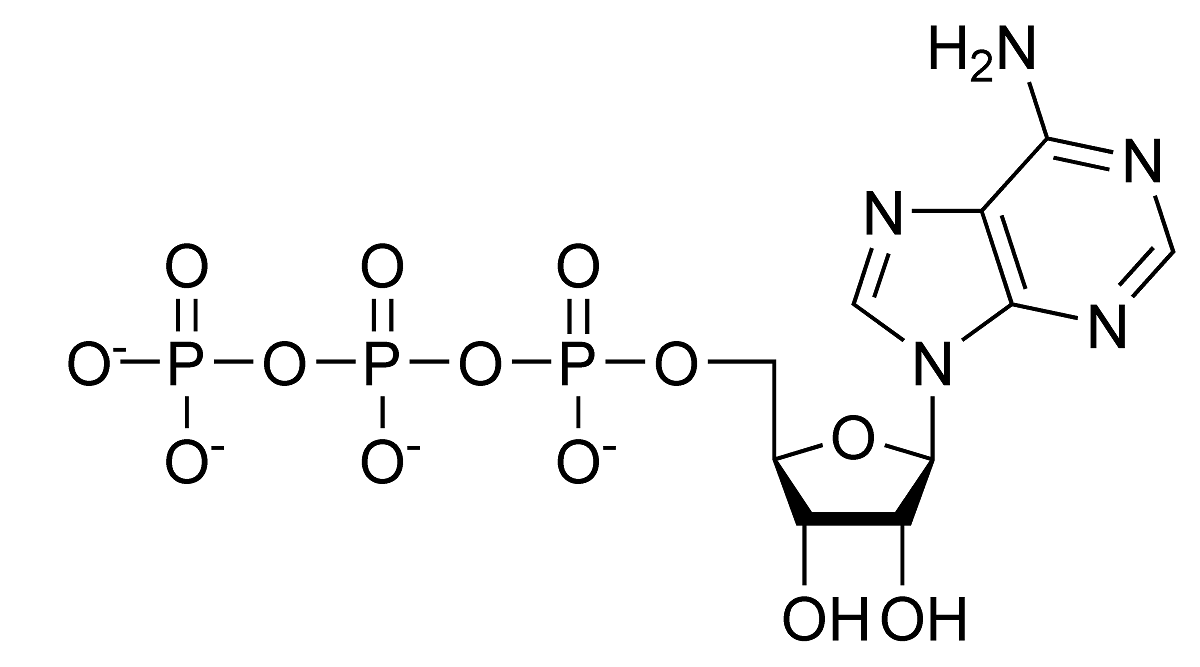
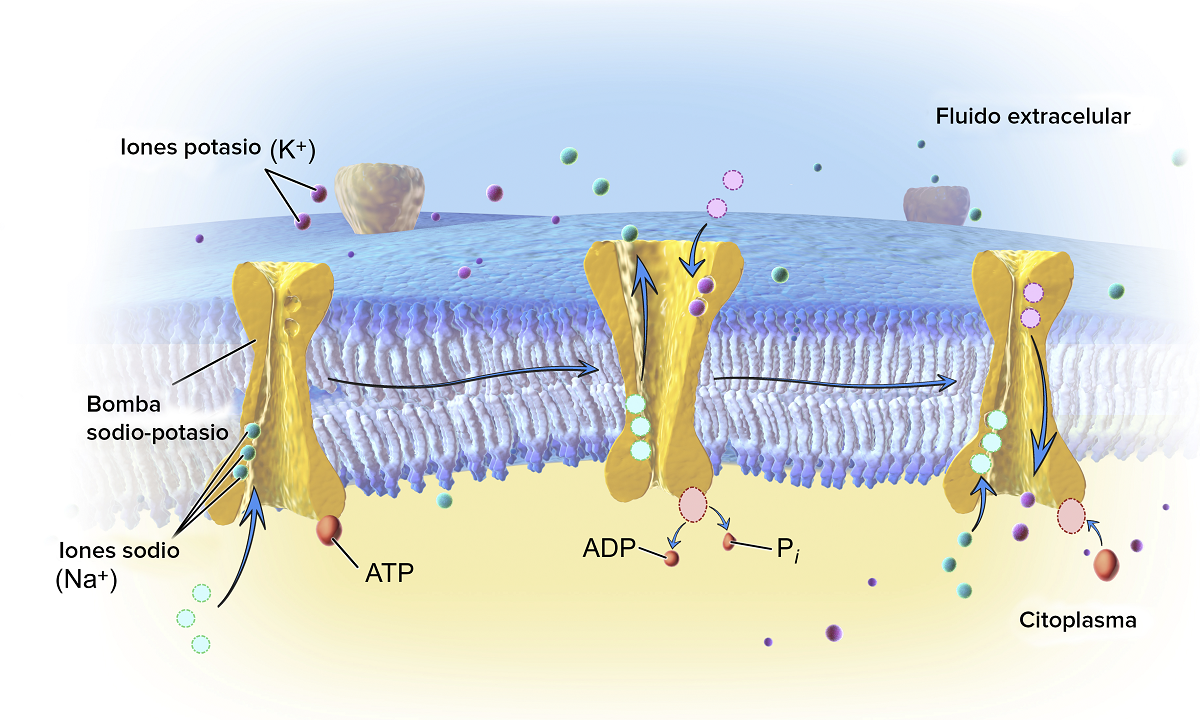
Poglejmo, kateri so glavni primeri hidrolize, ki se pojavljajo naravno. Najprej je videti reakcijo hidrolize ATP. Vemo, da ima ta molekula stabilne pH vrednosti med 6.8 in 7.4. Če pa se vrednosti pH povečajo in postanejo bolj alkalne, lahko spontano hidrolizira. Pri živih bitjih hidrolizo katalizirajo encimi, znani pod imenom ATPaze. Je vrsta eksergonične kemične reakcije. To pomeni, da je entropija ADP večja kot entropija ATP, zato do spremembe proste energije pride s hidrolizo ATP. Ta vrsta hidrolize ima številne endergonske reakcije.
Povezane reakcije so druga vrsta reakcije, pri kateri pride do hidrolize. V nekaterih primerih se uporablja za pretvorbo spojine A v spojino B. Najbolj znan primer hidrolize se naravno pojavi v vodi. Kot da bi lahko eno od molekul vode razbili na ione in se vodikov protonski vez poveže z atomom kisika druge molekule vode. Tako nastane hidronijev ion. Lahko bi ga poimenovali več kot hidroliza kot avtoionizacija ali avtoprotoliza vode.
Na koncu še en del, kjer te reakcije se na splošno generirajo v beljakovinah. Vemo, da so beljakovine stabilne molekule in da bi dosegli njihovo popolno hidrolizo, so potrebni ekstremni pogoji. Spomnimo se, da so beljakovine sestavljene iz aminokislin. Vendar so živa bitja obdarjena z arzenalom encimov, ki omogočajo hidrolizo beljakovin v aminokisline v dvanajstniku.
Upam, da boste s temi informacijami izvedeli več o hidrolizi in njenih značilnostih.