
В области химии энергия ионизации. Он относится к минимальному количеству энергии, которое требуется для отрыва электрона, введенного в атом в газовой фазе. Эта энергия обычно выражается в килоджоулей на моль. Это очень важно во многих областях химии, поэтому это интересно знать.
Поэтому мы собираемся посвятить эту статью, чтобы рассказать вам обо всех характеристиках и важности энергии ионизации.
Características principales
Когда мы говорим энергия, необходимая для вытеснения электрона из атома газовой фазы Мы подчеркиваем, что это газообразное состояние - это состояние, свободное от влияния, которое атомы могут оказывать на себя. Напомним, что в материале, находящемся в газообразном состоянии, любой тип межмолекулярного взаимодействия исключен, поскольку атомы разлетаются друг от друга. Величина энергии ионизации - это параметр, который служит для описания силы, с которой электрон связывается с атомом, частью которого он является.
Будут соединения, в которых электрон более высокая энергия ионизации, и это будет означать, что он имеет более высокую прочность связи с атомом. То есть, чем больше энергия ионизации, тем сложнее будет отрыв рассматриваемого электрона.
Энергетический потенциал ионизации
Когда мы начинаем изучать энергию ионизации вещества, мы должны знать его потенциал ионизации. Это не более минимального количества энергии, которое необходимо приложить, чтобы вызвать отрыв электрона от внешней оболочки атома, находящейся в его основном состоянии. Более того, нагрузка должна быть нейтральной. Следует отметить, что когда говорят о потенциале ионизации, используется термин, что каждый используется меньше. Это связано с тем, что определение этого свойства было основано на применении электростатического потенциала к исследуемому образцу.
При использовании этого электростатического потенциала произошло несколько вещей: с одной стороны, ионизация химических веществ произошла из-за электростатического воздействия. С другой стороны, произошло ускорение процесса отрыва удаляемого электрона. Когда для определения энергии ионизации стали использоваться спектроскопические методы, название потенциала стало меняться на название энергии. Точно так же известно, что химические свойства атомов определяются конфигурацией электронов, присутствующих на внешнем энергетическом уровне. На этих уровнях электроны дальше от ядра и могут дать больше информации.
Все это означает, что энергия ионизации этих частиц, которые имеют электроны, присутствующие на крайнем энергетическом уровне, напрямую связана со стабильностью валентных электронов.
Методы определения энергии ионизации
Существует множество методов определения этого вида энергии. Методы в основном даны процессами фотоэмиссии. Большинство этих процессов основано на определении энергии, испускаемой электронами в результате применения фотоэлектрического эффекта. Одним из самых быстрых методов количественной оценки энергии ионизации является атомная спектроскопия. Есть еще один интересный метод расчета этого типа энергии - фотоэлектронная спектроскопия. В этом типе метода измеряются энергии, с которыми электроны связаны с атомами.
В связи с этим, Используется метод, известный как ультрафиолетовая фотоэлектронная спектроскопия, который имеет аббревиатуру на английском языке UPS. Этот метод состоит из техники, использующей возбуждение атомов или молекул с помощью ультрафиолетового излучения. Таким образом, можно лучше измерить энергию, с которой электроны оптимального внешнего энергетического уровня связаны с ядром атома. Все это делается для того, чтобы проанализировать энергетические переходы внешних электронов исследуемых химических частиц. Он также используется для изучения характеристик связей, которые образуются между ними.
Другой способ узнать энергию ионизации - использовать спектральный метод рентгеновских фотоэлектронных копий. Он использует тот же принцип возбуждения электронов самого внешнего слоя и изучает различия в типах излучения, которое используется для воздействия на шоу. , скорость, с которой электроны удаляются, и полученное разрешение.
Первая и вторая энергия ионизации
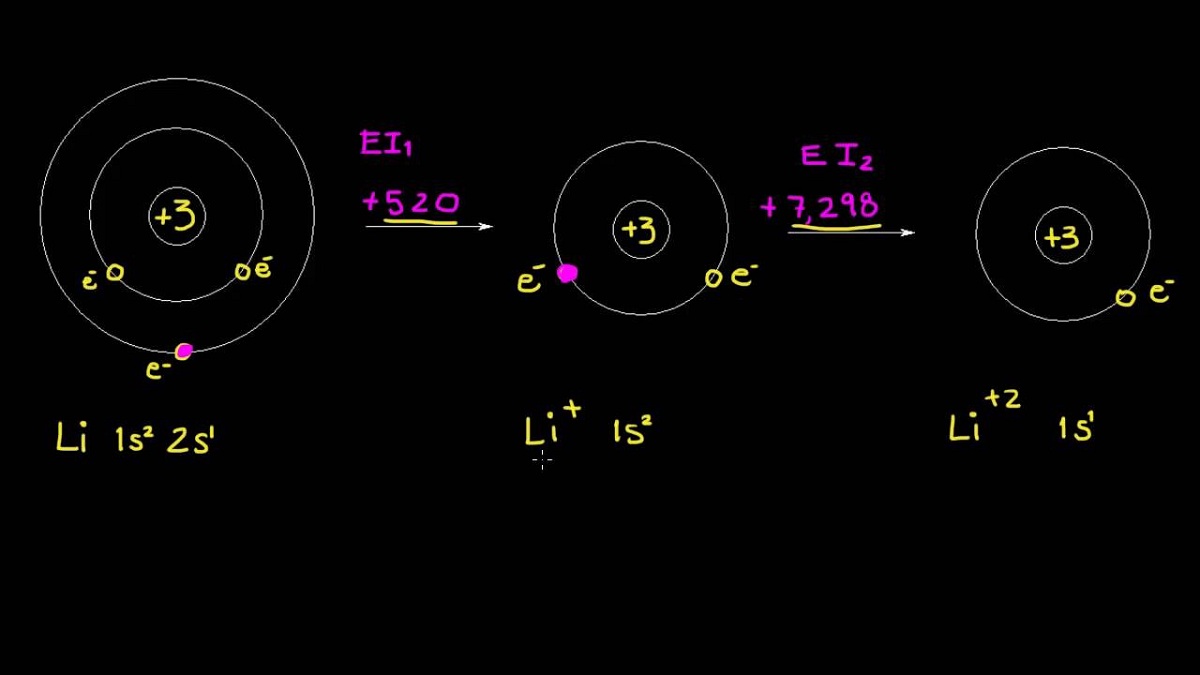
В случае атомов, которые имеют более одного электрона на внешнем уровне, мы обнаруживаем, что величина энергии, необходимая для удаления первого электрона из атома, осуществляется посредством эндотермической химической реакции. Атомы, которые имеют более одного электрона, называются полиэлектронными атомами.. Химическая реакция является эндотермической, поскольку прекращает подачу энергии к атому, чтобы получить электрон, добавленный к катиону этого элемента. Это значение известно как первая энергия ионизации. Все элементы, присутствующие в один и тот же период, увеличиваются пропорционально увеличению их атомного номера.
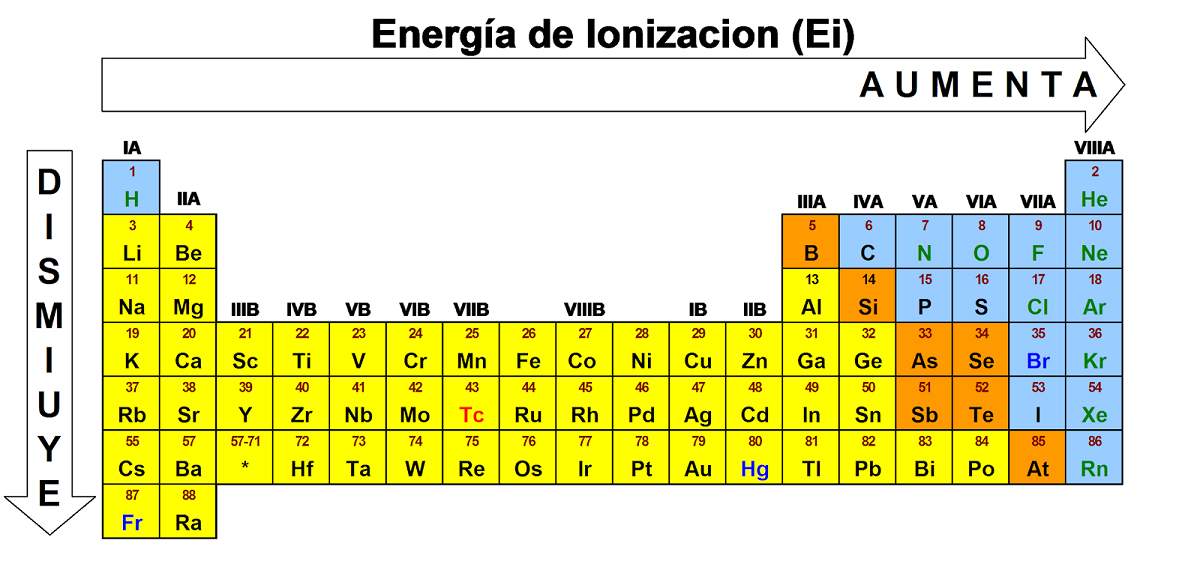
Это означает, что они уменьшаются справа налево в периоде и сверху вниз в пределах той же группы, которая существует в периодической таблице. Если мы будем следовать этому определению, благородные газы обладают большими значениями энергии ионизации. С другой стороны, элементы, которые Они относятся к группе щелочных и щелочноземельных металлов и имеют меньшее значение этой энергии.
Таким же образом, как мы описали первую энергию, удаляя второй электрон из того же атома, получается вторая энергия ионизации. Для расчета этой энергии сохраняется та же схема, и следующие электроны удаляются. Из этой информации получается, что отрыв электрона от атома в его основном состоянии уменьшает этот эффект отталкивания, который, как мы видим, существует среди остальных электронов. Это свойство известно как ядерный заряд и остается постоянным. Большее количество энергии требуется, чтобы оторвать другой электрон ионной разновидности, который имеет положительный заряд.
Я надеюсь, что с этой информацией вы сможете больше узнать об энергии ионизации.