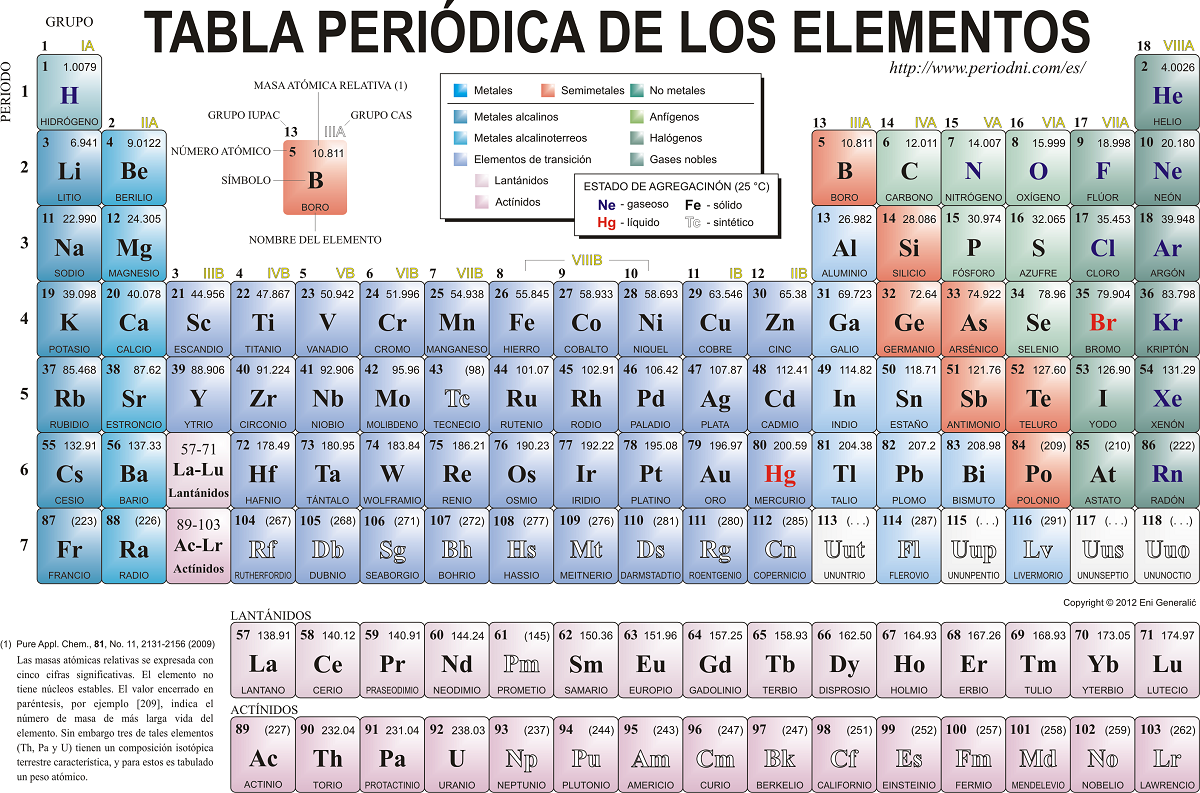
Het periodiek systeem is een grafisch en conceptueel hulpmiddel dat alle chemische elementen die de mens kent organiseert op basis van hun atoomnummer (dat wil zeggen het aantal protonen in de kern) en andere fundamentele chemische eigenschappen. Veel mensen kennen de oorsprong van het periodiek systeem.
Daarom gaan we je vertellen over de oorsprong van het periodiek systeem, de geschiedenis ervan en het belang dat het heeft voor de chemie.
Oorsprong van het periodiek systeem

De eerste versie van dit conceptuele model werd in 1869 in Duitsland gepubliceerd door de in Rusland geboren scheikundige Dimitri Mendelejev (1834-1907), die een herkenbaar schema ontdekte om ze grafisch te categoriseren en te ordenen. De naam komt van de hypothese van Mendelejev dat het atoomgewicht de periodieke eigenschappen van de elementen bepaalt.
Het eerste periodiek systeem der elementen rangschikte de 63 elementen die destijds werden ontdekt in zes kolommen, wat algemeen wordt aanvaard en gerespecteerd door geleerden van deze discipline. Het wordt beschouwd als de eerste poging om de door Antoine Lavoisier of André-Emile Bégueille de Champs Courtois voorgestelde elementen te systematiseren.
Naast het maken van het periodiek systeem, heeft Mendelejev gebruikte het als een hulpmiddel om het onvermijdelijke bestaan van nog te ontdekken elementen af te leiden, een voorspelling die later uitkwam toen veel van de elementen die de gaten in zijn tabel vulden, ontdekt werden.
Sindsdien is het periodiek systeem echter verschillende keren opnieuw uitgevonden en aangepast, waarbij de atomen die later zijn ontdekt of gesynthetiseerd, zijn uitgebreid. Mendeleev creëerde zelf een tweede versie in 1871. De huidige structuur is bedacht door de Zwitserse chemicus Alfred Werner (1866-1919) van de originele tafel, en het ontwerp van de standaardfiguur wordt toegeschreven aan de Amerikaanse chemicus Horace Groves Deming.
Een nieuwe versie van de tabel, voorgesteld door de Costa Ricaan Gil Chaverri (1921-2005), houdt rekening met de elektronische structuren van elementen in plaats van hun protonaantallen. De huidige acceptatie van de traditionele versie is echter absoluut.
Geschiedenis van het periodiek systeem

In de XNUMXe eeuw begonnen scheikundigen de bekende elementen te classificeren op basis van hun gelijkenis in fysische en chemische eigenschappen. Het einde van deze studies resulteerde in het moderne periodiek systeem der elementen zoals wij dat kennen.
Tussen 1817 en 1829 de Duitse chemicus Johan Dobereiner groepeerde enkele elementen in groepen van drie, tripletten genoemd, omdat ze vergelijkbare chemische eigenschappen deelden. In het chloor (Cl), broom (Br) en jodium (I) triplet, heb je bijvoorbeeld gemerkt dat de atoommassa van Br heel dicht bij de gemiddelde massa van Cl en I lag. Helaas zijn niet alle elementen ingedeeld in drieling en zijn pogingen kwamen niet tot een classificatie van elementen.
In 1863, de Britse chemicus John Newlands verdeelde de elementen in groepen en stelde de wet van octaven voor, bestaande uit elementen met toenemende atomaire massa waarin bepaalde eigenschappen elke 8 elementen worden herhaald.
In 1869 publiceerde de Russische chemicus Dmitri Mendelejev zijn eerste periodiek systeem, waarin hij de elementen opsomde in volgorde van toenemende atoommassa. Tegelijkertijd publiceerde de Duitse scheikundige Lothar Meyer zijn eigen periodiek systeem, waarin de elementen gerangschikt waren van de kleinste tot de grootste atoommassa. Mendeleev rangschikte hun tafels in horizontale opstellingen en liet lege plekken achter waar ze iets moesten toevoegen dat nog ontdekt moest worden. Binnen de organisatie had Mendelejev een duidelijk patroon voor ogen: elementen met vergelijkbare chemische eigenschappen verschijnen op regelmatige (of periodieke) intervallen in verticale kolommen op een tafel. Na de ontdekking van gallium (Ga), scandium (Sc) en germanium (Ge) tussen 1874 en 1885, Mendelejevs voorspellingen werden ondersteund door ze in die gaten te plaatsen, waardoor zijn periodiek systeem een wereld werd die meer waarde en acceptatie heeft gekregen.
In 1913 bepaalde de Britse chemicus Henry Moseley de nucleaire lading (atoomnummer) van de elementen door middel van röntgenonderzoek en hergroepeerde ze in volgorde van oplopend atoomnummer zoals we dat nu kennen.
Wat zijn de groepen van het periodiek systeem der elementen?
In de chemie is een periodiek systeem een kolom met samenstellende elementen, overeenkomend met een groep chemische elementen met veel atomaire kenmerken. In werkelijkheid, de belangrijkste functie van het periodiek systeem, gemaakt door de Russische chemicus Dmitri Mendelejev (1834-1907), was juist bedoeld als een diagram om de verschillende groepen van bekende chemische elementen te classificeren en te organiseren, waarvan de populatie een van de belangrijkste componenten is.
De groepen worden weergegeven in de kolommen van de tabel, terwijl de rijen de perioden vormen. Er zijn 18 verschillende groepen, genummerd van 1 tot 18, die elk een variabel aantal chemische elementen bevatten. Elke groep elementen heeft hetzelfde aantal elektronen in hun laatste atoomschil, daarom hebben ze vergelijkbare chemische eigenschappen, aangezien de chemische eigenschappen van chemische elementen nauw verwant zijn aan de elektronen in de laatste atoomschil.
De nummering van de verschillende groepen in de tabel is momenteel vastgesteld door de International Union of Pure and Applied Chemistry (IUPAC) en komt overeen met Arabische cijfers (1, 2, 3...18) ter vervanging van de traditionele Europese methode die Romeinse cijfers gebruikte en letters (IA, IIA, IIIA…VIIIA) en de Amerikaanse methode gebruiken ook Romeinse cijfers en letters, maar in een andere opstelling dan de Europese methode.
- IUPAC. 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, 13, 14, 15, 16, 17, 18.
- Europees systeem. IA, IIA, IIIA, IVA, VA, VIA, VIIA, VIIIA, VIIIA, VIIIA, IB, IIB, IIIB, IVB, VB, VIB, VIIB, VIIIB.
- Amerikaans systeem. IA, IIA, IIIB, IVB, VB, VIB, VIIB, VIIIB, VIIIB, VIIIB, IB, IIB, IIIA, IVA, VA, VIA, VIIA, VIIIA.
Op deze manier komt elk element dat in het periodiek systeem voorkomt altijd overeen met een specifieke groep en periode, wat de manier weerspiegelt waarop de menselijke wetenschap zich ontwikkelt om materie te classificeren.
Zoals je kunt zien, is het periodiek systeem door de geschiedenis heen en vandaag de dag een enorme vooruitgang geweest in de chemie. Ik hoop dat je met deze informatie meer te weten kunt komen over de oorsprong van het periodiek systeem en de kenmerken ervan.