물은 우리가 살아야하고 오늘날 우리가 알고있는 생명체가 지구에 존재하기 위해 필요한 요소입니다. 그만큼 물 분자 그것은 공유 결합으로 연결된 두 개의 수소 원자와 하나의 산소 원자로 구성됩니다. 이것은 수소의 두 원자와 산소의 두 원자가 서로 전자를 공유하기 때문에 결합된다는 것을 의미합니다. 물 분자의 공식은 H2O입니다. 물 분자에는 많은 특성이 있으며 그 덕분에 생명의 발달을 일으키는 수많은 과정이 있습니다.
따라서 우리는 물 분자에 대해 알아야 할 모든 것을 설명하기 위해이 기사를 바칠 것입니다.
물 분자 분석
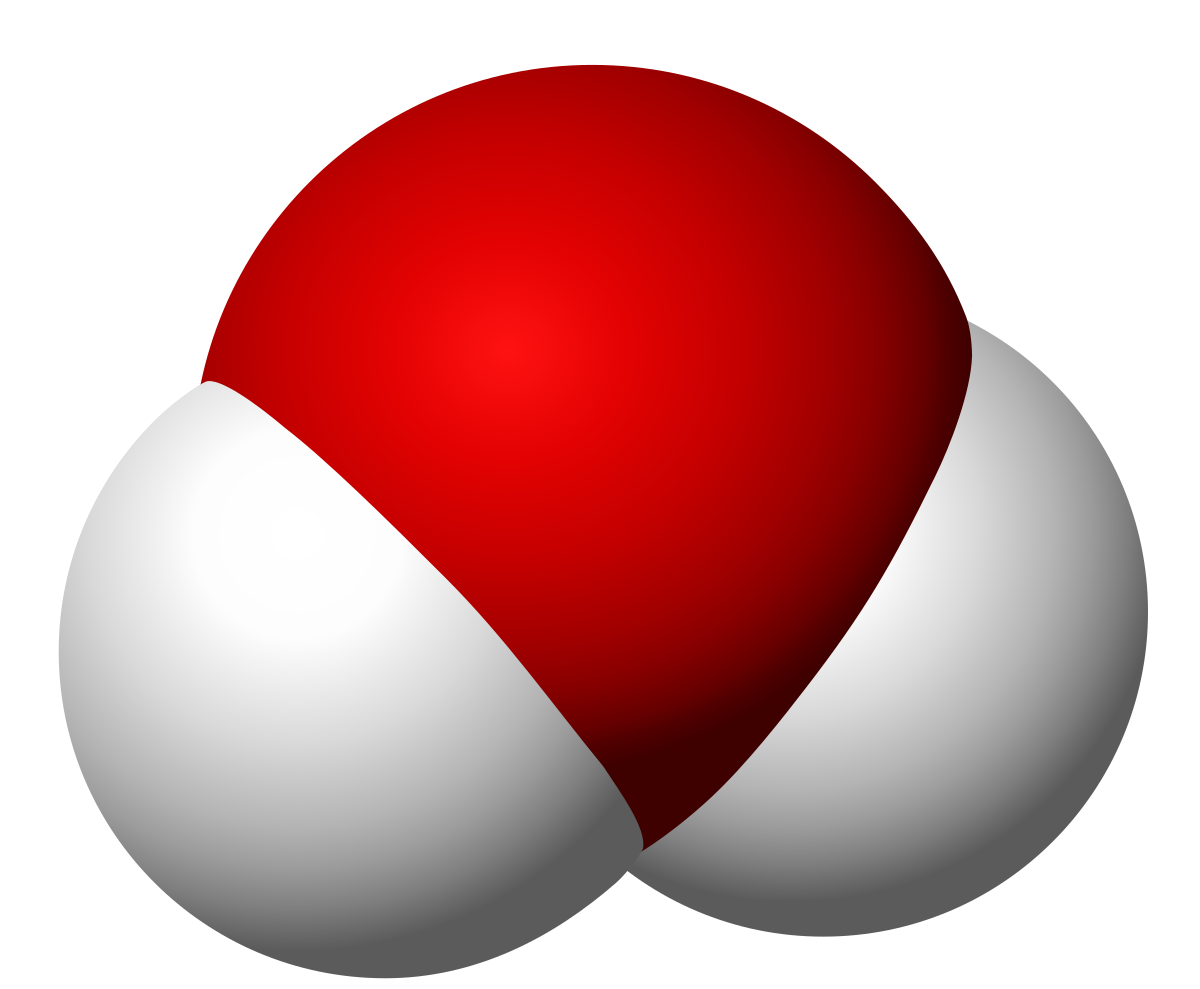
이 분자를 분석하면 수소와 산소 사이의 공유 결합의 부착 각도가 104.5도에서 시작 함을 알 수 있습니다. 이것은 분광 및 X-ray 분석을 통해 얻을 수 있으며 수소와 산소 원자 사이의 평균 거리는 다음과 같습니다. 오후 96.5 또는 같은 것, 9.65 • 10-8 밀리미터.
이 거리는 인간의 눈으로 볼 수있는 어떤 것과도 비교할 수 없습니다. 물 분자의 전자 배열은 수소와 산소 사이에 전기 음성도가 다르기 때문에 전기적 비대칭 성을 전달합니다. 우리는 전기 음성도를 공유 결합으로 공유되는 전자를 끌어 당기는 원자의 능력. 공유 결합은 두 비금속 원자 사이에 형성되는 결합이라는 것을 기억합니다.
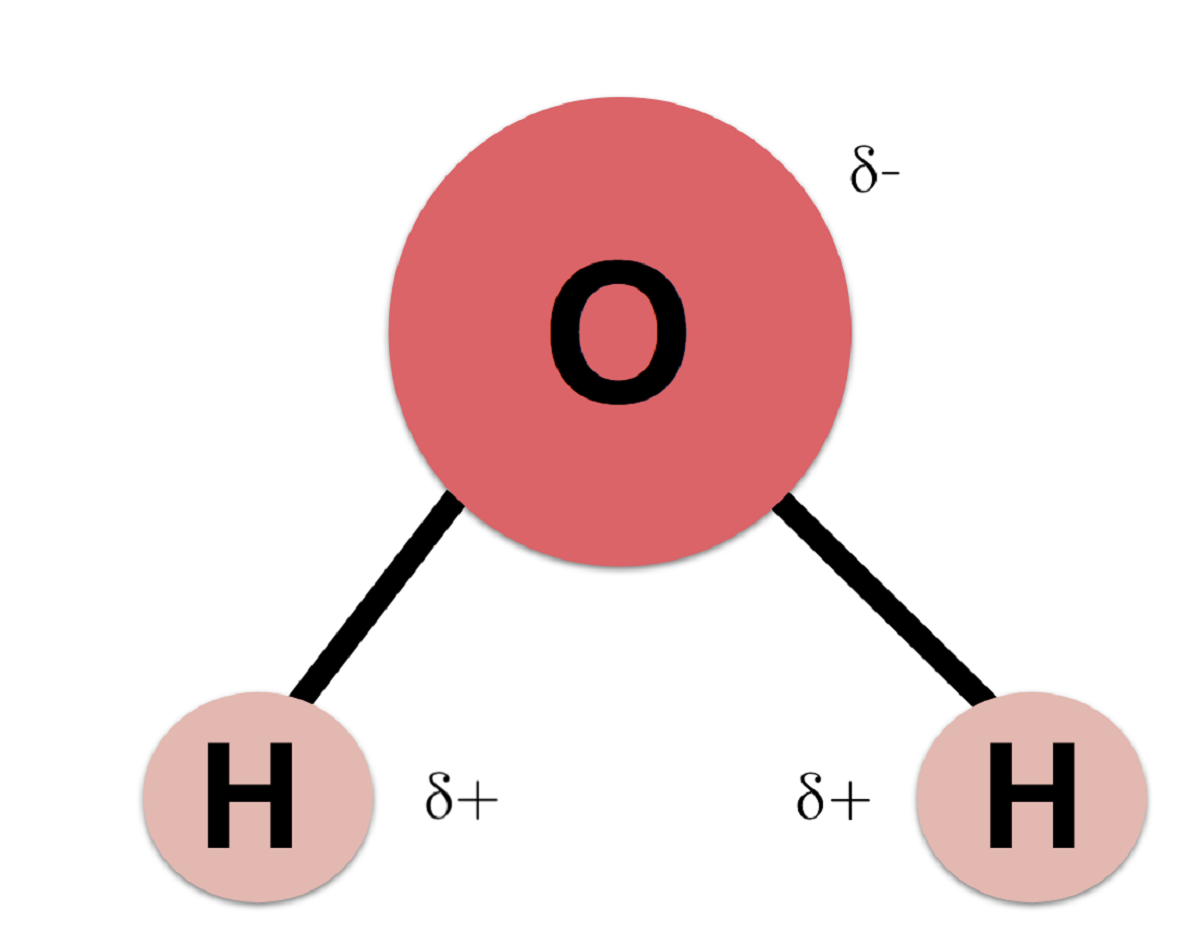
산소는 수소보다 전기 음성도가 높기 때문에 전자는 수소보다 산소 원자에 더 가깝습니다. 이것은 전자가 음전하를 띠기 때문입니다. 전자가 대부분 산소 원자로 이동한다는 사실은 수소 원자가 특정 양전하를 갖도록 만듭니다. 이 전하를 양의 부분 전하라고합니다. 산소의 것을 음의 부분 전하라고합니다.
두 원자에 가까운 양전자와 음 전자의 차이는 물 분자를 극성 분자로 만듭니다. 즉, 분자에는 음극이있는 부분과 양극이있는 다른 부분이 있습니다. 분자 전체가 중성이지만 모든 물리 화학적 및 생물학적 특성이이 극성 특성에서 파생됩니다.
분자 간의 상호 작용
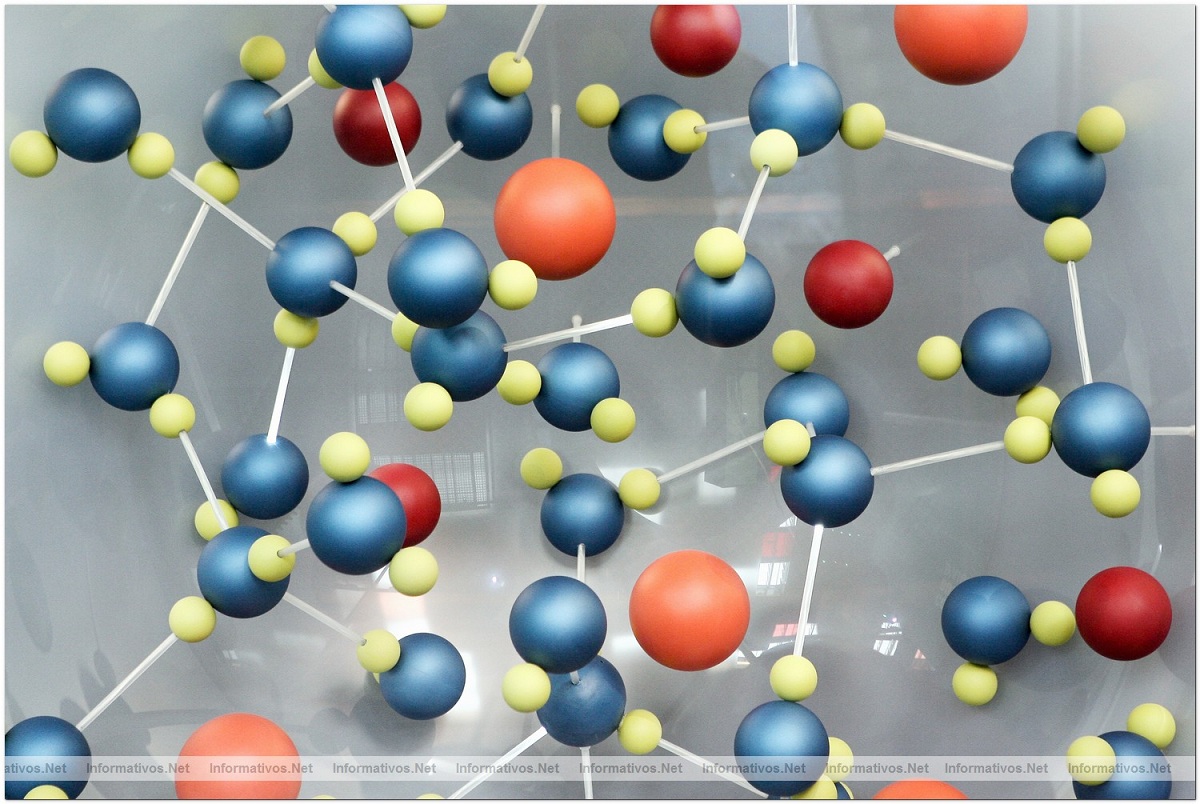
여러 물 분자가 서로 매우 가까울 때 분자의 산소 원자 사이에 개별적으로 견인력을 설정할 수 있습니다. 이것은 산소가 음의 부분 전하를 갖고 수소 중 하나가 양의 부분 전하를 갖기 때문입니다. 따라서 한 물 분자의 양의 부분은 다른 물 분자의 음의 부분에 끌립니다. 이러한 유형의 분자 간의 상호 작용을 수소 공급원이라고합니다. 이 분자들은 다음과 같은 방식으로 배열되어 있기 때문에 많은 일이 발생합니다. 각 물 분자는 4 개 이상의 분자와 결합 할 수 있습니다. 이러한 유형의 상호 작용은 얼음과 함께 발생합니다.
수소 사이의 결합은 음의 부분 전하를 가진 원자와 양의 부분 전하를 가진 수소가 있다는 사실 덕분에 발생합니다. 이것은 링크가 물에 고유하지 않게 만듭니다. 이러한 상호 작용 결합은 단백질과 DNA를 포함하는 다른 분자의 질소, 불소 및 수소에서도 발생합니다.
물 분자의 물리 화학적 특성이 무엇인지 살펴 보겠습니다. 이러한 특성과 특성 중에서 용량과 용매를 강조 할 수 있습니다. 물이 보편적 인 용매로 간주된다는 사실을 잊지 말아야합니다. 물 분자의 또 다른 특징은 높은 비열과 기화열입니다. 또한 높은 응집력과 접착력, 비정상적인 밀도를 가지며 화학 시약으로 기능합니다.
물의 특성을 사용하면 극성 특성 덕분에 그 안에 많은 수의 화합물을 분산시킬 수 있음을 알 수 있습니다. 앞서 언급했듯이 분자 전체가 중성이지만 양의 부분과 음의 부분이 있다는 사실은 그것은 물이 생명에 필요한 물리 화학적 특성을 부여합니다. 따라서 물 분자가 극을 향하는 염 및 기타 이온 물질과 함께 작동합니다. 이 극의 방향은 두 이온의 전하의 함수로 주어지며, 음극은 한쪽에, 양극은 다른쪽에 놓입니다. 예를 들어, 에탄올과 같은 극성 물질의 경우 물은 비슷한 방식으로 작용합니다. 그것은 물질의 반대 기호로 한 극을 다른 극에 반대합니다.
물 분자의 특성
물 분자는 비열이 높습니다. 이 비열은 관리해야하는 열의 양에 지나지 않습니다. 온도를 XNUMX도 올릴 수있는 물 XNUMXg. 반면에 우리는 기화열을 가지고 있습니다. 이것은 XNUMX 그램의 증기로 통과 할 수 있도록 액체 XNUMX 그램에 적용되어야하는 증기의 양입니다. 우리는 물 분자가 수소 원자를 결합하는 결합 덕분에 높은 비열과 기화를 가지고 있다는 것을 알고 있습니다. 즉, 물의 온도를 XNUMX도 올리려면 모든 분자가 진동을 증가시켜야합니다. 이를 위해 그들은 수소 결합을 끊어서 액체 물 XNUMXg을 증기 물 XNUMXg에 전달할 수 있습니다.
기화열의 가치가 높은 것은 통과 할 수 있기 때문입니다. 물 분자의 또 다른 특징은 응집력입니다. 문제는 두 분자가 결합되어야하는 경향입니다. 물 분자의 수소 결합 덕분에 응집력이 높습니다. 가입은 두 개의 다른 분자가 서로 결합하는 경향. 이것은 물 분자가 이온 성 및 극성 화합물에 대해 높은 접착력을 갖도록 만듭니다. 이것은 물이 다른 표면에 달라 붙을 때 발생하는 응용 프로그램입니다.
이 정보를 통해 물 분자에 대해 더 많이 배울 수 있기를 바랍니다.