Air adalah elemen yang kita butuhkan untuk hidup dan untuk itu ada kehidupan di bumi seperti yang kita kenal sekarang. Itu molekul air Ini terdiri dari dua atom hidrogen dan satu atom oksigen yang dihubungkan oleh ikatan kovalen. Ini berarti bahwa dua atom hidrogen dan satu oksigen bersatu karena mereka berbagi elektron di antara keduanya. Rumus molekul air adalah H2O. Ada banyak karakteristik yang dimiliki molekul air dan berkat itu ada banyak proses yang mendorong perkembangan kehidupan.
Oleh karena itu, kami akan mendedikasikan artikel ini untuk memberi tahu Anda semua yang perlu Anda ketahui tentang molekul air.
Analisis molekul air
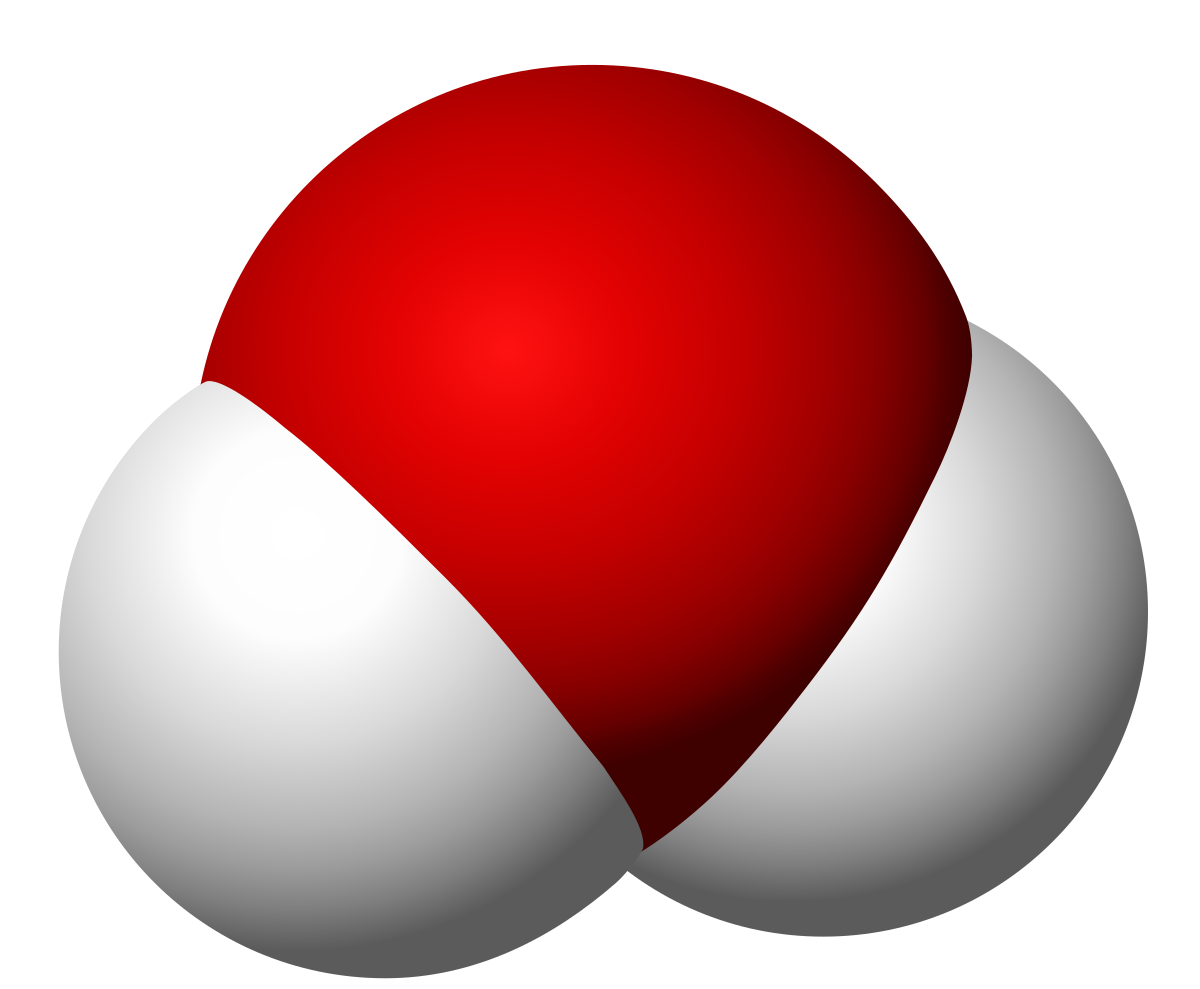
Jika kita menganalisis molekul ini, kita dapat melihat bahwa sudut perlekatan ikatan kovalen antara hidrogen dan oksigen dari 104.5 derajat. Hal ini dapat dicapai dengan analisis spektroskopi dan sinar X. Jarak rata-rata antara atom hidrogen dan oksigen adalah dari 96.5 pm atau, yang sama, 9.65 • 10-8 milimeter.
Jarak ini tidak bisa dibandingkan dengan apa pun yang bisa dilihat oleh mata manusia. Susunan elektron dalam molekul air inilah yang mengkomunikasikan asimetri listrik karena terdapat perbedaan tingkat keelektronegatifan antara hidrogen dan oksigen. Kami menyebut elektronegativitas menjadi kemampuan atom untuk menarik elektron yang terbagi dalam ikatan kovalen. Kita ingat bahwa ikatan kovalen adalah ikatan yang terbentuk antara dua atom non-logam.
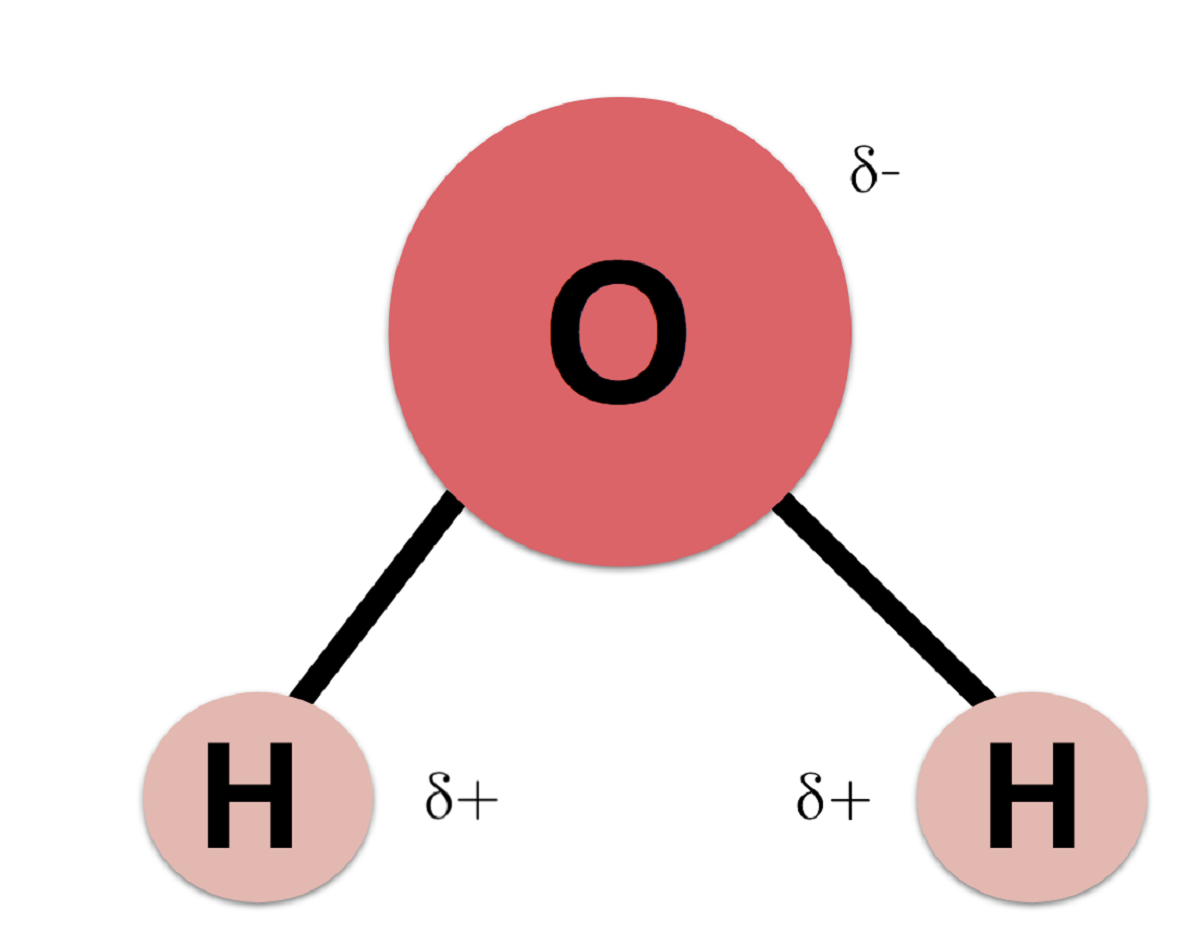
Karena oksigen memiliki lebih banyak keelektronegatifan daripada hidrogen, elektron lebih cenderung lebih dekat ke atom oksigen daripada hidrogen. Ini karena elektron bermuatan negatif. Fakta bahwa elektron sebagian besar menuju ke atom oksigen membuat atom hidrogen memiliki muatan positif tertentu. Muatan ini disebut muatan parsial positif. Oksigen disebut muatan parsial negatif.
Perbedaan antara elektron positif dan negatif yang dekat dengan kedua atom menjadikan molekul air sebagai molekul polar. Artinya, molekul memiliki bagian dengan kutub negatif dan bagian lain dengan kutub positif. Meskipun seluruh molekul netral, dari karakter kutub inilah semua sifat fisikokimia dan biologisnya diturunkan.
Interaksi antar molekul
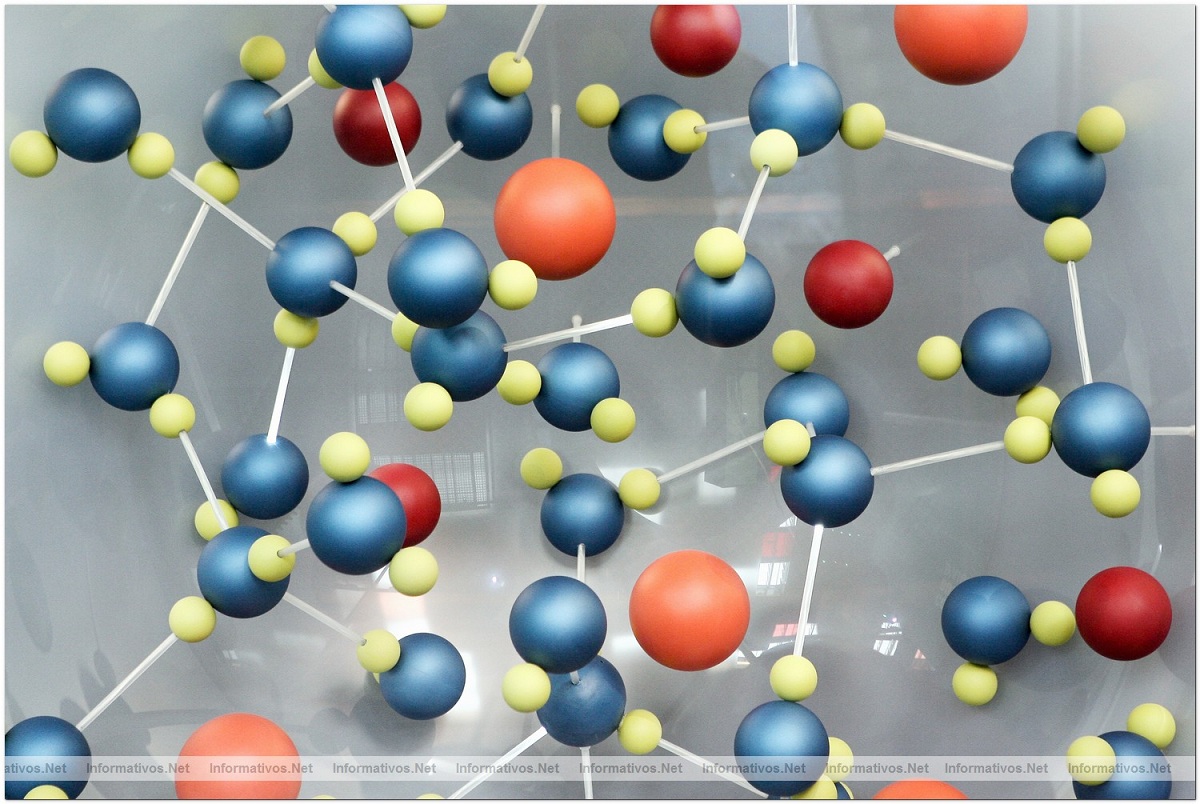
Ketika beberapa molekul air sangat dekat satu sama lain, mereka dapat membuat traksi antara atom oksigen dari molekul secara terpisah. Ini karena oksigen memiliki muatan parsial negatif dan salah satu hidrogen bermuatan parsial positif. Oleh karena itu, bagian positif dari satu molekul air tertarik ke bagian negatif dari molekul air lainnya. Jenis interaksi antar molekul ini disebut sebagai sumber hidrogen. Itu banyak terjadi pada molekul-molekul ini karena mereka diatur sedemikian rupa setiap molekul air mampu berasosiasi dengan 4 molekul lagi. Jenis interaksi ini terjadi dengan es.
Ikatan antara hidrogen terjadi berkat fakta bahwa ada atom dengan muatan parsial negatif dan hidrogen dengan muatan parsial positif. Ini membuat tautan tidak unik ke air. Ikatan interaksi ini juga terjadi pada nitrogen, fluor, dan hidrogen pada molekul lain yang mengandung protein dan DNA.
Mari kita lihat apa saja sifat fisikokimia dari molekul air. Di antara sifat dan karakteristik ini kita dapat menyoroti kapasitas dan pelarut. Kita tidak boleh lupa bahwa air dianggap sebagai pelarut universal. Karakteristik lain dari molekul air adalah kalor jenisnya yang tinggi dan kalor penguapannya. Ia juga memiliki kohesi dan adhesi yang hebat, kepadatan abnormal, dan berfungsi sebagai reagen kimia.
Jika kita menggunakan sifat-sifat air, kita melihat bahwa ia mampu mendispersi sejumlah besar senyawa di dalamnya berkat sifat kutubnya. Seperti yang telah kami sebutkan sebelumnya, meskipun seluruh molekul netral, fakta bahwa ia memiliki bagian positif dan bagian negatif adalah apa Ini memberikan sifat fisikokimia yang membuat air sangat diperlukan untuk kehidupan. Jadi, ia bekerja dengan garam dan zat ionik lainnya di mana molekul air mengarahkan kutubnya. Orientasi kutub ini diberikan sebagai fungsi dari muatan dua ion, menempatkan kutub negatif di satu sisi dan kutub positif di sisi lain. Misalnya, dengan zat polar seperti etanol, air bertindak dengan cara yang serupa. Ini menentang satu kutub terhadap kutub lain dengan tanda substansi yang berlawanan.
Sifat molekul air
Molekul air memiliki kalor jenis yang tinggi. Panas jenis ini tidak lebih dari jumlah panas yang perlu diberikan satu gram air untuk menaikkan suhunya satu derajat. Di sisi lain, kita mengalami panas penguapan. Ini adalah jumlah uap yang harus diterapkan pada satu gram cairan agar bisa berubah menjadi satu gram uap. Kita tahu bahwa molekul air memiliki kalor jenis dan penguapan yang tinggi berkat jembatan yang menghubungkan atom hidrogen. Artinya, untuk menaikkan suhu air satu derajat, semua molekul perlu meningkatkan getarannya. Untuk melakukan ini, mereka memutuskan ikatan hidrogen sehingga mereka dapat melewatkan satu gram air cair ke satu gram air uap.
Fakta bahwa ia memiliki nilai kalor penguapan yang tinggi karena ia mampu lewat. Karakteristik lain dari molekul air adalah kohesi. Pertanyaannya adalah kecenderungan bahwa dua molekul harus bersatu. Sekali lagi, berkat ikatan hidrogen dari molekul air, kohesi menjadi tinggi. Aksesi adalah kecenderungan dua molekul berbeda untuk terikat satu sama lain. Hal ini membuat molekul air memiliki daya rekat tinggi terhadap senyawa yang bersifat ionik dan polar. Ini adalah aplikasi yang terjadi ketika air menempel pada permukaan yang berbeda.
Saya berharap dengan informasi ini Anda dapat mempelajari lebih lanjut tentang molekul air.