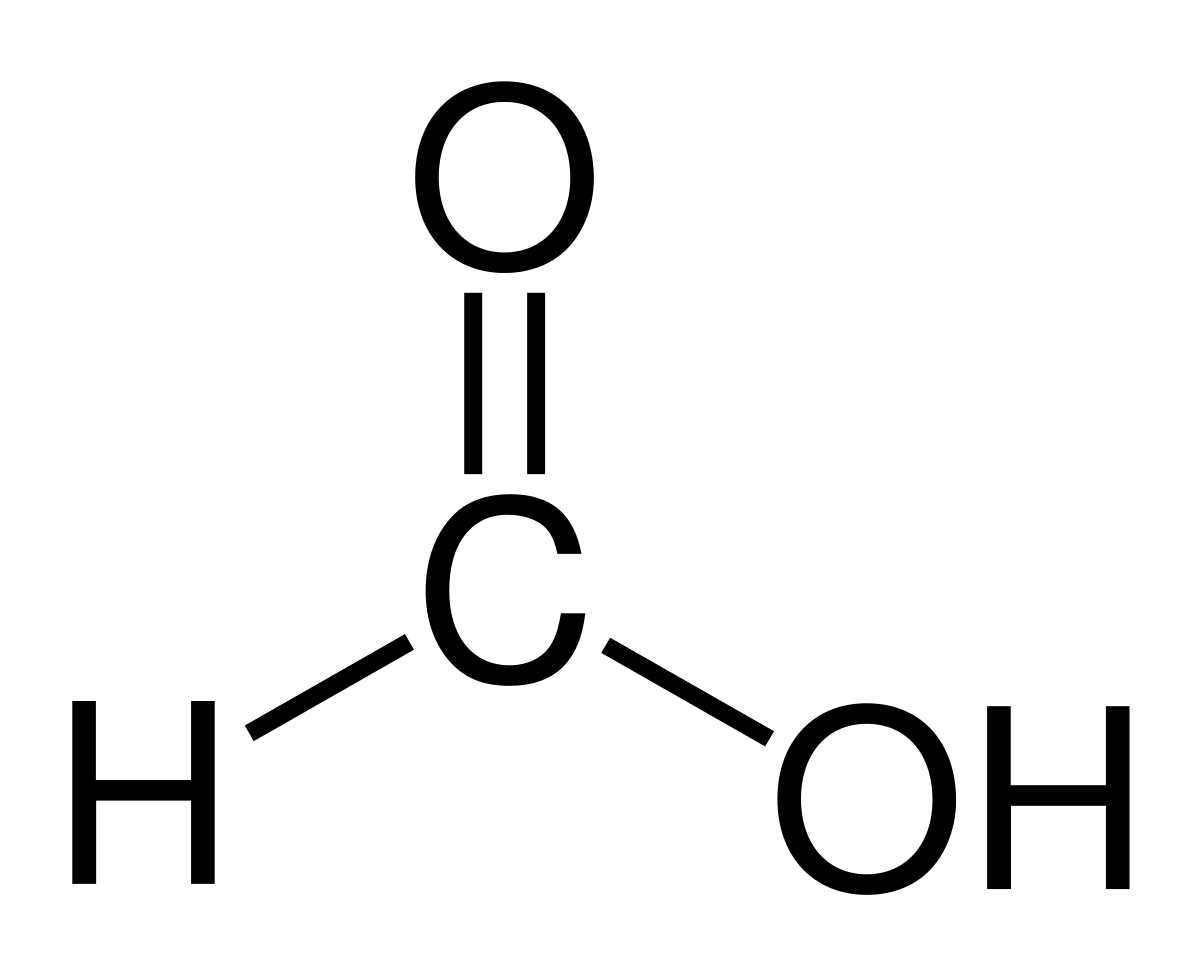
El hangyasav o A metánsav a szerves savak közül a legegyszerűbb és legkisebb vegyület. Molekulaképlete HCOOH, csak egy hidrogénatom kapcsolódik egy szénatomhoz. Neve a formica szóból származik, ami latinul hangyát jelent. Ez egy meglehetősen fontos vegyület a kémia világában, és ma széles körben használják.
Emiatt ezt a cikket annak szenteljük, hogy elmondjunk mindent, amit a hangyasavról, annak jellemzőiről és fontosságáról tudni kell.
Főbb jellemzők
A XNUMX. századi természetkutatók felfedezték, hogy bizonyos típusú rovarok (termicidek), mint pl hangyák, termeszek, méhek és bogarak, ezt a vegyületet választják ki, amitől a harapásuk fájdalmas. Ezenkívül ezek a rovarok ezt a vegyületet támadási, védekezési és kémiai jelátviteli mechanizmusként használják.
Mérgező mirigyeik vannak, amelyek ezt és más savakat, például az ecetsavat köd formájában kiszorítják a szervezetből. A hangyasav erősebb, mint az ecetsav (CH3COOH); ezért vízben feloldott azonos mennyiségű hangyasav alacsonyabb pH-jú oldatot eredményez.
John Ray angol természettudós 1671-ben sikerült izolálni ezt a vegyületet, nagyszámú hangyából nyerték ki. Másrészt ennek a vegyületnek az első sikeres szintézisét Joseph Gay-Lussac francia kémikus és fizikus végezte hidrogén-cianid (HCN) reagens felhasználásával.
hangyasav a természetben

A hangyasav létezhet szárazföldi szinten, a biomassza alkotóelemeként vagy a légkörben, kémiai reakciók széles skálájában részt vesz, sőt a föld alatt, olajban vagy a felszínén gázfázisban is megtalálható.
A biomassza tekintetében ennek a savnak a fő termelői a rovarok és a növények. Amikor a fosszilis tüzelőanyagok égnek, hangyasav gáz keletkezik; ezért az autómotorok ezt a savat a légkörbe bocsátják.
Azonban, sok hangya él a földön, és a köztük lévő hangyasav termelése ezerszer nagyobb, mint az emberi ipar által egy év alatt előállított metánsav mennyisége. Az erdőtüzek a hangyasav gáznemű forrása is.
Feljebb, a komplex légköri mátrixban zajlanak a hangyasav szintéziséhez szükséges fotokémiai folyamatok. Ezen a ponton sok illékony szerves vegyület (VOC) lebomlik az UV-sugárzás hatására, vagy az OH gyök mechanizmusa révén oxidálódik. A gazdag és összetett légköri kémia messze a metánsav fő forrása a Földön.
A hangyasav atomszerkezete
A fenti ábra a hangyasav gázfázisú dimerjének szerkezetét mutatja. A fehér gömbök a hidrogénatomoknak, a pirosak az oxigénatomoknak, a feketék a szénatomoknak felelnek meg.
Ezekben a molekulákban két csoport látható: hidroxil (-OH) és formil (-CH=O), amelyek hidrogénkötések kialakítására képesek. Ezek a kölcsönhatások OHO típusúak, ahol a hidroxilcsoport a H donor és a formilcsoport az O donor.
A szénatomokhoz kötött H azonban nem rendelkezik ezzel a képességgel. Ezek a kölcsönhatások nagyon erősek, és az OH csoportban lévő hidrogén savasabb az elektronhiányos H atom miatt; És így, ez a hidrogén tovább stabilizálja a hidat. A fentiek eredményeképpen a hangyasav dimerként létezik, és nem önálló molekulaként.
Ahogy a hőmérséklet csökken, a dimer orientálja hidrogénkötéseit, hogy a legstabilabb szerkezetet hozza létre más dimerekkel együtt, ami végtelen számú metánsav alfa- és béta-láncot eredményez. Ez a kristályszerkezet Ez a rá ható fizikai változóktól függ, például a nyomástól és a hőmérséklettől.. Ezért a karakterlánc konvertálható. Ha a nyomást szélsőséges szintre emelik, a láncok annyira összenyomódnak, hogy hangyasav kristályos polimerének tekintsék.
tulajdonságok
A hangyasav főbb tulajdonságainak leírására fogunk összpontosítani:
- a metánsav az szobahőmérsékleten színtelen, erős szúrós szagú folyadék. Molekulatömege 46 g/mol, olvadáspontja 8,4 °C, forráspontja 100,8 °C, ami magasabb, mint a vízé.
- Vízzel és poláros szerves oldószerekkel, például éterrel, acetonnal, metanollal és etanollal elegyedik.
- Ezzel szemben az aromás oldószerekben, például a benzolban és a toluolban rosszul oldódik, mivel a hangyasav szerkezetében kevés szénatom van.
- PKa értéke 3,77, amely savasabb, mint az ecetsav, ami azzal magyarázható, hogy a metilcsoport elektronsűrűséget biztosít a két oxigénnel oxidált szénatomnak. Ez a protonok (CH3COOH, HCOOH) savasságának enyhe csökkenését eredményezi.
- Miután a sav deprotonáltHCOO- formiát anionná alakul, amely delokalizálja a negatív töltést a két oxigénatom között. Ezért ez egy stabil anion, és felelős a hangyasav magas savasságáért.
Hangyasav felhasználások
Az élelmiszeripar és a mezőgazdaság
Olyan káros, mint a metánsav, antibakteriális hatása miatt kellő koncentrációban használják élelmiszer-tartósítószerként. Ugyanabból az okból, amiért a mezőgazdaságban használják, rovarölő tulajdonságokkal is rendelkezik. Antiszeptikus hatása is van a fűfélékre, és segít megelőzni a haszonállatok bélgázosodását.
A textil- és cipőipar
A textiliparban textíliák festésére és finomítására használják, és valószínűleg ez a sav legelterjedtebb felhasználási módja. A hangyasavat a bőr megmunkálására és az anyag szőrtelenítésére használják zsírtalanító hatása. A hangyasav deprotonálása HCOO- formiát anionná alakul, amely delokalizálja a negatív töltést a két oxigénatom között. Ezért ez egy stabil anion, és felelős a hangyasav magas savasságáért.
Közúti biztonság
Svájcban és Ausztriában a meghatározott ipari felhasználásokon kívül hangyasav-származékokat (formátum) használnak a téli utakon. a balesetek kockázatának csökkentése érdekében. Ez a kezelés hatékonyabb, mint az asztali só használata.
Remélem, hogy ezen információk birtokában többet megtudhat a hangyasavról, annak szerkezetéről és felhasználásáról.