
Az a víz, amelynek különböző paraméterei és jellemzői vannak, amelyek többé-kevésbé fontosak a felhasznált felhasználástól függően. Minőségének osztályozásakor az egyik legfontosabb kémiai paraméter a a víz keménysége. Bár a törvény nem ír elő semmilyen korlátot a víz keménységére és értékére az emberi fogyasztásban, ezúttal néhány közvetett összefüggés van. Lehetséges, hogy a víz, amelynek nagy keménységgel kell rendelkeznünk, és a norma nem állapít meg ennek értéket.
Ezen okokból fogjuk szentelni ezt a cikket, hogy elmondhassuk Önnek mindazt, amit a vízkeménységről tudnia kell.
Mekkora a víz keménysége

Mivel a törvény nem korlátozza az ivóvíz keménységét, a tudósoknak kell felmérniük a nagy keménységű ivóvíz következményeit. Ez a víz paraméter különféle következményekkel jár számos napi folyamatban akárcsak személyes mosáshoz vagy mosáshoz. A vízminőség osztályozásának egyik jellemzője a keménysége. Ha vizet fogunk használni öntözésre, akkor biztosan számos alkalommal látta, hogy bizonyos növényeknek sajátos vízkeménységre van szükségük.
A víz keménységét a benne lévő kalcium- és magnéziumionok összkoncentrációjaként határozzuk meg. Ez a két ion élő kation, és leggyakrabban a természetes vízben található meg. Vagyis a víz keménységét úgy lehetne meghatározni az összes többértékű kation összege, bár a magnézium plakáton sokkal fontosabb a víz globális keménysége.
Gyakran tapasztalhatjuk, hogy a víz keménységét a kalcium-karbonát tömegeként határozzuk meg, és milligrammban / liter oldatban mérjük. Ez nem azt jelenti, hogy a kemény vízben lévő összes kalcium kalcium-karbonátból származik. Egyszerűen a megállapodást általában úgy kezelik, mintha lenne. A víz keménységének kiszámításához a kalcium tömege és az mg és a kalcium-karbonát tömegének közötti együtthatókat alkalmazzuk. Ha elosztjuk a kapcsolatukat 10-nel, akkor nagyon használt egységünk lehet. Ez az az egység, amelyben a víz keménységét mérik. Hívták őket Francia hidrimetriai fokok, GHF vagy ºfH néven. Vannak más egységek is, amelyek jelzik a víz keménységét, de kevésbé elterjedtek.
Vízkeménységi értékek
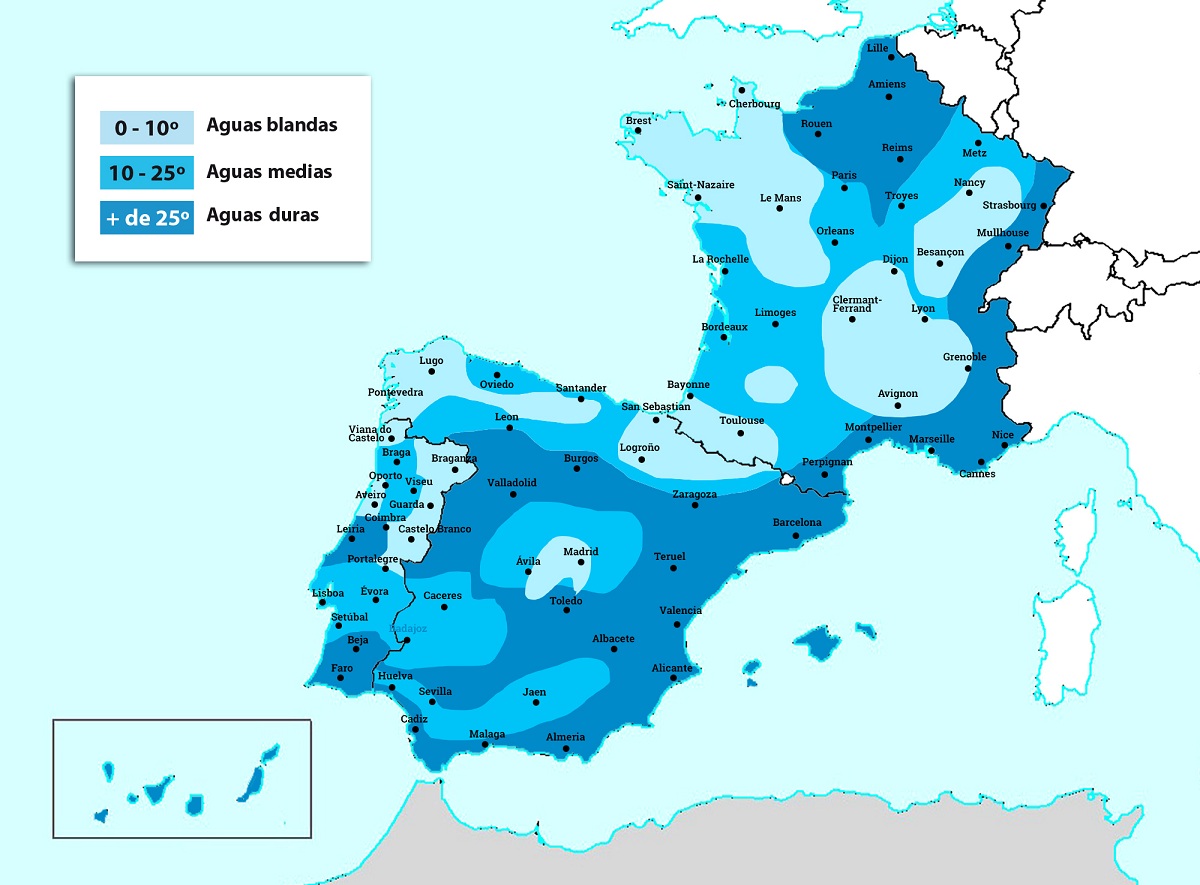
Ha egy víz nagyon édes vagy nagyon puha, akkor a keménységi értéke alacsonyabb, mint 7ºHH. Ez az érték azt jelzi, hogy minden liter vízben 70 milligramm kalcium-karbonát koncentrációja van. Másrészt nagyon kemény vízünk lesz, ha az 54ºfH-nál nagyobb mennyiséget mutat, vagy ami volt 540 mg kalcium-karbonát koncentráció minden liter vízhez.
Ha elemezzük a spanyol vizeket, akkor azt látjuk, hogy a keménység nagyon változatos. Azokban a vizekben, amelyek fő célpontja az emberi fogyasztás, nagyon sokféle keménységet találunk. Például egyes tartományokban, például Segovia vagy Madrid körül keménységi értékek vannak 5ºfH, míg más helyeken, például Almeríában, elérheti a 60-at. Fontos tudni, hogy a kemény víz milyen negatív hatásokat gyakorolhat a szervezetre.
A hidrogén-karbonátok jelenléte a vízben azt jelenti, hogy melegítés közben kalcium-karbonát csapadék képződhet. Ennek eredményeként meszes kéreg képződik. Bizonyára már mészként is ismeri. A köznyelvben a mész utal ezekre a fehér foltokra, amelyek a mosdók közelében vagy a zuhanyképernyőn keletkeznek. Ez a mész nem azt jelenti, hogy közvetlenül a betáplált vízből származik, hanem egy kémiai reakció, amely a kalcium és a szappan között történik. A víz keménysége nemcsak a tisztítási problémákra hat, hanem ipari környezetben is szilárd lerakódásokat eredményez, amelyek problémákhoz és meghibásodásokhoz vezethetnek a kazánokban, hűtőtornyokban és egyéb berendezésekben.
A meszes kéregeket általában úgy távolítják el, hogy az előzőhöz képest fordított kémiai reakciót váltanak ki. Vagyis úgy, hogy ismét oldható kalcium és hidrogén-karbonát képződik belőle. Használhat gyenge savat, mint pl ecetsav (megtalálhatjuk ecetben) vagy citromsav (megtalálhatjuk citromlében). Emiatt a mészhez használt legtöbb tisztítószer enyhén savas pH-jú terméken alapul.
A kemény víz negatív hatásai és annak megszüntetése
Ha a háztartási környezetbe megyünk, akkor azt látjuk, hogy a kemény víznek negatív hatásai vannak, például a varasodás felhalmozódása kazánokban, éttermekben, vízcsövekben és fűtőberendezésekben. Ezért szükség van nagyobb mennyiségű szappan és mosószer használatára ezeknek a maradványoknak a eltávolítására. Ha szappanokat használunk a csatorna maradványainak felszámolására, akkor ezt tudnunk kell ezek zsírsavak alkálifém-karboxilátjai. A kalcium ugyanis képes közvetlenül reagálni a szappannal. Könnyen láthatja a reakciót, mivel oldhatatlan csomók képződnek.
Ami a szappan tulajdonságainak elpusztítását segíti, az a habképesség. Minél keményebb a víz, annál nagyobb mennyiségű sampont vagy gélt kell használnunk ahhoz, hogy ugyanazt a habot érhessük el. A további mosószer használatának problémája az megnövekedett gazdasági kiadások és a a víz. A kemény víz másik hátránya, hogy a mosáshoz több mosószerre is szükség van.
Számos módszerre van szükség a felesleges keménység eltávolításához a vízből. A legalapvetőbb a víz melegítése. A víz keménységét hevítéssel csak akkor lehet megszüntetni, ha ez az úgynevezett átmeneti keménység. Az átmeneti keménység az, hogy ebben a kalcium-karbonát kalcium-hidrogén-karbonát formájában van. Ez a módszer azonban nem jó, mivel a mészt csövekben és vízmelegítőkben tárolják. A vízkőtelenítéshez a legjobb különféle vegyszereket használni. Ezek általában egy alkálifém karbonátjai, amelyek elősegítik a kémiai reakció kialakulását.
Remélem, hogy ezekkel az információkkal többet megtudhat a víz keménységéről.
