L'eau est un élément dont nous avons besoin pour vivre et pour qu'il y ait de la vie sur terre telle que nous la connaissons aujourd'hui. La molécule d'eau Il est composé de deux atomes d'hydrogène et d'un atome d'oxygène reliés par une liaison covalente. Cela signifie que les deux atomes d'hydrogène et celui d'oxygène sont unis grâce à ce qu'ils partagent des électrons entre eux. La formule de la molécule d'eau est H2O. La molécule d'eau possède de nombreuses caractéristiques et c'est grâce à elle que de nombreux processus donnent lieu au développement de la vie.
Par conséquent, nous allons dédier cet article pour vous dire tout ce que vous devez savoir sur la molécule d'eau.
Analyse de la molécule d'eau
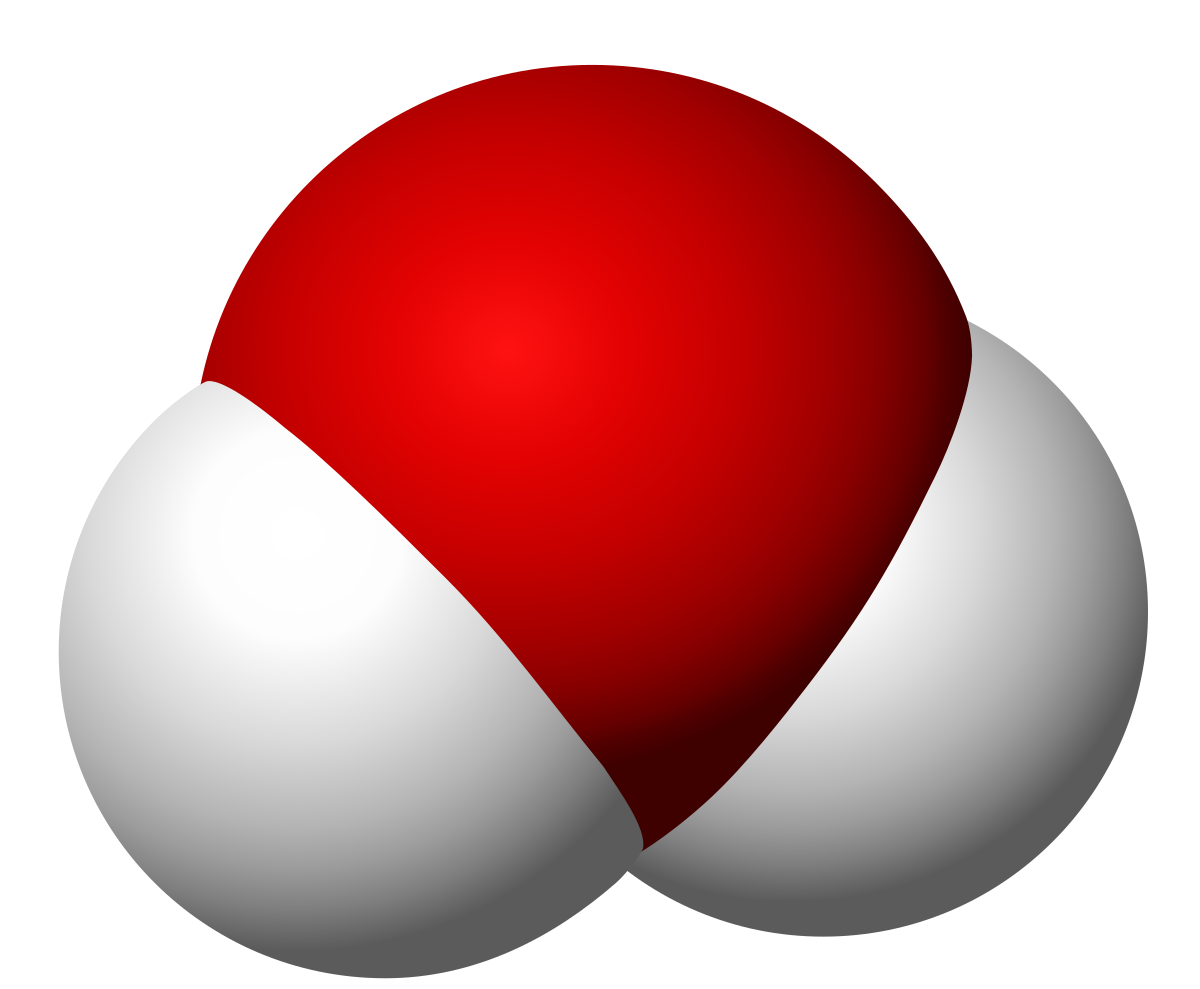
Si nous analysons cette molécule, nous pouvons voir que l'angle d'attachement de la liaison covalente entre l'hydrogène et l'oxygène commence à 104.5 degrés. Ceci peut être réalisé par analyse spectroscopique et aux rayons X. La distance moyenne entre les atomes d'hydrogène et d'oxygène est de 96.5 pm ou, ce qui est pareil, 9.65 • 10-8 millimètres.
Ces distances ne peuvent être comparées à tout ce que l'œil humain peut voir. La disposition des électrons dans la molécule d'eau est ce qui communique l'asymétrie électrique car il existe un niveau d'électronégativité différent entre l'hydrogène et l'oxygène. Nous appelons électronégativité à la capacité d'un atome à attirer des électrons partagés dans une liaison covalente. Nous rappelons qu'une liaison covalente est celle qui est établie entre deux atomes non métalliques.
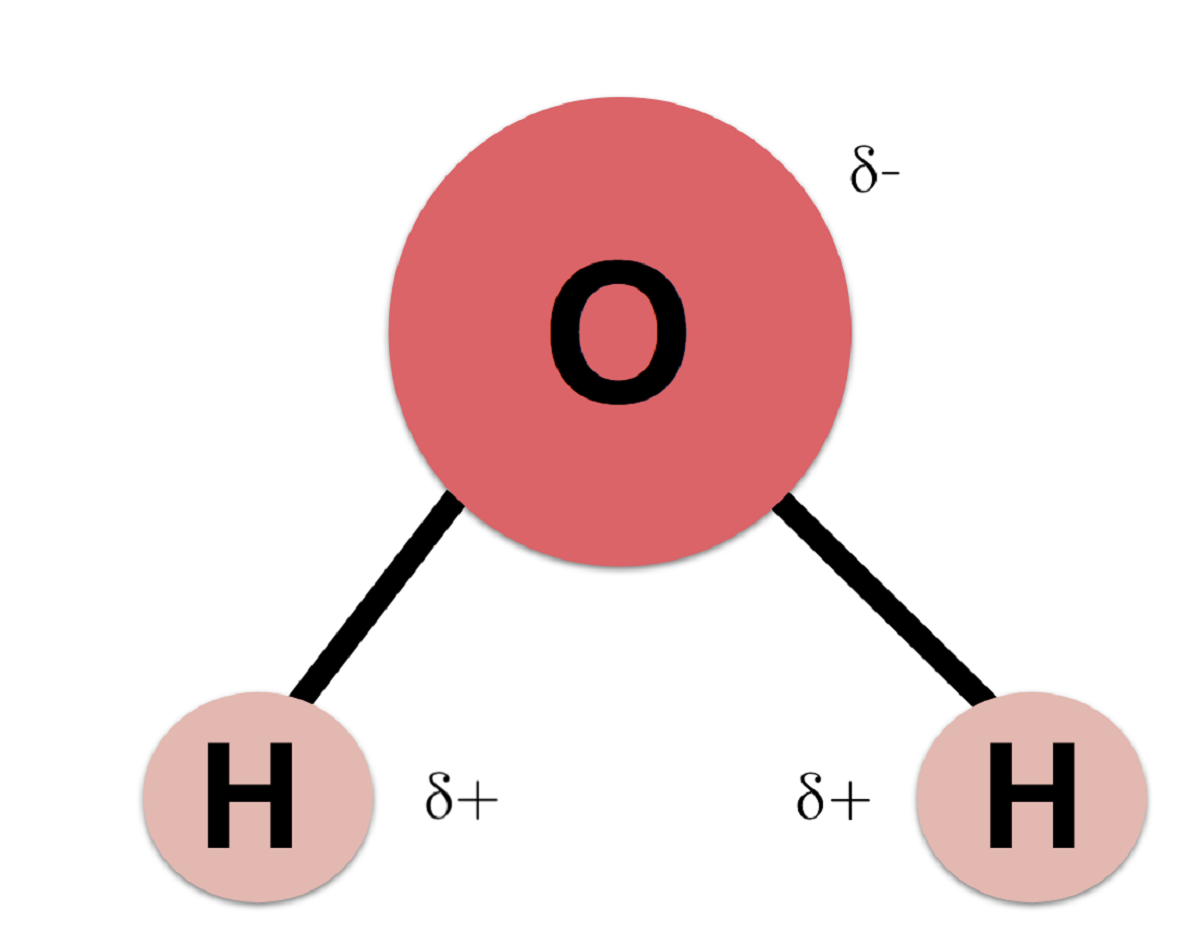
Étant donné que l'oxygène a plus d'électronégativité que l'hydrogène, les électrons sont plus susceptibles d'être plus proches de l'atome d'oxygène que de l'hydrogène. C'est parce que les électrons sont chargés négativement. Le fait que les électrons se dirigent principalement vers les atomes d'oxygène donne à l'atome d'hydrogène une certaine charge positive. Cette charge est appelée la charge partielle positive. Celle de l'oxygène s'appelle la charge partielle négative.
La différence entre les électrons positifs et négatifs proches des deux atomes fait de la molécule d'eau une molécule polaire. Autrement dit, la molécule a une partie avec un pôle négatif et une autre partie avec un pôle positif. Bien que toute la molécule soit neutre, c'est de ce caractère polaire que dérivent toutes ses propriétés physico-chimiques et biologiques.
Interactions entre molécules
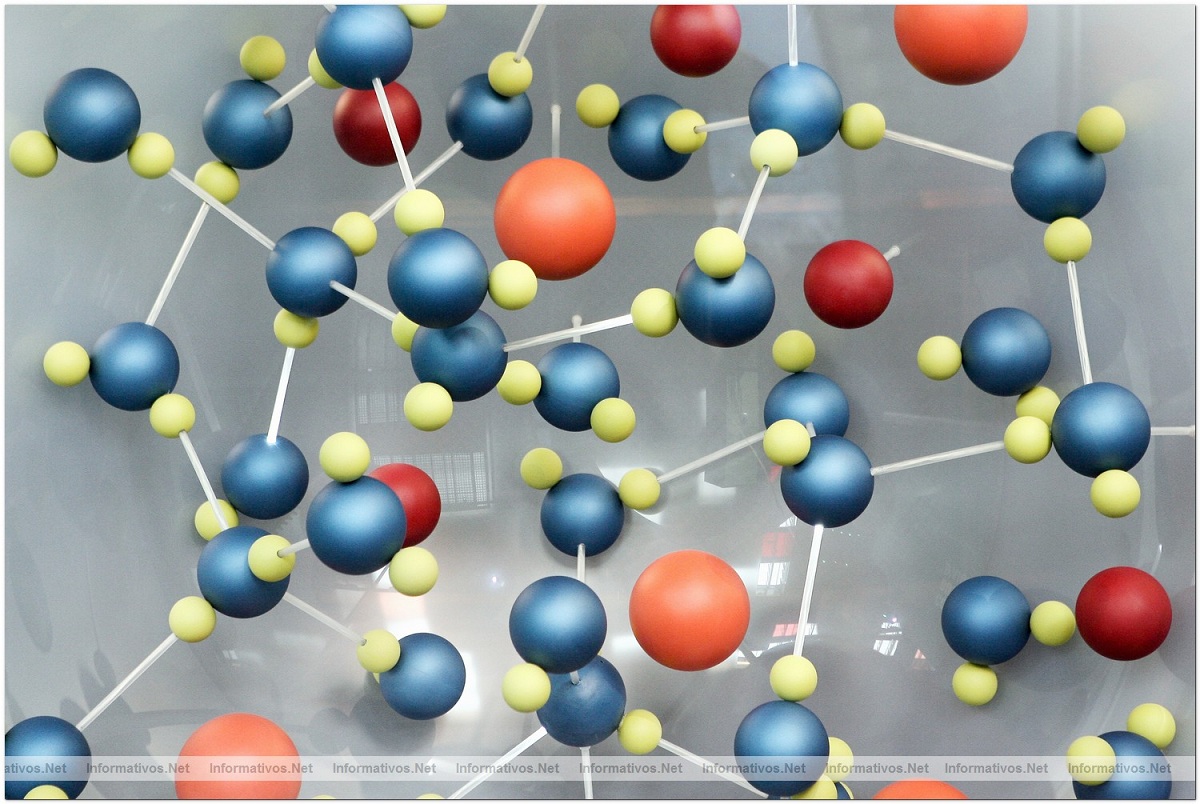
Lorsque plusieurs molécules d'eau sont très proches les unes des autres, elles sont capables d'établir une traction entre les atomes d'oxygène des molécules séparément. En effet, l'oxygène a une charge partielle négative et l'un des hydrogènes a une charge partielle positive. Par conséquent, la partie positive d'une molécule d'eau est attirée par la partie négative de l'autre molécule d'eau. Ce type d'interaction entre les molécules est appelé source d'hydrogène. Cela arrive souvent dans ces molécules car elles sont ordonnées de telle manière que chaque molécule d'eau est capable de s'associer à 4 molécules supplémentaires. Ce type d'interaction se produit avec la glace.
Les liaisons entre les hydrogènes ont lieu grâce au fait qu'il existe un atome avec une charge partielle négative et un hydrogène avec une charge partielle positive. Cela rend les liens non uniques à l'eau. Ces liaisons d'interaction se produisent également dans l'azote, le fluor et l'hydrogène dans d'autres molécules contenant des protéines et de l'ADN.
Voyons quelles sont les propriétés physico-chimiques de la molécule d'eau. Parmi ces propriétés et caractéristiques, nous pouvons souligner la capacité et le solvant. Il ne faut pas oublier que l'eau est considérée comme le solvant universel. Une autre caractéristique de la molécule d'eau est sa chaleur spécifique élevée et sa chaleur de vaporisation. Il a également une grande cohésion et adhérence, une densité anormale et fonctionne comme un réactif chimique.
Si nous utilisons les propriétés de l'eau, nous voyons qu'elle est capable de disperser un grand nombre de composés en son sein grâce à son caractère polaire. Comme nous l'avons mentionné précédemment, bien que la molécule entière soit neutre, le fait qu'elle ait une partie positive et une partie négative est ce que Il donne les propriétés physico-chimiques pour lesquelles l'eau est si nécessaire à la vie. Ainsi, il fonctionne avec des sels et d'autres substances ioniques dans lesquelles la molécule d'eau oriente ses pôles. Cette orientation des pôles est donnée en fonction des charges de deux ions, mettant le pôle négatif d'un côté et le pôle positif de l'autre. Par exemple, avec des substances polaires comme l'éthanol, l'eau agit de la même manière. Il oppose un pôle à un autre avec le signe opposé de la substance.
Propriétés de la molécule d'eau
La molécule d'eau a une chaleur spécifique élevée. Cette chaleur spécifique n'est rien de plus que la quantité de chaleur qui doit être administrée un gramme d'eau pour pouvoir élever sa température d'un degré. D'autre part, nous avons la chaleur de vaporisation. C'est la quantité de vapeur qui doit être appliquée à un gramme de liquide pour qu'il puisse passer dans un gramme de vapeur. Nous savons que la molécule d'eau a une chaleur spécifique élevée et une vaporisation grâce aux liaisons qui relient les atomes d'hydrogène. Autrement dit, pour élever la température de l'eau d'un degré, toutes les molécules doivent augmenter leur vibration. Pour ce faire, ils rompent les liaisons hydrogène afin de pouvoir passer un gramme d'eau liquide à un gramme d'eau vapeur.
Le fait qu'il ait une valeur élevée de chaleur de vaporisation est dû à sa capacité à passer. Une autre caractéristique de la molécule d'eau est la cohésion. La question est la tendance selon laquelle deux molécules doivent être unies. Grâce à nouveau aux liaisons hydrogène de la molécule d'eau, la cohésion est élevée. L'adhésion est la tendance de deux molécules différentes à se lier l'une à l'autre. Cela confère à la molécule d'eau une forte adhérence aux composés ioniques et polaires. C'est l'application qui a lieu lorsqu'il arrive que l'eau colle à différentes surfaces.
J'espère qu'avec ces informations, vous pourrez en savoir plus sur la molécule d'eau.