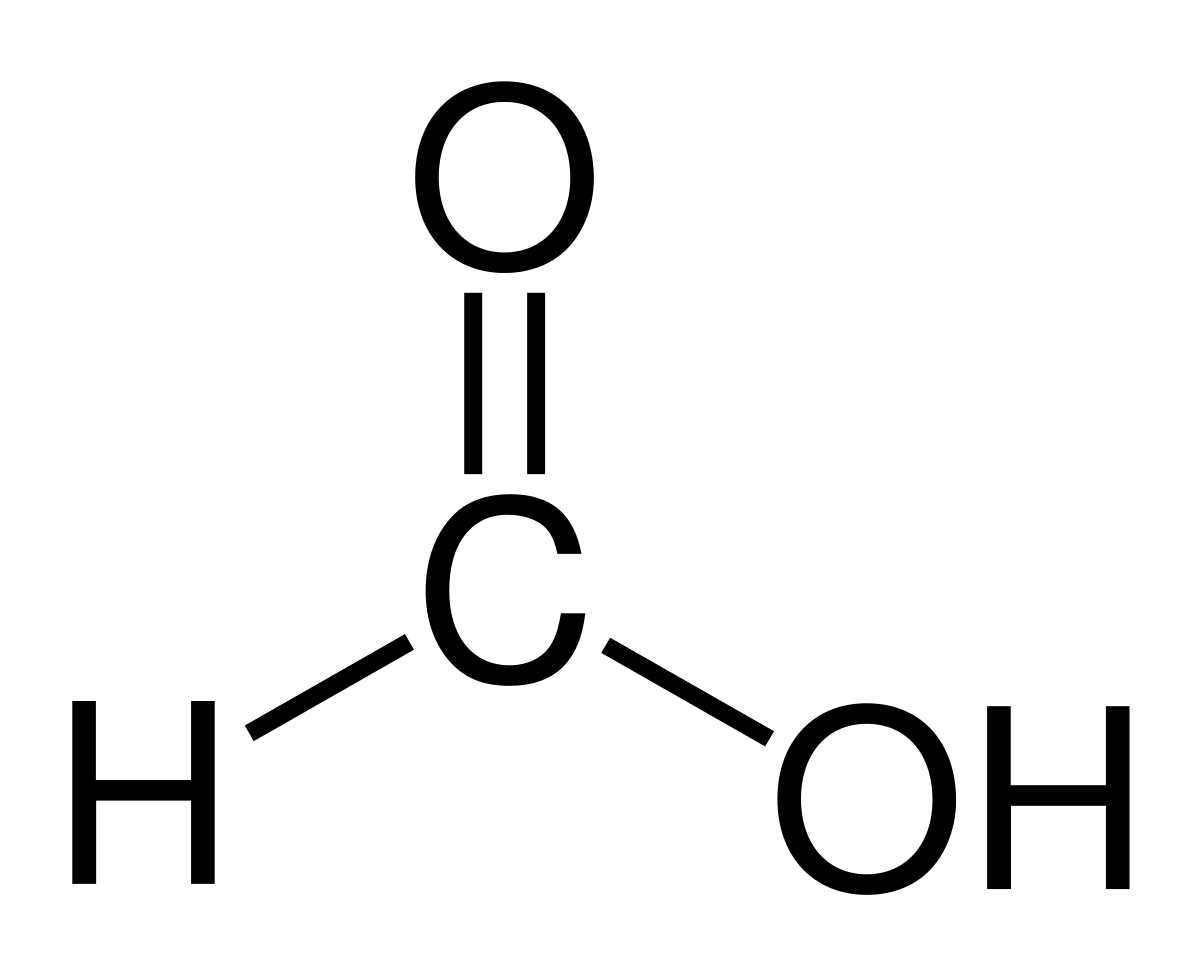
El l'acide formique o L'acide méthanoïque est le composé le plus simple et le plus petit de tous les acides organiques. Il a la formule moléculaire HCOOH avec un seul atome d'hydrogène lié à un atome de carbone. Son nom vient du mot formica, qui signifie fourmi en latin. C'est un composé assez important dans le monde de la chimie et largement utilisé aujourd'hui.
Pour cette raison, nous allons consacrer cet article à vous dire tout ce que vous devez savoir sur l'acide formique, ses caractéristiques et son importance.
Caractéristiques principales
Les naturalistes du XVe siècle ont découvert que certains types d'insectes (termicides), tels que fourmis, termites, abeilles et coléoptères, ils sécrètent ce composé qui rend leurs morsures douloureuses. De plus, ces insectes utilisent ce composé comme mécanisme d'attaque, de défense et de signalisation chimique.
Ils ont des glandes toxiques qui expulsent cet acide et d'autres, comme l'acide acétique, du corps sous forme de brouillard. L'acide formique est plus fort que l'acide acétique (CH3COOH) ; par conséquent, une quantité égale d'acide formique dissous dans l'eau se traduira par une solution avec un pH inférieur.
naturaliste anglais John Ray a réussi à isoler ce composé en 1671, extrait d'un grand nombre de fourmis. D'autre part, la première synthèse réussie de ce composé a été réalisée par le chimiste et physicien français Joseph Gay-Lussac en utilisant l'acide cyanhydrique (HCN) comme réactif.
acide formique dans la nature

L'acide formique peut exister au niveau terrestre, en tant que composant de la biomasse ou dans l'atmosphère, participant à un large éventail de réactions chimiques, il peut même être trouvé sous terre, dans le pétrole ou en phase gazeuse à sa surface.
En termes de biomasse, les insectes et les plantes sont les principaux producteurs de cet acide. Lorsque les combustibles fossiles brûlent, ils produisent de l'acide formique gazeux ; par conséquent, les moteurs de voiture libèrent cet acide dans l'atmosphère.
Toutefois, il y a beaucoup de fourmis qui vivent sur terre, et la production d'acide formique entre eux est des milliers de fois supérieure à la quantité d'acide méthanoïque produite par l'industrie humaine en un an. Les incendies de forêt sont également une source gazeuse d'acide formique.
Plus haut, dans la complexe matrice atmosphérique, se déroulent les processus photochimiques de synthèse de l'acide formique. A ce stade, de nombreux composés organiques volatils (COV) se dégradent sous l'action des rayonnements UV ou sont oxydés par le mécanisme radicalaire OH. La chimie atmosphérique riche et complexe est de loin la principale source d'acide méthanoïque sur Terre.
Structure atomique de l'acide formique
La figure ci-dessus montre la structure du dimère en phase gazeuse de l'acide formique. Les sphères blanches correspondent aux atomes d'hydrogène, les rouges aux atomes d'oxygène et les noires aux atomes de carbone.
Deux groupes peuvent être vus dans ces molécules : hydroxyle (-OH) et formyle (-CH=O), qui sont capables de former des liaisons hydrogène. Ces interactions sont de type OHO, où le groupe hydroxyle est le donneur H et le groupe formyle est le donneur O.
Cependant, H lié aux atomes de carbone n'a pas cette capacité. Ces interactions sont très fortes et l'hydrogène dans le groupe OH est plus acide en raison de l'atome H déficient en électrons ; donc, cet hydrogène stabilise davantage le pont. En raison de ce qui précède, l'acide formique existe sous forme de dimère et non de molécule individuelle.
Lorsque la température baisse, le dimère oriente ses liaisons hydrogène pour créer la structure la plus stable avec d'autres dimères, ce qui donne des chaînes alpha et bêta infinies d'acide méthanoïque. Cette structure cristalline Cela dépend des variables physiques qui agissent sur elle, telles que la pression et la température.. La chaîne est donc convertible. Si la pression est augmentée à des niveaux extrêmes, les chaînes sont suffisamment comprimées pour être considérées comme un polymère cristallin d'acide formique.
Propriétés
Nous allons nous concentrer sur la description des principales propriétés de l'acide formique :
- l'acide méthanoïque est un liquide incolore à température ambiante avec une forte odeur piquante. Il a un poids moléculaire de 46 g/mol, un point de fusion de 8,4 ºC et un point d'ébullition de 100,8 ºC, supérieur à celui de l'eau.
- Miscible avec l'eau et les solvants organiques polaires tels que l'éther, l'acétone, le méthanol et l'éthanol.
- Au contraire, dans les solvants aromatiques tels que le benzène et le toluène, il est peu soluble car l'acide formique a peu d'atomes de carbone dans sa structure.
- Il a un pKa de 3,77, qui est plus acide que l'acide acétique, ce qui peut s'expliquer par le fait que le groupe méthyle fournit une densité électronique à l'atome de carbone oxydé par deux oxygènes. Il en résulte une légère diminution de l'acidité des protons (CH3COOH, HCOOH).
- Une fois l'acide déprotoné, est converti en anion formiate HCOO-, qui délocalise la charge négative entre les deux atomes d'oxygène. Par conséquent, c'est un anion stable et il est responsable de l'acidité élevée de l'acide formique.
Utilisations de l'acide formique
L'industrie agro-alimentaire
Aussi nocif que l'acide méthanoïque, il est utilisé à des concentrations suffisantes comme conservateur alimentaire en raison de son effet antibactérien. Pour la même raison qu'il est utilisé en agriculture, il possède également des propriétés insecticides. Il a également un effet antiseptique sur les graminées et aide à prévenir les gaz intestinaux chez les animaux de la ferme.
L'industrie du textile et de la chaussure
Il est utilisé dans l'industrie textile pour teindre et raffiner les textiles et est probablement l'utilisation la plus courante de cet acide. L'acide formique est utilisé pour le traitement du cuir et l'épilation de ce matériau par son action dégraissante. La déprotonation de l'acide formique se transforme en anion formiate HCOO-, qui délocalise la charge négative entre les deux atomes d'oxygène. Par conséquent, c'est un anion stable et il est responsable de l'acidité élevée de l'acide formique.
Sécurité routière
En plus des utilisations industrielles spécifiées, les dérivés de l'acide formique (format) sont utilisés sur les routes d'hiver en Suisse et en Autriche pour réduire les risques d'accidents. Ce traitement est plus efficace que l'utilisation de sel de table.
J'espère qu'avec ces informations, vous pourrez en apprendre davantage sur l'acide formique, sa structure et ses utilisations.