Kemian alalla meillä on kemiallisia reaktioita, joita tapahtuu molekyylien ja atomien välillä. Tänään aiomme puhua hydrolyysi. Hydrolyysi on eräänlainen kemiallinen reaktio, joka voi tapahtua epäorgaanisten ja orgaanisten molekyylien tai ionien välillä. Hydrolyysin pääominaisuus on, että siihen liittyy vettä, jotta sidokset voidaan rikkoa.
Tässä artikkelissa aiomme kertoa sinulle kaikista hydrolyysin ominaisuuksista ja merkityksestä kemian alalla.
Mikä on hydrolyysi
Puhumme eräänlaisesta kemiallisesta reaktiosta, joka voi tapahtua sekä orgaanisten että epäorgaanisten molekyylien välillä. Olennainen edellytys on, että vettä on oltava mukana, jotta se voi rikkoa näiden molekyylien sidokset. Sana hydrolyysi tulee kreikkalaisesta hydrosta, joka tarkoittaa vettä, ja hajoamisesta, joka tarkoittaa repeämistä. Muotoon käännettynä hydrolyysi voidaan kutsua veden hajoamiseksi. Tässä tapauksessa puhumme joidenkin reaktanttien sidosten rikkoutumisesta veden osallistumisen kautta.
Vesimolekyyli koostuu kahdesta vetyatomista ja yhdestä happiatomista. Tämän atomien yhdistelmän ansiosta muodostuu tasapaino heikkojen happojen ja emästen suolojen ionien välillä. Hapot ja emäkset ovat kemian ja analyyttisen kemian yleisissä tutkimuksissa esiintyviä käsitteitä. Hydrolyysin voidaan sanoa olevan yksi yksinkertaisimmista kemiallisista reaktioista siellä. Hydrolyysin yleinen yhtälö on seuraava:
AB + H2 = AH + B-OH
On olemassa useita esimerkkejä hydrolyysistä, jossa vesi tai sinänsä ei voi rikkoa tiettyä kovalenttista sidosta. Muistamme, että kovalenttinen sidos on sellainen useat molekyylit, joilla ei ole metallisia ominaisuuksia, yhdistyvät muodostaen toisen uuden molekyylin. Niihin liittyvä sidos tunnetaan kovalenttisena sidoksena. Kun vesi yksinään ei pysty hajottamaan tätä sidosta, prosessi kiihtyy tai katalysoidaan happamoittamalla tai alustalla. Toisin sanoen hydrolyysi voidaan katalysoida ionien läsnä ollessa. Ja on, että on entsyymejä, jotka pystyvät katalysoimaan hydrolyysin kemiallisen reaktion.
Tärkeimmät ominaisuudet

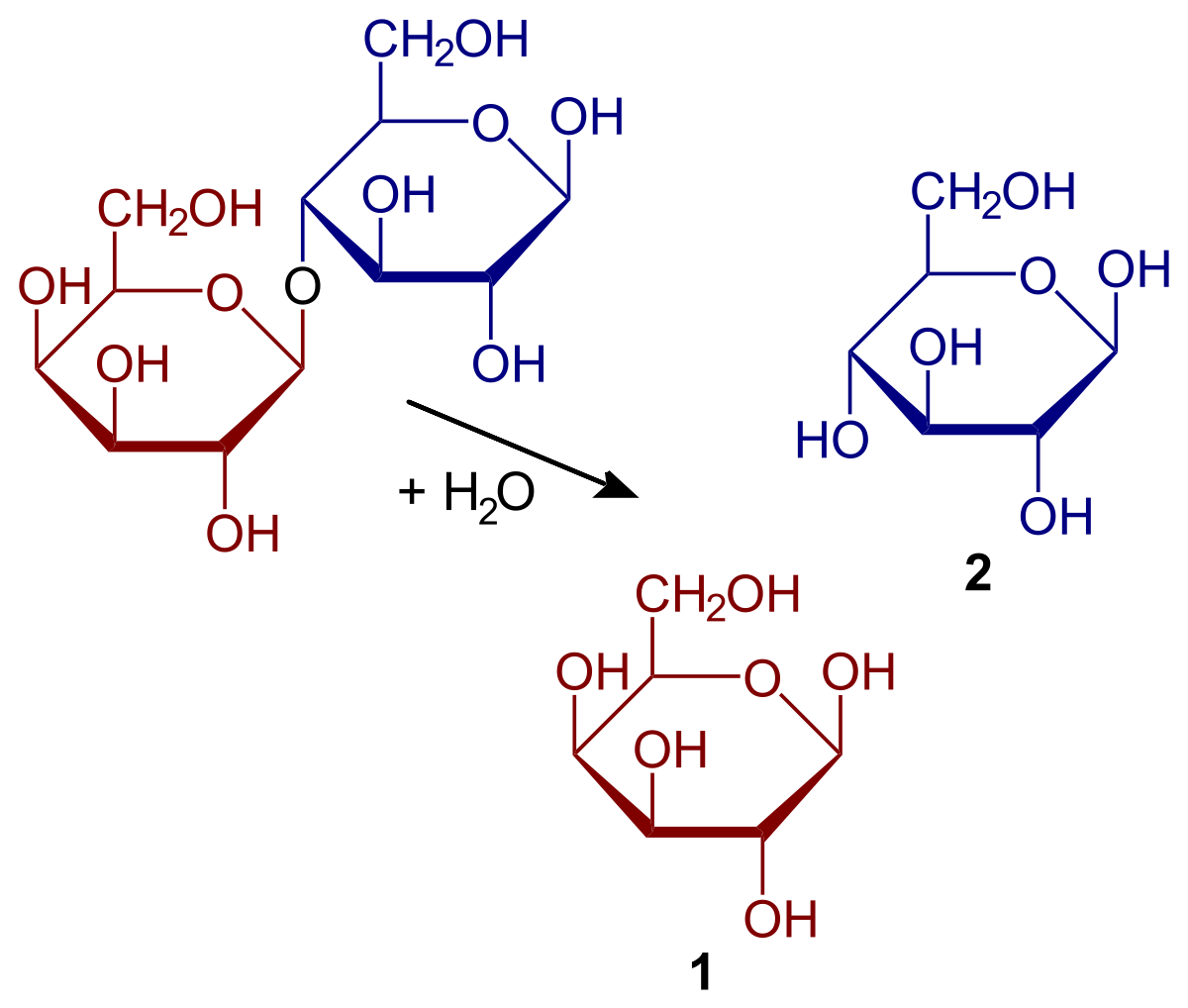
Katsotaanpa, mitkä ovat ominaisuudet ja mistä hydrolyysi koostuu. Tämän tyyppinen reaktio on erityinen paikka biomolekyylien suhteen. Ja se on, että sidokset, jotka pitävät molekyylien monomeerit yhdessä, ovat alttiita hydrolysoitumaan tietyissä olosuhteissa. Toisin sanoen kovalenttiset sidokset, joihin molekyylit ovat kiinnittyneet, voidaan rikkoa veden läsnä ollessa. Esimerkki tästä ovat sokerit. Sokerit pystyvät hydrolysoitumaan polysakkaridien hajottamiseksi monosakkarideiksi. Tämä tapahtuu glukosidaaseina tunnettujen entsyymien toiminnan ansiosta.
On otettava huomioon, että sidos ei hajoa vain molekyyli, joka on substraatti. Vesi itse myös murtuu ja lopulta erottaa ionit. Veden murtuminen H +: ksi ja OH-: ksi, missä H + päättyy A: lla ja OH– B.: llä. AB reagoi siten vesimolekyylin kanssa, jolloin syntyy kaksi tuotetta, AH ja B-OH.
Siksi voimme sanoa, että hydrolyysi on kemiallinen reaktio, joka on kondensaation vastainen. Kondensaatiosta, kaksi tuotetta liittyy vapauttamalla pieni molekyyli. Tämä pieni molekyyli on vettä. Päinvastoin, hydrolyysissä kuluu molekyyli, kun taas kondensaatiossa tämä elektrolyysimolekyyli kuluu, vapautuu tai tuotetaan.
Jotta ymmärtäminen olisi paljon helpompaa, selitämme esimerkin sokereista uudelleen. Oletetaan, että AB on sakkaroosidimeeri. Tässä tapauksessa A edustaa glukoosia ja B edustaa fruktoosia. Tämä sidos, joka tunnetaan glykosidinnimellä, voidaan hydrolysoida, jolloin saadaan kaksi erillistä monosakkaridia ja liuos. Sama tapahtuu oligosakkaridien ja polysakkaridien kanssa, jos entsyymit toimivat reaktioissa.
Tiedämme, että tällä kemiallisella reaktiolla on vain yksi suunta. Tämä tarkoittaa, että se on eräänlainen peruuttamaton hydrolyysi. Toisaalta on hydrolyysireaktioita, jotka ovat palautuvia, kun tasapaino on saavutettu.
Esimerkkejä hydrolyysireaktioista
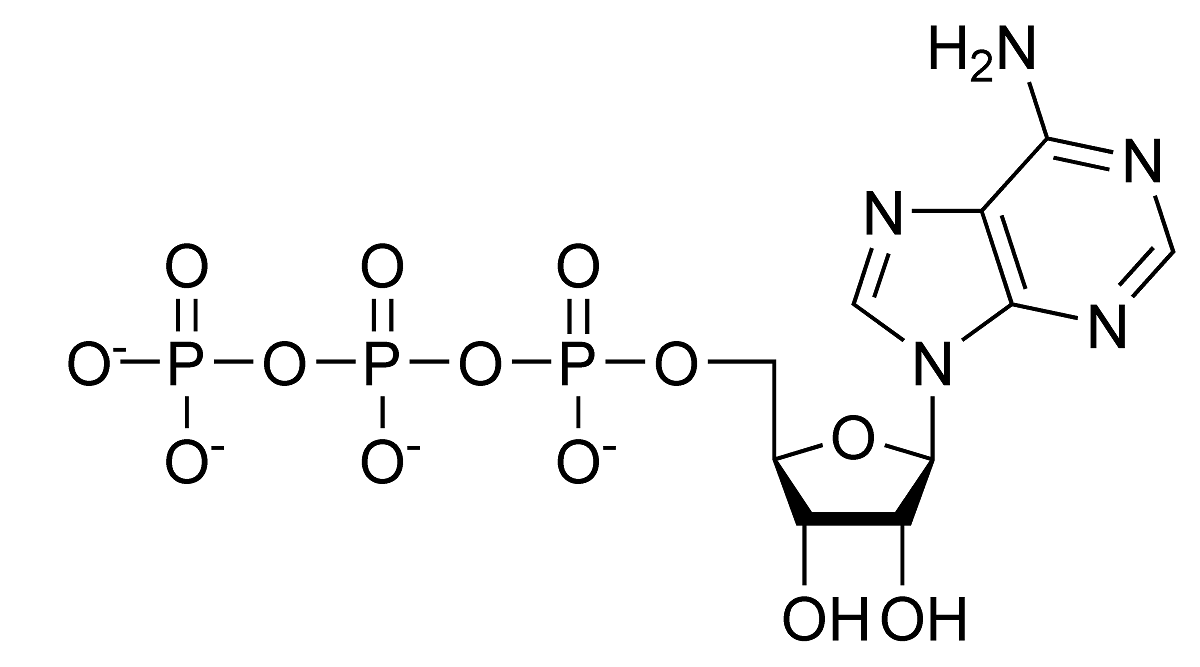
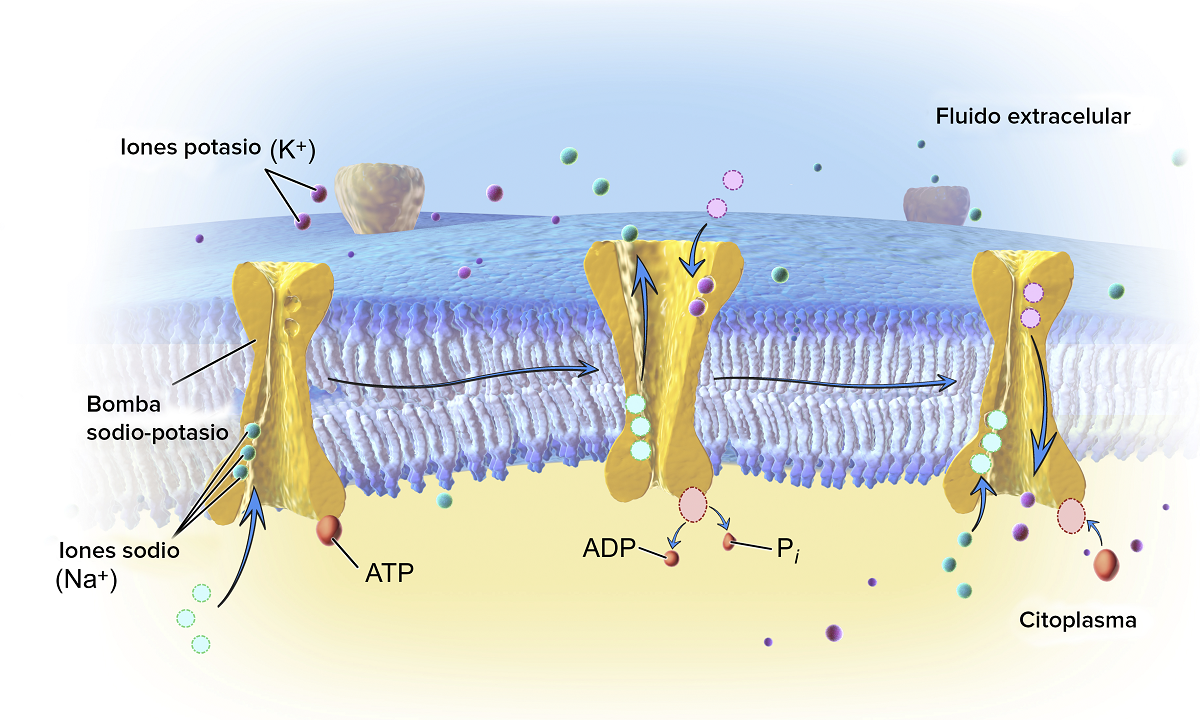
Katsotaanpa, mitkä ovat tärkeimmät esimerkit hydrolyysistä, joka tapahtuu luonnollisesti. Ensinnäkin on nähdä ATP: n hydrolyysireaktio. Tiedämme, että tämän molekyylin pH-arvot ovat vakaat välillä 6.8–7.4. Jos pH-arvot kuitenkin nousevat paljon emäksisemmiksi, se voi hydrolysoitua itsestään. Elävissä olennoissa hydrolyysiä katalysoivat entsyymit, jotka tunnetaan nimellä ATPaasit. Se on eräänlainen eksergoninen kemiallinen reaktio. Tämä tarkoittaa, että ADP: n entropia on suurempi kuin ATP: n, joten vapaa energian vaihtelu tapahtuu ATP: n hydrolyysillä. Tämän tyyppinen hydrolyysi käyttää lukuisia endergonisia reaktioita.
Yhdistetyt reaktiot ovat toinen reaktiotyyppi, jossa hydrolyysi tapahtuu. Joissakin tapauksissa sitä käytetään yhdisteen A muuttamiseksi yhdisteeksi B. Tunnetuin esimerkki hydrolyysistä esiintyy luonnollisesti vedessä. On kuin yksi vesimolekyyleistä voisi murtua ioneiksi ja vetyprotoni sitoutuu toisen vesimolekyylin happiatomiin. Tämä synnyttää hydroniumionin. Sitä voidaan kutsua enemmän kuin hydrolyysi veden autoionisaationa tai autoprotolyysinä.
Lopuksi toinen osista, joissa nämä reaktiot syntyvät yhteisellä tavalla proteiineissa. Tiedämme, että proteiinit ovat stabiileja molekyylejä ja niiden täydellisen hydrolyysin saavuttamiseksi tarvitaan äärimmäisiä olosuhteita. Muistamme, että proteiinit koostuvat aminohapoista. Eläville olennoille on kuitenkin annettu entsyymiarsenaali, joka sallii proteiinien hydrolyysin pohjukaissuolessa oleviksi aminohapoiksi.
Toivon, että näiden tietojen avulla voit oppia lisää hydrolyysistä ja sen ominaisuuksista.