
Voda koja ima različite parametre i karakteristike koje su više ili manje važne ovisno o upotrebi koja se podiže. Jedan od najvažnijih kemijskih parametara pri klasifikaciji njegove kvalitete je tvrdoća vode. Iako zakon ne zahtijeva ograničenje tvrdoće vode i njezinih vrijednosti u ljudskoj potrošnji, ovaj put neki indirektni odnosi. Moguće je da voda za koju moramo imati visoku tvrdoću i da norma ne utvrđuje nikakvu vrijednost.
Iz ovih razloga posvetit ćemo vam ovaj članak da bismo vam ispričali sve što trebate znati o tvrdoći vode koja je njena važnost.
Kolika je tvrdoća vode

Budući da zakon ne ograničava tvrdoću vode za piće, naučnici su ti koji moraju procijeniti koje su posljedice pijenja vode velike tvrdoće. Ovaj parametar vode ima različite posljedice u velikom broju dnevnih procesa kao i njegova upotreba za lično pranje ili pranje rublja. Jedna od karakteristika po kojoj se može klasificirati kvalitet vode je tvrdoća. Ako ćemo vodu koristiti za navodnjavanje, sigurno ste u više navrata vidjeli da određene biljke trebaju određenu tvrdoću vode.
Tvrdoća vode definira se kao ukupna koncentracija u njoj prisutnih jona kalcijuma i magnezijuma. Ova dva iona su živi kationi i najčešće se nalaze u prirodnoj vodi. Odnosno, tvrdoća vode bi se mogla definirati kao zbroj svih polivalentnih kationova koje ima, iako magnezijev poster ima mnogo važnije globalnu tvrdoću vode.
Često otkrijemo da se tvrdoća vode određuje kao masa kalcijum-karbonata i mjeri u miligramima po litri otopine. To ne znači da sav kalcijum u tvrdoj vodi dolazi iz kalcijum karbonata. Jednostavno, sporazum se obično tretira kao da jeste. Za izračunavanje tvrdoće vode koriste se koeficijenti u odnosu između mase kalcijuma i mg i mase kalcijum-karbonata. Ako odnos između njih podijelimo s 10, možemo dobiti vrlo korištenu jedinicu. To je jedinica u kojoj se mjeri tvrdoća vode. Oni se nazivaju Francuski hidrimetrijski stepeni poznati kao GHF ili ºfH. Postoje i druge jedinice za označavanje tvrdoće vode, ali one su manje raširene.
Vrijednosti tvrdoće vode
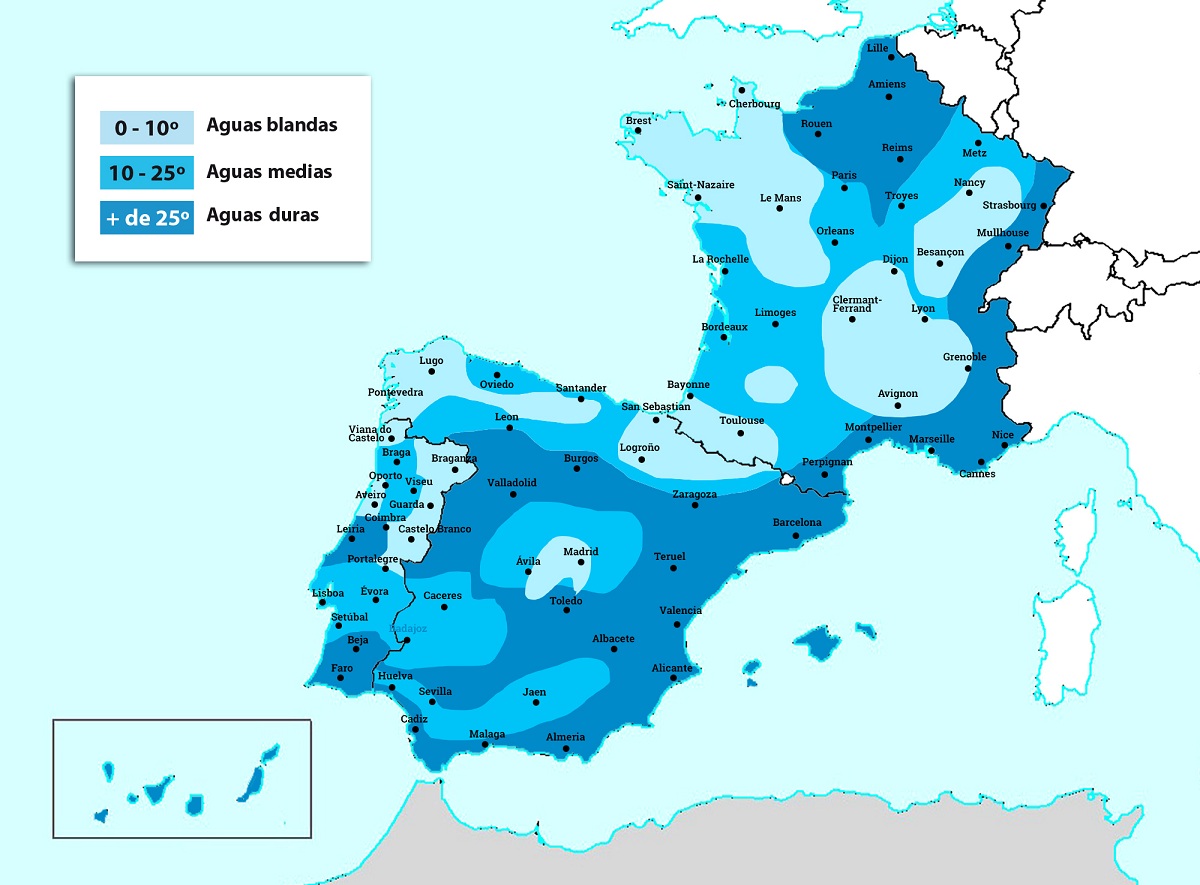
Ako je voda vrlo slatka ili vrlo mekana, tvrdoća će imati vrijednosti niže od 7ºfH. Ova vrijednost pokazuje da imaju koncentraciju od 70 miligrama kalcijum-karbonata za svaku litru vode. S druge strane, imat ćemo vrlo tvrdu vodu ako predstavlja količinu veću od 54ºfH ili ono što je bilo koncentracija od 540 miligrama kalcijum-karbonata za svaku litru vode.
Ako analiziramo španske vode, vidjet ćemo da postoji velika raznolikost tvrdoće. U vodama kojima se daje, a čija je glavna destinacija prehrana ljudi, nalazimo veliku količinu tvrdoće. Na primjer, neke provincije poput Segovije ili Madrida imaju vrijednosti tvrdoće oko sebe 5ºfH, dok na drugim mjestima poput Almerije može doseći i 60. Važno je znati koji negativni efekti tvrda voda može imati na tijelo.
Prisustvo bikarbonata u vodi znači da precipitati kalcijum-karbonata mogu nastati zagrijavanjem. To rezultira stvaranjem vapnenastih kora. Sigurno ga već obično znate kao kreč. U razgovornom jeziku, vapno se koristi za označavanje ovih bijelih mrlja koje nastaju u blizini umivaonika ili na zaslonu tuša. Ovaj kreč ne znači da dolazi izravno iz vode u zalihi, već je to kemijska reakcija koja se događa između kalcijuma i sapuna. Tvrdoća vode ne utječe samo na probleme čišćenja, već također stvara čvrste naslage u industrijskim okruženjima što može dovesti do problema i kvarova u kotlovima, rashladnim tornjevima i drugoj opremi.
Vapnene kore se obično uklanjaju uzrokujući obrnutu hemijsku reakciju na prethodnu. Odnosno, tako da se ponovo formira u topljivi kalcijum i bikarbonat. Možete koristiti slabu kiselinu kao što je octena kiselina (možemo je naći u octu) ili limunska kiselina (možemo je naći u limunovom soku). Iz tog razloga, većina proizvoda za čišćenje koji se koriste za kreč temelje se na proizvodima s blago kiselim pH.
Negativni efekti tvrde vode i kako je eliminisati
Ako krenemo u domaće okruženje, vidimo da tvrda voda ima negativne efekte poput nakupljanja krasta u kotlovima, kafeterijama, vodovodnim cijevima i grijačima. Zbog toga je potrebno ukloniti veće ostatke sapuna i deterdženta. Ako koristimo sapune kako bismo mogli eliminirati ostatke kanala, to moramo znati oni su karboksilati alkalnih metala iz masnih kiselina. To je zato što kalcij može direktno reagirati sapunom. Reakciju možete lako vidjeti dok se stvaraju netopive nakupine.
Ono što pomaže uništavanju svojstava sapuna je njegova sposobnost pjenjenja. Što će voda biti tvrđa, to će nam trebati veća količina šampona ili gela da bismo mogli postići istu pjenu. Problem s korištenjem više deterdženta je veća ekonomska potrošnja i zagađenje Voda. Još jedan nedostatak tvrde vode je što vam je potrebno i više deterdženta za pranje odjeće.
Potrebno je nekoliko metoda za uklanjanje viška tvrdoće iz vode. Najosnovnije je zagrijavanje vode. Tvrdoća vode može se eliminirati zagrijavanjem samo ako je to takozvana privremena tvrdoća. Privremena tvrdoća je ta da je kalcijum karbonat u obliku kalcijum bikarbonata. Međutim, ova metoda nije dobra jer se kreč skladišti u cijevima i bojlerima. Za uklanjanje kamenca najbolje je koristiti razne hemikalije. To su obično karbonati alkalnih metala koji pomažu u stvaranju hemijske reakcije.
Nadam se da ćete s ovim informacijama saznati više o tvrdoći vode.
