В областта на химията имаме химичните реакции, които протичат между молекулите и атомите. Днес ще говорим за хидролиза. Хидролизата е вид химическа реакция, която може да възникне между неорганични и органични молекули или йони. Основната характеристика на хидролизата е, че тя включва участието на вода, за да могат връзките да се разкъсат.
В тази статия ще ви разкажем за всички характеристики и значение на хидролизата в областта на химията.
Какво е хидролиза
Говорим за вид химическа реакция, която може да възникне между органични и неорганични молекули. Същественото условие е водата да бъде замесена, за да може разкъсват връзките на тези молекули. Думата хидролиза идва от гръцкото hydro, което означава вода и от лизис, което означава разкъсване. Преведено във форма, хидролизата може да бъде известна като разграждане на водата. В този случай говорим за разкъсване на връзките на някои реагенти чрез участието на вода.
Водната молекула се състои от два водородни атома и един кислородни атоми. Благодарение на тази комбинация от атоми се формира равновесие между йони на соли на слаби киселини и основи. Киселините и основите са понятия, които се появяват в общите изследвания на химията и аналитичната химия. Може да се каже, че хидролизата е една от най-простите химически реакции там. Общото уравнение за хидролиза е както следва:
AB + H2O = AH + B-OH
Има няколко примера за хидролиза, при които водата или сама по себе си не може да разруши определена ковалентна връзка. Помним, че ковалентната връзка е тази, в която няколко молекули с неметални характеристики се обединяват, за да образуват друга нова молекула. Връзката, която се присъединява към тях, е известна като ковалентна връзка. Когато само водата не е в състояние да разруши тази връзка, процесът се ускорява или катализира чрез подкисляване или алкализиране на средата. Тоест, в присъствието на йони, хидролизата може да бъде катализирана. И има ензими, които са способни да катализират химическата реакция на хидролиза.
ключови характеристики

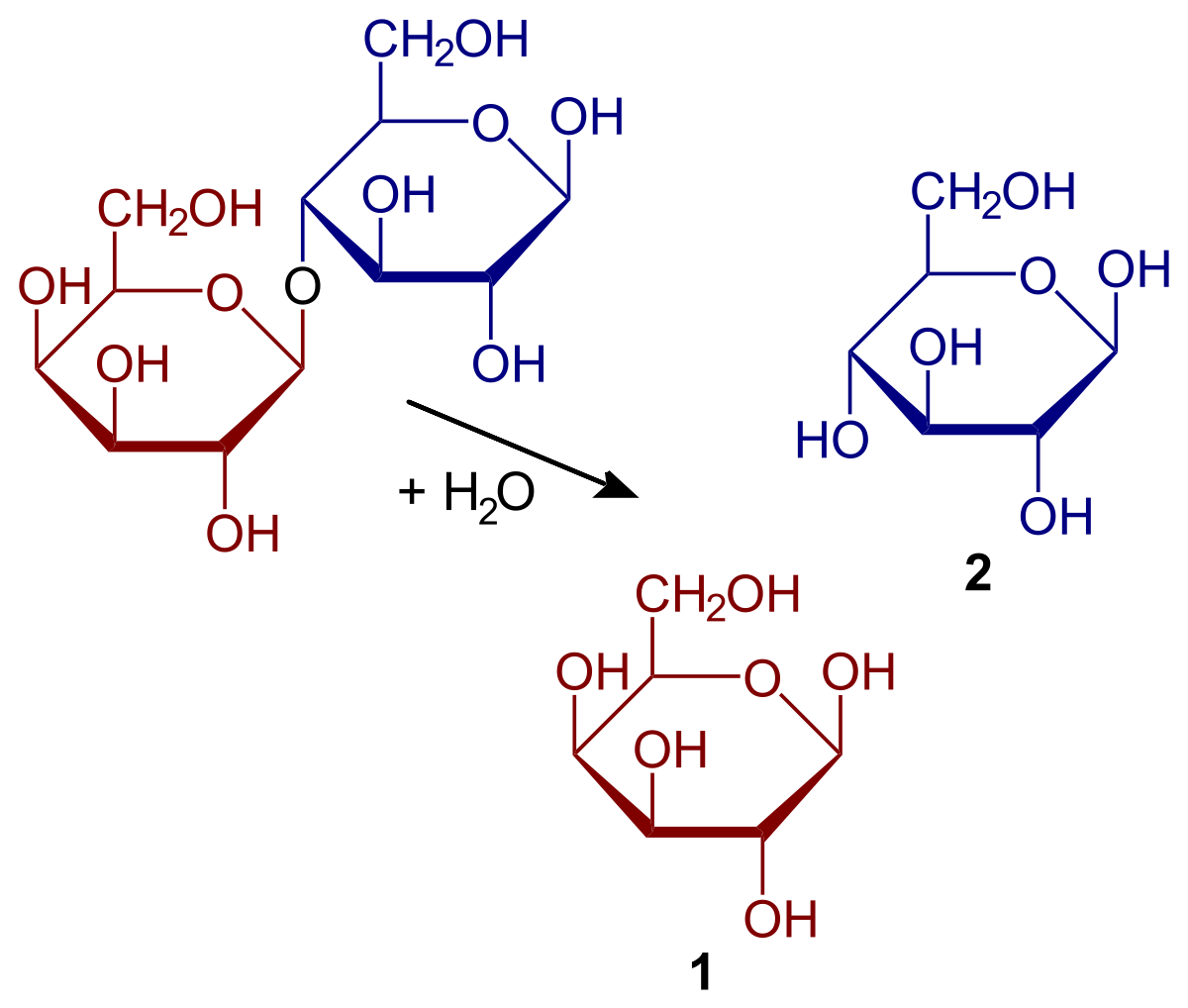
Нека да видим какви са характеристиките и от какво се състои хидролизата. Този тип реакция заема специално място, когато става въпрос за биомолекули. И то е, че връзките, които държат мономерите на молекулите заедно, са податливи на хидролиза при определени условия. Тоест, ковалентните връзки, с които са прикрепени молекулите, могат да се разкъсат в присъствието на вода. Пример за това са захарите. Захарите са способни да хидролизират, за да разграждат полизахаридите до монозахариди. Това се случва благодарение на действието на ензимите, известни като глюкозидази.
Трябва да се има предвид, че не само молекулата е субстрат, който разрушава връзката. Самата вода също се счупва и в крайна сметка разделя йоните. Водата се счупва в H + и OH–, където H + завършва с A, а OH– с B. AB по този начин реагира с водна молекула, образувайки два продукта, AH и B-OH.
Следователно можем да кажем, че хидролизата е химическа реакция, противоречаща на кондензацията. От конденз, два продукта се съединяват чрез освобождаване на малка молекула. Тази малка молекула е вода. Напротив, при хидролизата се консумира молекула, докато при кондензацията тази молекула за електролиза се консумира, освобождава или произвежда.
За да го улесним много по-лесно, ще обясним отново примера със захарите. Нека приемем, че AB е захарозен димер. В този случай А представлява глюкоза, а В представлява фруктоза. Тази връзка, която е известна с гликозидното наименование, може да бъде хидролизирана, за да се получат два отделни монозахарида и разтвора. Същото се случва и с олигозахаридите и полизахаридите, ако ензимите са тези, които действат в реакциите.
Знаем, че тази химическа реакция има само една посока. Това означава, че това е вид необратима хидролиза. От друга страна, има реакции на хидролиза, които са обратими след достигане на равновесие.
Примери за реакции на хидролиза
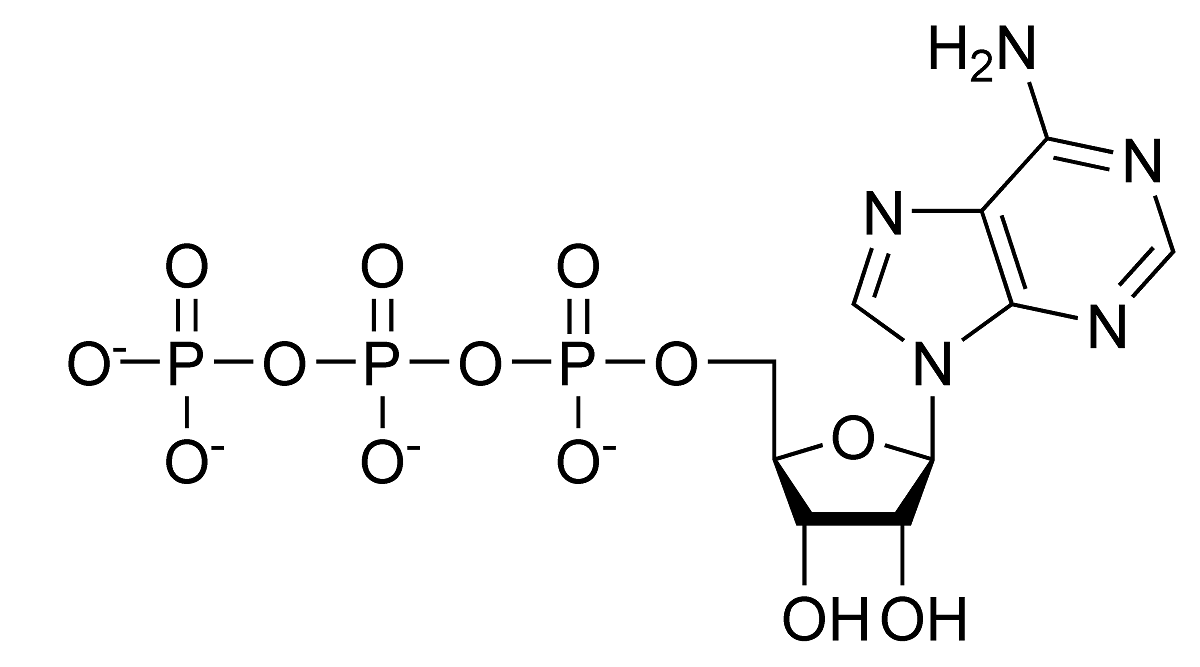
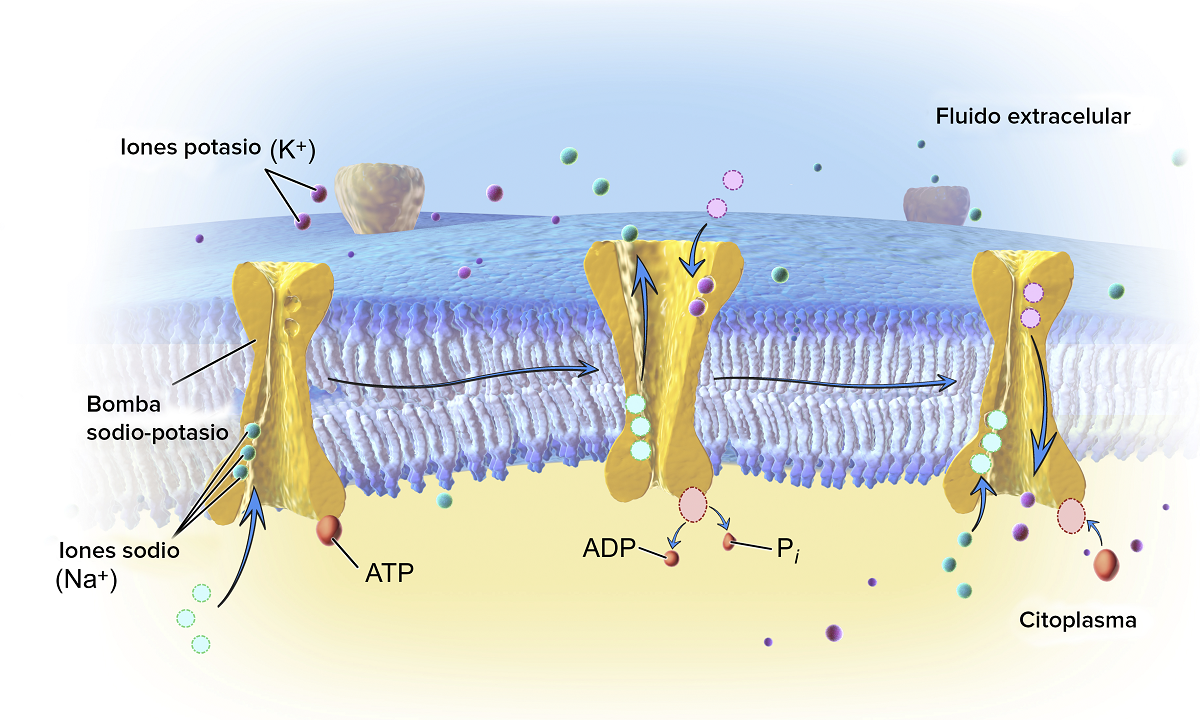
Нека да видим кои са основните примери за хидролиза, които се срещат естествено. На първо място, вижте реакцията на хидролиза на АТФ. Знаем, че тази молекула има стабилни стойности на рН между 6.8 и 7.4. Ако обаче стойностите на рН се увеличат, за да станат много по-алкални, той може да се хидролизира спонтанно. При живите същества хидролизата се катализира от ензими, известни с името на АТФази. Това е вид ексергонична химическа реакция. Това означава, че ентропията на ADP е по-голяма от тази на ATP, така че варирането на свободната енергия се получава чрез хидролиза на ATP. Този тип хидролиза използва множество ендергонични реакции.
Свързаните реакции са друг вид реакции, при които се получава хидролиза. В някои случаи се използва за превръщане на съединение А в съединение В. Най-известният пример за хидролиза се среща естествено във вода. Сякаш една от водните молекули може да се счупи на йони и водородният протон се свързва с кислородния атом на другата водна молекула. Това поражда хидрониевия йон. Може да се нарече нещо повече от хидролиза като автоионизация или автопротолиза на вода.
И накрая, друга от частите, където тези реакции се генерират по общ начин в протеините. Знаем, че протеините са стабилни молекули и за постигане на пълната им хидролиза са необходими екстремни условия. Помним, че протеините са изградени от аминокиселини. Живите същества обаче са снабдени с арсенал от ензими, които позволяват хидролизата на протеини в аминокиселини в дванадесетопръстника.
Надявам се, че с тази информация можете да научите повече за хидролизата и нейните характеристики.