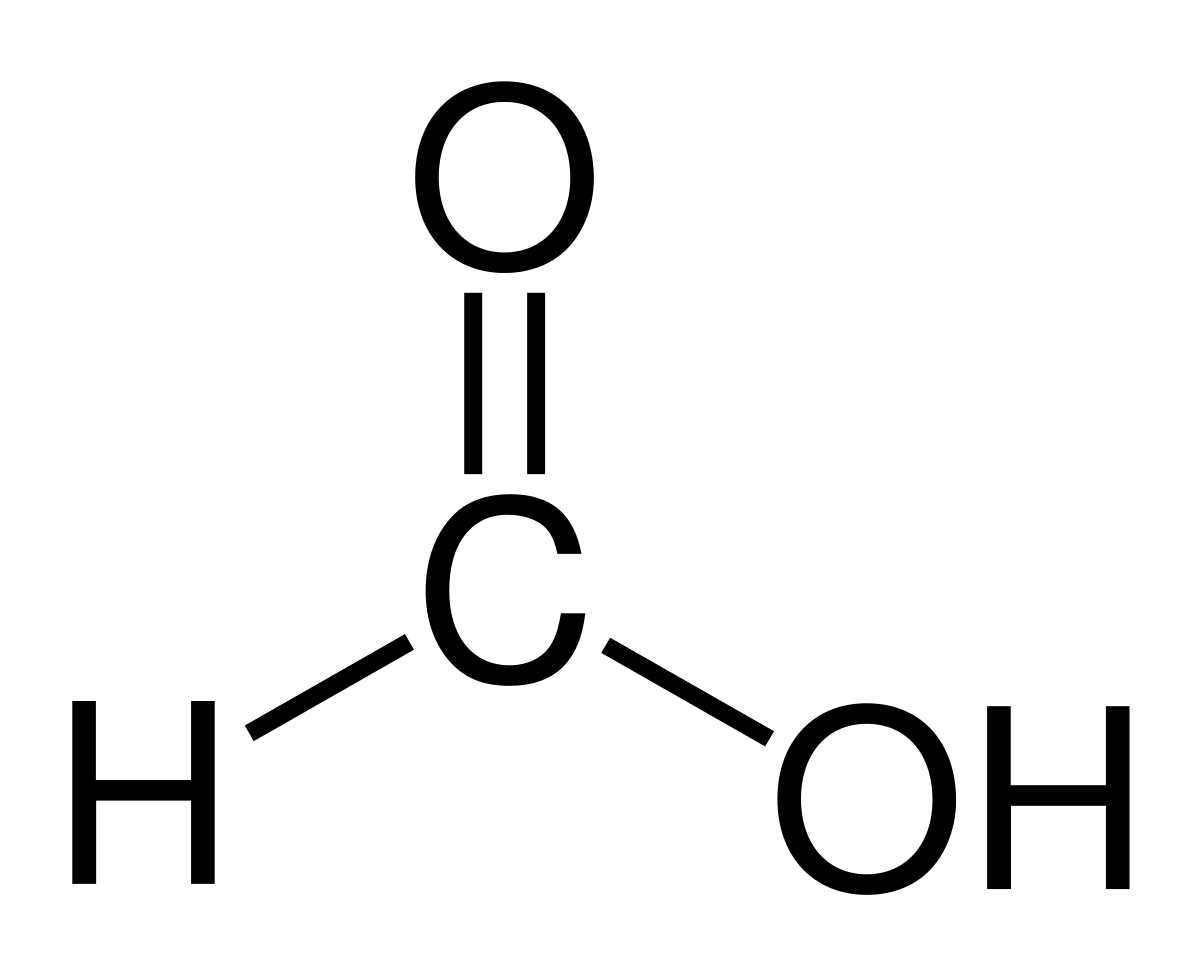
El мравчена киселина o Метановата киселина е най-простото и най-малкото съединение от всички органични киселини. Той има молекулна формула HCOOH с само един водороден атом, свързан с въглероден атом. Името му идва от думата formica, която на латински означава мравка. Това е доста важно съединение в света на химията и широко използвано днес.
Поради тази причина ще посветим тази статия, за да ви кажем всичко, което трябва да знаете за мравчена киселина, нейните характеристики и значение.
ключови характеристики
Натуралистите от XV век откриват, че някои видове насекоми (термициди), като напр мравки, термити, пчели и бръмбари, те отделят това съединение, което прави ухапванията им болезнени. В допълнение, тези насекоми използват това съединение като механизъм за атака, защита и химическа сигнализация.
Те имат токсични жлези, които изхвърлят тази и други киселини, като оцетната киселина, от тялото под формата на мъгла. Мравчена киселина е по-силна от оцетната киселина (CH3COOH); следователно, еднакво количество мравчена киселина, разтворена във вода, ще доведе до разтвор с по-ниско рН.
Английският натуралист Джон Рей постига изолирането на това съединение през 1671 г, извлечен от голям брой мравки. От друга страна, първият успешен синтез на това съединение е извършен от френския химик и физик Жозеф Гей-Люсак, използвайки циановодородна киселина (HCN) като реагент.
мравчена киселина в природата

Мравчена киселина може да съществува на земни нива, като компонент на биомасата или в атмосферата, участвайки в широк спектър от химични реакции, дори може да се намери под земята, в нефт или в газообразна фаза на повърхността си.
По отношение на биомасата, насекомите и растенията са основните производители на тази киселина. Когато изкопаемите горива горят, те произвеждат газообразна мравчена киселина; следователно автомобилните двигатели изпускат тази киселина в атмосферата.
Въпреки това, на земята живеят много мравки, и производството на мравчена киселина между тях е хиляди пъти по-голямо от количеството метанова киселина, произведена от човешката индустрия за една година. Горските пожари също са газообразен източник на мравчена киселина.
По-високо, в сложната атмосферна матрица, протичат фотохимични процеси за синтез на мравчена киселина. В този момент много летливи органични съединения (ЛОС) се разграждат под действието на UV лъчение или се окисляват по механизма на OH радикала. Богатата и сложна атмосферна химия е далеч основният източник на метанова киселина на Земята.
Атомна структура на мравчена киселина
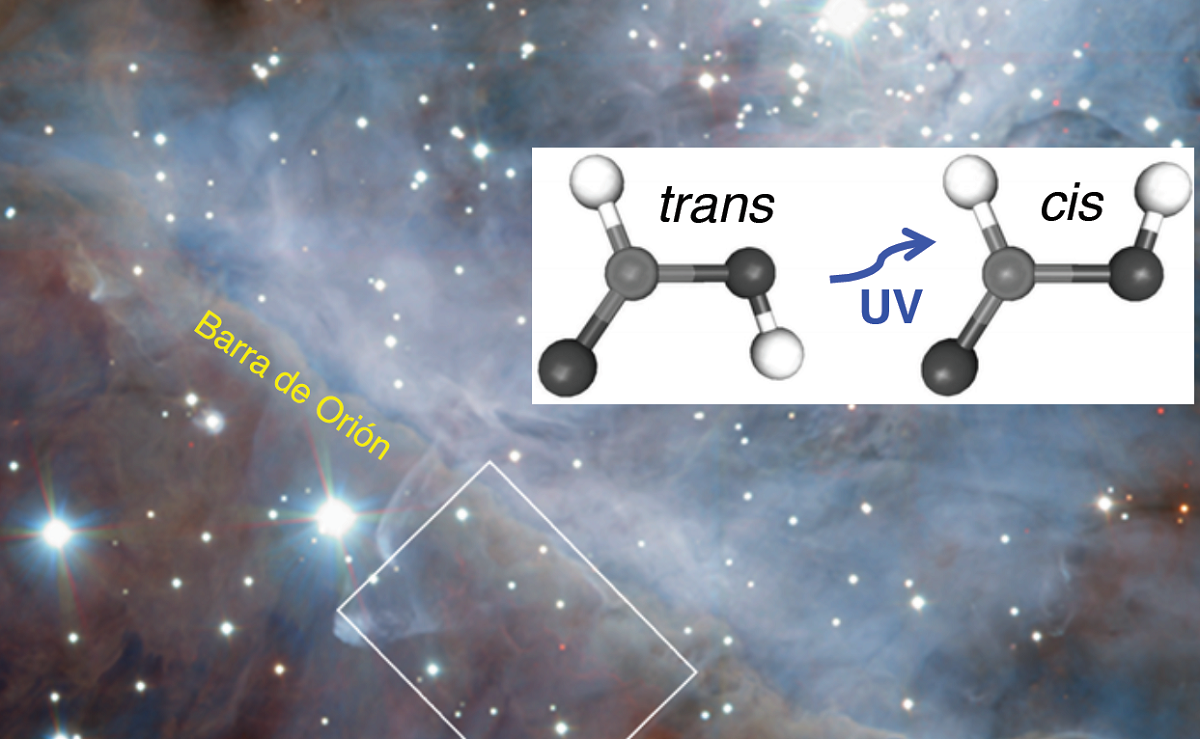
Фигурата по-горе показва структурата на димера в газовата фаза на мравчена киселина. Белите сфери съответстват на водородни атоми, червените на кислородни атоми, а черните на въглеродни атоми.
В тези молекули могат да се видят две групи: хидроксил (-OH) и формил (-CH=O), които са способни да образуват водородни връзки. Тези взаимодействия са от типа OHO, където хидроксилната група е Н донор, а формилната група е О донор.
Въпреки това, Н, свързан с въглеродните атоми, няма тази способност. Тези взаимодействия са много силни и водородът в ОН групата е по-кисел поради електрон-дефицитния Н атом; По този начин, този водород допълнително стабилизира моста. В резултат на горното мравчена киселина съществува като димер, а не като отделна молекула.
Тъй като температурата пада, димерът ориентира своите водородни връзки, за да създаде най-стабилната структура с други димери, което води до безкрайни алфа и бета вериги на метанова киселина. Тази кристална структура Зависи от физическите променливи, които действат върху него, като налягане и температура.. Следователно веригата е конвертируема. Ако налягането се увеличи до екстремни нива, веригите се компресират достатъчно, за да се считат за кристален полимер на мравчена киселина.
свойства
Ще се съсредоточим върху описанието на основните свойства на мравчена киселина:
- метанова киселина е безцветна течност при стайна температура със силна остра миризма. Има молекулно тегло от 46 g/mol, точка на топене 8,4ºC и точка на кипене от 100,8ºC, по-висока от тази на водата.
- Смесва се с вода и полярни органични разтворители като етер, ацетон, метанол и етанол.
- За разлика от тях, в ароматни разтворители като бензол и толуен, той е слабо разтворим, тъй като мравчена киселина има малко въглеродни атоми в структурата си.
- Има pKa от 3,77, която е по-кисела от оцетната киселина, което може да се обясни, защото метиловата група осигурява електронна плътност на въглеродния атом, окислен от два кислорода. Това води до леко намаляване на киселинността на протоните (CH3COOH, HCOOH).
- След като киселината е депротонирана, се превръща в формиат анион HCOO-, което делокализира отрицателния заряд между двата кислородни атома. Следователно, той е стабилен анион и е отговорен за високата киселинност на мравчена киселина.
Употреби на мравчена киселина
Хранителната и селскостопанската индустрия
Вреден като метанова киселина, използва се в достатъчни концентрации като хранителен консервант поради антибактериалния си ефект. Поради същата причина, поради която се използва в селското стопанство, той има и инсектицидни свойства. Освен това има антисептичен ефект върху тревите и помага за предотвратяване на чревни газове при селскостопански животни.
Текстилната и обувната промишленост
Използва се в текстилната индустрия за боядисване и рафиниране на текстил и е може би най-често срещаната употреба на тази киселина. Мравчена киселина се използва за обработка на кожа и депилация на този материал чрез обезмасляващото му действие. Депротонирането на мравчена киселина се превръща в формиат анион HCOO-, който делокализира отрицателния заряд между двата кислородни атома. Следователно, той е стабилен анион и е отговорен за високата киселинност на мравчена киселина.
Пътна безопасност
В допълнение към посочените промишлени употреби, производните на мравчена киселина (формат) се използват по зимните пътища в Швейцария и Австрия за намаляване на риска от злополуки. Това лечение е по-ефективно от използването на готварска сол.
Надявам се, че с тази информация можете да научите повече за мравчена киселина, нейната структура и нейното приложение.