
В областта на химията, йонизационна енергия. Той се отнася до минималното количество енергия, което е необходимо, за да може да се получи отделянето на електрон, който е въведен в атом в газовата фаза. Тази енергия обикновено се изразява в единици килоджаули на мол. Това е много важно в много области на химията, така че е интересно да се знае.
Затова ще посветим тази статия, за да ви разкажем за всички характеристики и значение на йонизационната енергия.
ключови характеристики
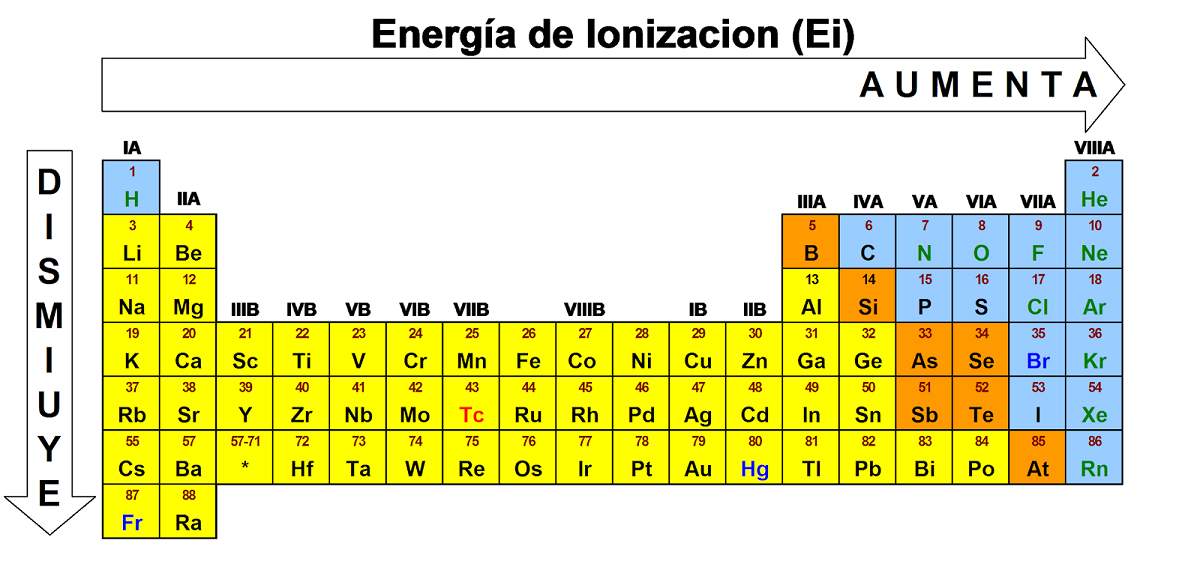
Когато говорим за енергията, необходима за изместване на електрон от атом на газова фаза Ние подчертаваме, че това газообразно състояние е състоянието, което е свободно от влиянието, което атомите могат да оказват върху себе си. Припомняме, че в материал, който е в газообразно състояние, е изключен всякакъв вид междумолекулно взаимодействие, тъй като атомите са разпръснати един от друг. Величината на йонизационната енергия е параметър, който служи за описване на силата, с която един електрон се свързва с атома, от който е част.
Ще има съединения, където електронът има по-висока йонизационна енергия и това ще означава, че той има по-висока сила на свързване към атома. Тоест, колкото по-голяма е йонизационната енергия, толкова по-сложно ще бъде откъсването на въпросния електрон.
Йонизационен енергиен потенциал
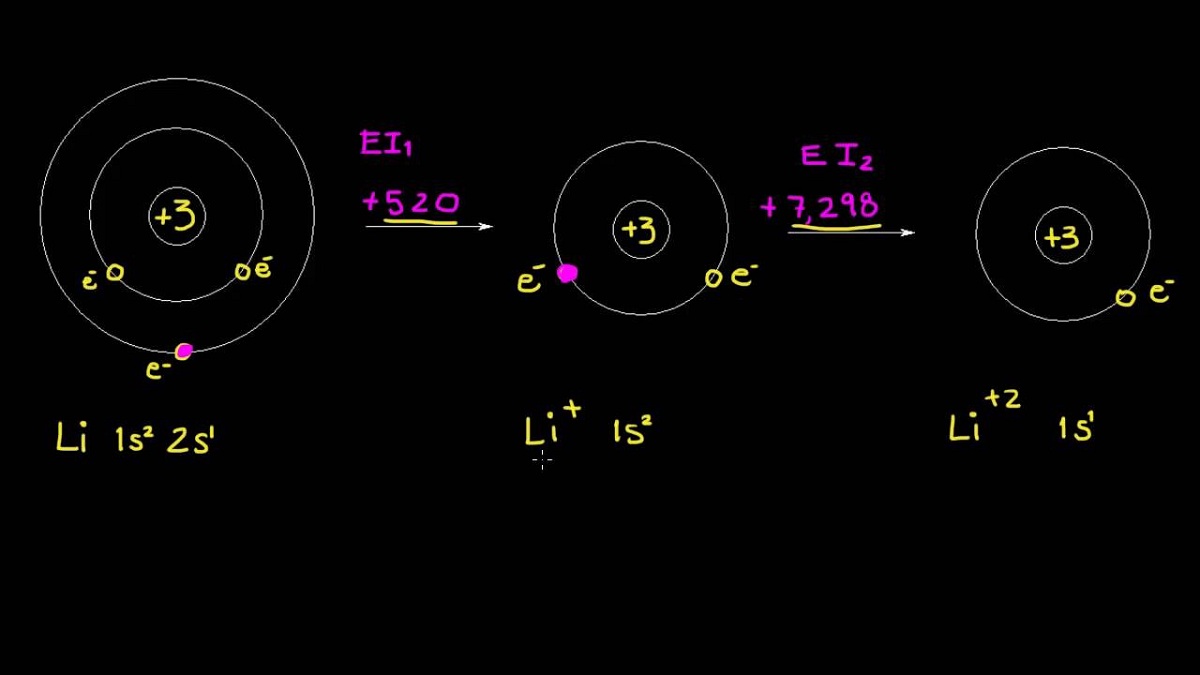
Когато започнем да изучаваме йонизационната енергия на дадено вещество, ние трябва да знаем неговия йонизационен потенциал. Трябва да се приложи само минималното количество енергия, за да се предизвика откъсването на електрон от най-външната обвивка на атома, което е в основното си състояние. Какво още, натоварването трябва да е неутрално. Трябва да се отбележи, че когато се говори за йонизационен потенциал, се използва термин, който се използва по-малко. Това е така, защото определянето на това свойство се основава на използването на електростатичен потенциал към изследваната проба.
Чрез използването на този електростатичен потенциал се случиха няколко неща: от една страна, йонизацията на химичните видове се случи поради електростатично действие. От друга страна, настъпи ускоряването на процеса на откъсване на електрона, който трябва да бъде отстранен. Тъй като спектроскопските техники започнаха да се използват за определяне на йонизационната енергия, името на потенциала започна да се променя на това на енергията. По същия начин е известно, че химичните свойства на атомите се определят от конфигурацията на електроните, намиращи се в най-външното енергийно ниво. На тези нива електроните са по-далеч от ядрото и могат да дадат повече информация.
Всичко това означава, че йонизационната енергия на тези видове, които имат електроните в най-външното енергийно ниво, е пряко свързана със стабилността на валентните електрони.
Методи за определяне на йонизационната енергия
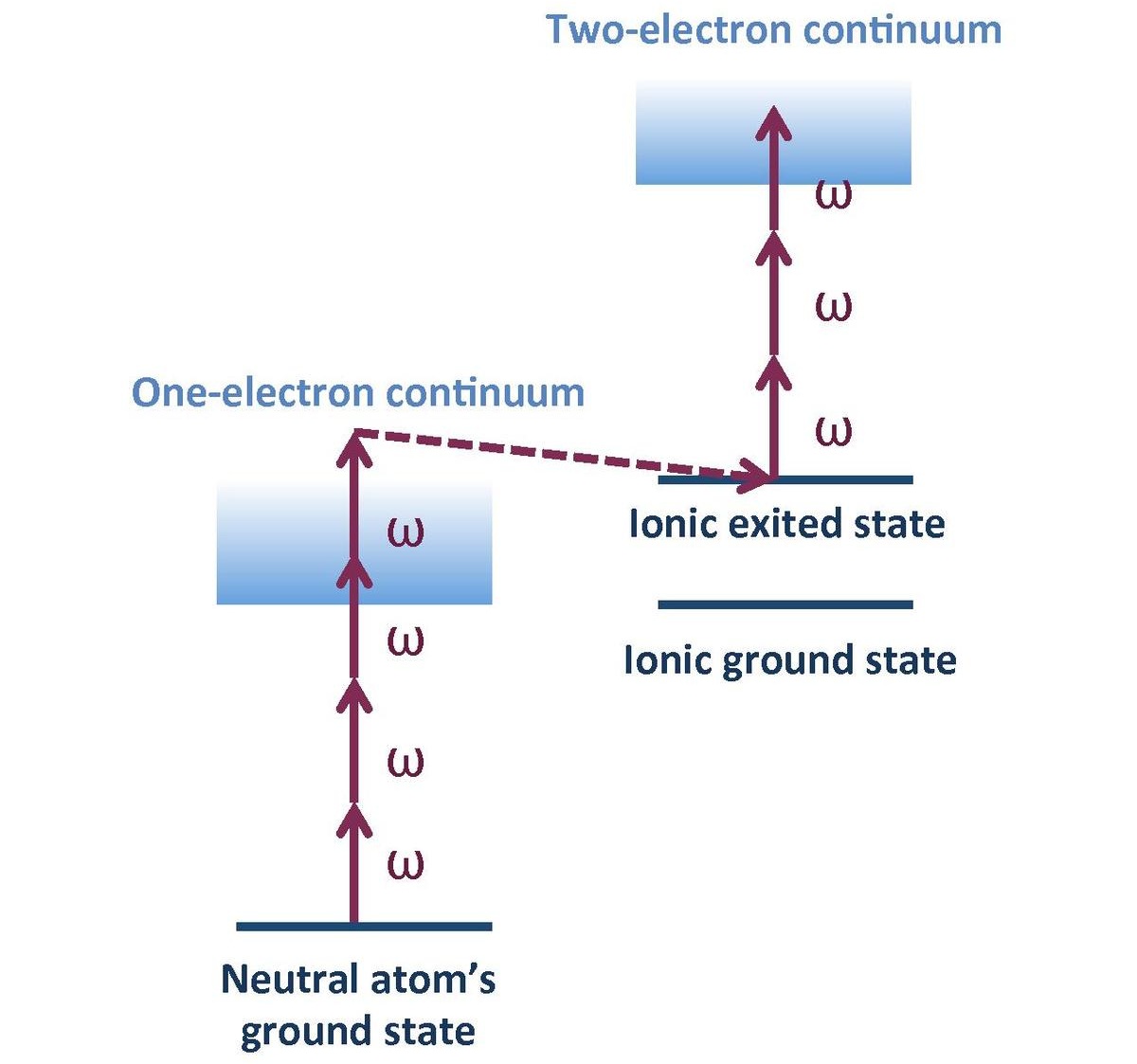
Съществуват множество методи за определяне на този вид енергия. Методите се дават главно чрез фотоемисионни процеси. Повечето от тези процеси се основават на определянето на енергията, излъчвана от електрони, като последица от прилагането на фотоелектричния ефект. Един от най-бързите методи за количествено определяне на йонизационната енергия е атомната спектроскопия. Съществува и друг интересен метод за изчисляване на този вид енергия, който е фотоелектронната спектроскопия. При този тип метод се измерват енергиите, с които електроните са свързани към атомите.
В тази връзка, Използва се метод, известен като ултравиолетова фотоелектронна спектроскопия, който има съкращението на английски UPS. Този метод се състои от техника, която използва възбуждането на атоми или молекули чрез прилагане на ултравиолетово лъчение. По този начин енергията, с която електроните на оптималното външно енергийно ниво са свързани към ядрото на атома, може да бъде по-добре измерена. Всичко това се прави, за да се анализират енергийните преходи на външните електрони на изследваните химични видове. Използва се и за изследване на характеристиките на връзките, които се образуват между тях.
Друг начин за познаване на йонизационната енергия е чрез метода на рентгеновите фотоелектронни копия, който използва същия принцип на възбуждане на електроните на най-външния слой и изследва разликите във вида на излъчването, което се влияе върху шоу , скоростта, с която се изхвърлят електроните и получената разделителна способност.
Първа и втора йонизационна енергия
В случай на атоми, които имат повече от един електрон на най-външното ниво, ние откриваме, че стойността на енергията, необходима за отстраняване на първия електрон от атома, се извършва чрез ендотермична химическа реакция. Атомите, които имат повече от един електрон, се наричат полиелектронни атоми.. Химичната реакция е ендотермична, тъй като спира да доставя енергия на атома, за да се получи електрон, добавен към катиона на този елемент. Тази стойност е известна като първата йонизационна енергия. Всички елементи, присъстващи в същия период, се увеличават пропорционално с увеличаването на атомния им брой.
Това означава, че те намаляват отдясно наляво в период и отгоре надолу в рамките на една и съща група, съществуваща в периодичната таблица. Ако следваме тази дефиниция, благородните газове имат високи величини в енергията си на йонизация. От друга страна елементите, които Те принадлежат към групата на алкални и алкалоземни метали и имат по-ниска стойност на тази енергия.
По същия начин, по който описахме първата енергия, чрез отстраняване на втори електрон от същия атом, се получава втората йонизационна енергия. За да се изчисли тази енергия, се поддържа същата схема и се отстраняват следните електрони. От тази информация се получава, че отделянето на електрона от атом в основно състояние намалява този отблъскващ ефект, който виждаме съществуващ сред останалите електрони. Това свойство е известно като ядрен заряд и остава постоянно. Необходимо е по-голямо количество енергия, за да се откъсне друг електрон от йонните видове, който има положителен заряд.
Надявам се, че с тази информация можете да научите повече за йонизационната енергия.