
المياه التي لها معايير وخصائص مختلفة أكثر أو أقل أهمية اعتمادًا على الاستخدام الذي يتم رفعه. من أهم المعلمات الكيميائية عند تصنيف جودتها هو عسر الماء. على الرغم من أن القانون لا يشترط أي حد لعسر الماء وقيمه في الاستهلاك البشري ، إلا أن هذه المرة بعض العلاقات غير المباشرة. من الممكن أن يكون الماء الذي يجب أن يكون لدينا صلابة عالية والعرف لا يثبت أي قيمة له.
لهذه الأسباب ، سنخصص هذه المقالة لنخبرك أن كل ما تحتاج لمعرفته حول عسر الماء هو أهميته.
ما هي عسر الماء

نظرًا لأن القانون لا يحد من عسر مياه الشرب ، فإن العلماء هم الذين يجب عليهم تقييم عواقب شرب المياه ذات الصلابة العالية. هذه المعلمة المياه له عواقب مختلفة في عدد كبير من العمليات اليومية كما يتم استخدامه للغسيل الشخصي أو الغسيل. من الخصائص التي يمكن من خلالها تصنيف جودة المياه هي صلابتها. إذا كنا سنستخدم المياه للري ، فقد رأيت بالتأكيد في مناسبات عديدة أن بعض النباتات تحتاج إلى عسر ماء معين.
تُعرَّف صلابة الماء بأنها التركيز الكلي لأيونات الكالسيوم والمغنيسيوم الموجودة فيه. هذه الأيونات هي الكاتيونات الحية وهي الأكثر شيوعًا في المياه الطبيعية. وهذا يعني أن صلابة الماء يمكن تعريفها على أنها مجموع كل الكاتيونات متعددة التكافؤ التي لديها، على الرغم من أن ملصق المغنيسيوم له أهمية أكبر بكثير في صلابة الماء العالمية.
غالبًا ما نجد أن عسر الماء يتم تحديده على أنه كتلة كربونات الكالسيوم ويتم قياسه بالملليغرام لكل لتر من المحلول. هذا لا يعني أن كل الكالسيوم الموجود في الماء العسر يأتي من كربونات الكالسيوم. ببساطة ، عادة ما يتم التعامل مع الاتفاقية كما لو كانت كذلك. من أجل حساب عسر الماء ، تُستخدم المعاملات فيما يتعلق بين كتلة الكالسيوم والمليجرام مع كتلة كربونات الكالسيوم. إذا قسمنا العلاقة بينهما على 10 ، فيمكننا الحصول على وحدة مستخدمة للغاية. هي الوحدة التي يتم فيها قياس عسر الماء. يطلق عليهم الدرجات المائية الفرنسية المعروفة باسم GHF أو ºfH. هناك أيضًا وحدات أخرى للإشارة إلى عسر الماء ولكنها أقل انتشارًا.
قيم عسر الماء
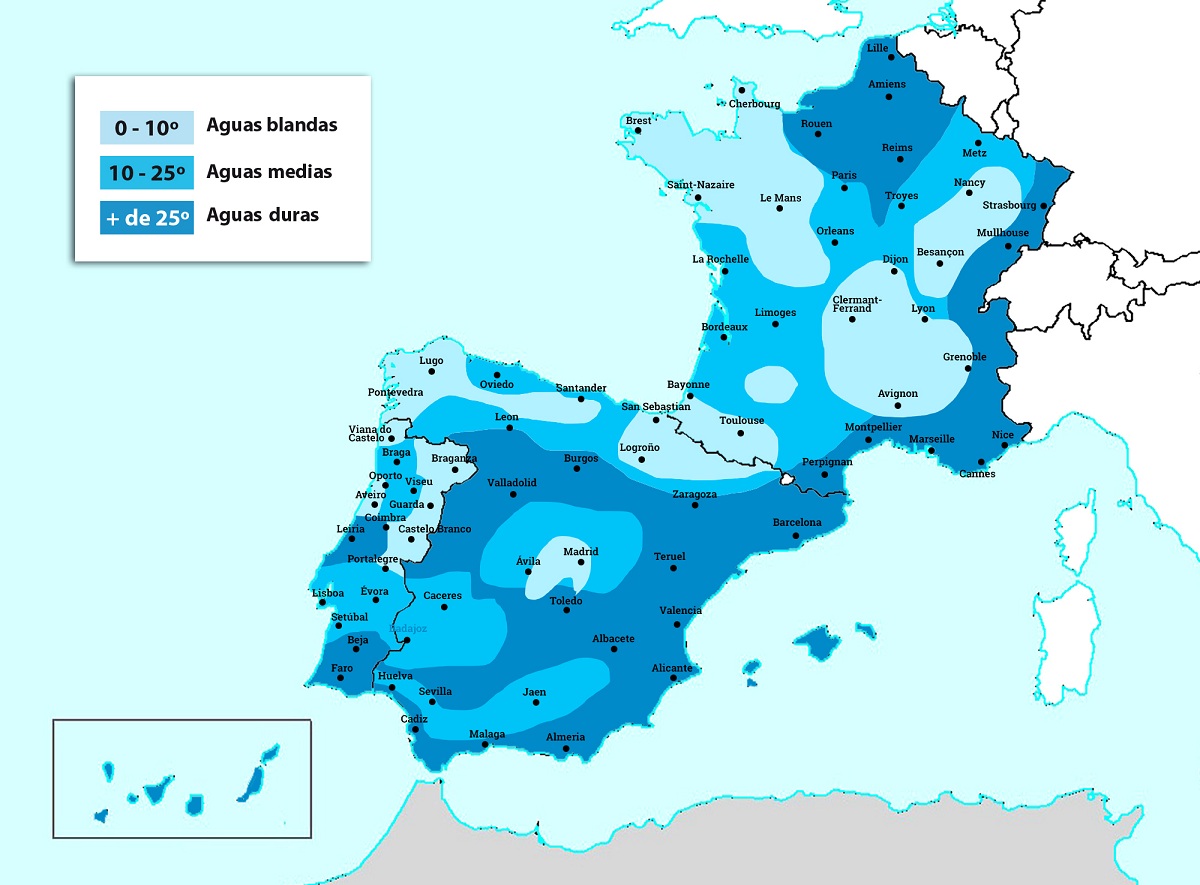
إذا كان الماء حلوًا جدًا أو شديد النعومة ، فستكون قيم عسره أقل من 7 درجة فهرنهايت. تشير هذه القيمة إلى أن لديهم تركيز 70 ملليغرام من كربونات الكالسيوم لكل لتر من الماء. من ناحية أخرى ، سيكون لدينا ماء عسر للغاية إذا كان يحتوي على كمية أكبر من 54ºfH أو ما كان عليه بتركيز 540 ملليجرام من كربونات الكالسيوم لكل لتر ماء.
إذا قمنا بتحليل المياه الإسبانية ، نرى أن هناك تنوعًا كبيرًا في الصلابة. في المياه التي يتم إدارتها والتي وجهتها الرئيسية هي الاستهلاك البشري ، نجد قدرًا كبيرًا من التنوع في الصلابة. على سبيل المثال ، بعض المقاطعات مثل سيغوفيا أو مدريد لديها قيم صلابة حولها 5ºfH ، بينما في أماكن أخرى مثل ألمرية يمكن أن تصل إلى 60. الشيء المهم هو معرفة الآثار السلبية التي يمكن أن تحدثها المياه العسرة على الجسم.
يعني وجود البيكربونات في الماء أن رواسب كربونات الكالسيوم يمكن أن تتشكل عند تسخينها. ينتج عن هذا تكوين قشور كلسية. بالتأكيد أنت تعرفه بالفعل بشكل شائع مثل الجير. في اللغة العامية ، يستخدم الجير للإشارة إلى هذه البقع البيضاء التي تتشكل بالقرب من الأحواض أو على شاشة الدش. لا يعني هذا الجير أنه يأتي مباشرة من إمدادات المياه ، بل هو تفاعل كيميائي يحدث بين الكالسيوم والصابون. لا يقتصر تأثير عسر الماء على مشاكل التنظيف فحسب ، بل ينتج عنه أيضًا رواسب صلبة في البيئات الصناعية يمكن أن تؤدي إلى مشاكل وتعطل في الغلايات وأبراج التبريد وغيرها من المعدات.
عادة ما تتم إزالة القشور الجيرية عن طريق التسبب في التفاعل الكيميائي العكسي للقشور السابقة. أي أنه يتشكل مرة أخرى في الكالسيوم القابل للذوبان وبيكربونات. يمكنك استخدام حمض ضعيف مثل حمض الخليك (يمكننا العثور عليه في الخل) أو حمض الستريك (يمكننا العثور عليه في عصير الليمون). لهذا السبب ، تعتمد معظم منتجات التنظيف المستخدمة للجير على منتج يحتوي على درجة حموضة حمضية قليلاً.
الآثار السلبية لعسر الماء وكيفية القضاء عليه
إذا ذهبنا إلى البيئة المنزلية ، نرى أن الماء العسر له آثار سلبية مثل تراكم الجلبة في الغلايات والكافيتريات وأنابيب المياه والسخانات. هذا يجعل من الضروري استخدام كمية أكبر من الصابون والمنظفات لإزالة هذه البقايا. إذا استخدمنا الصابون للتخلص من بقايا القناة ، يجب أن نعرف ذلك وهي عبارة عن كربوكسيلات فلزية قلوية مشتقة من الأحماض الدهنية. وذلك لأن الكالسيوم قادر على التفاعل مباشرة مع الصابون. يمكنك بسهولة رؤية التفاعل حيث تتشكل كتل غير قابلة للذوبان.
ما يساعد على تدمير خصائص الصابون هو قدرته على الرغوة. كلما زادت صعوبة الماء ، زادت كمية الشامبو أو الجل الذي نحتاجه للحصول على نفس الرغوة. مشكلة استخدام المزيد من المنظفات هي ارتفاع الإنفاق الاقتصادي وتلوث المياه. عيب آخر للمياه العسر هو أنك تحتاج أيضًا إلى المزيد من المنظفات لغسل ملابسك.
هناك عدة طرق مطلوبة لإزالة العسر الزائد من الماء. أبسط شيء هو تسخين الماء. لا يمكن التخلص من عسر الماء إلا بالتسخين إذا كانت تسمى الصلابة المؤقتة. الصلابة المؤقتة هي تلك التي تكون فيها كربونات الكالسيوم على شكل بيكربونات الكالسيوم. ومع ذلك ، فإن هذه الطريقة ليست جيدة حيث يتم تخزين الجير في الأنابيب وسخانات المياه. من الأفضل استخدام مواد كيميائية مختلفة لإزالة الترسبات. عادة ما تكون هذه هي كربونات المعدن القلوي الذي يساعد على إنتاج تفاعل كيميائي.
آمل أن تتمكن من خلال هذه المعلومات من معرفة المزيد عن عسر الماء.
