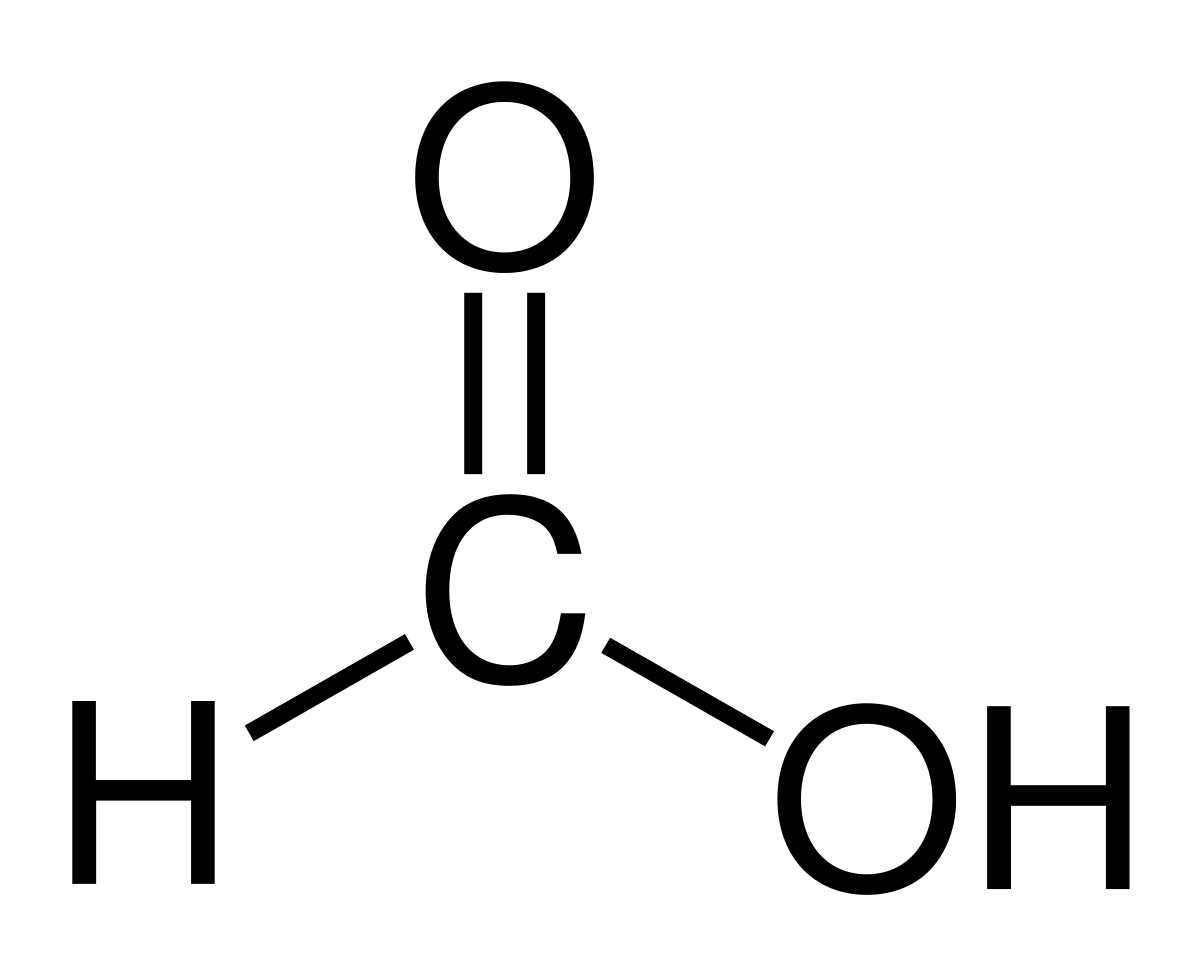
El axit formic o Axit metanoic là hợp chất đơn giản nhất và nhỏ nhất trong tất cả các axit hữu cơ. Nó có công thức phân tử HCOOH với chỉ một nguyên tử hydro liên kết với một nguyên tử cacbon. Tên của nó bắt nguồn từ chữ formica, có nghĩa là con kiến trong tiếng Latinh. Nó là một hợp chất khá quan trọng trong thế giới hóa học và được sử dụng rộng rãi ngày nay.
Vì lý do này, chúng tôi sẽ dành bài viết này để cho bạn biết mọi thứ bạn cần biết về axit formic, đặc điểm và tầm quan trọng của nó.
Các tính năng chính
Các nhà tự nhiên học thế kỷ XNUMX đã phát hiện ra rằng một số loại côn trùng (thuốc diệt mối), chẳng hạn như kiến, mối, ong và bọ cánh cứng, chúng tiết ra hợp chất này khiến vết cắn của chúng trở nên đau đớn. Ngoài ra, những loài côn trùng này sử dụng hợp chất này như một cơ chế tấn công, phòng thủ và phát tín hiệu hóa học.
Chúng có các tuyến độc giúp thải axit này và axit khác, chẳng hạn như axit axetic, ra khỏi cơ thể dưới dạng sương mù. Axit fomic mạnh hơn axit axetic (CH3COOH); do đó, một lượng bằng nhau của axit fomic hòa tan trong nước sẽ tạo ra dung dịch có độ pH thấp hơn.
Nhà tự nhiên học người Anh John Ray đạt được sự phân lập của hợp chất này vào năm 1671, chiết xuất từ một số lượng lớn kiến. Mặt khác, quá trình tổng hợp thành công đầu tiên của hợp chất này được thực hiện bởi nhà hóa học và vật lý người Pháp Joseph Gay-Lussac bằng cách sử dụng axit hydrocyanic (HCN) làm thuốc thử.
axit fomic trong tự nhiên

Axit fomic có thể tồn tại trên mặt đất, như một thành phần của sinh khối hoặc trong khí quyển, tham gia vào một loạt các phản ứng hóa học, thậm chí nó có thể được tìm thấy dưới lòng đất, trong dầu hoặc trong pha khí trên bề mặt của nó.
Về mặt sinh khối, côn trùng và thực vật là những nhà sản xuất chính của axit này. Khi đốt cháy nhiên liệu hóa thạch, chúng tạo ra axit formic ở thể khí; do đó, động cơ ô tô thải loại axit này vào khí quyển.
Tuy nhiên, có rất nhiều kiến sống trên trái đất, và sản lượng axit fomic giữa chúng lớn hơn hàng nghìn lần lượng axit methanoic do công nghiệp của con người tạo ra trong một năm. Cháy rừng cũng là một nguồn axit formic ở dạng khí.
Ở tầng cao hơn, trong ma trận phức tạp của khí quyển, các quá trình quang hóa để tổng hợp axit formic diễn ra. Lúc này, nhiều hợp chất hữu cơ dễ bay hơi (VOC) bị phân hủy dưới tác dụng của bức xạ UV hoặc bị oxy hóa theo cơ chế gốc OH. Hóa học khí quyển phong phú và phức tạp cho đến nay nguồn axit methanoic chính trên Trái đất.
Cấu trúc nguyên tử của axit fomic
Hình trên mô tả cấu trúc của chất dimer pha khí của axit fomic. Các quả cầu màu trắng tương ứng với nguyên tử hydro, quả cầu màu đỏ là nguyên tử oxy và quả cầu màu đen tương ứng với nguyên tử cacbon.
Có thể thấy hai nhóm trong các phân tử này: hydroxyl (-OH) và formyl (-CH = O), có khả năng tạo liên kết hydro. Những tương tác này thuộc loại OHO, trong đó nhóm hydroxyl là chất cho H và nhóm formyl là chất cho O.
Tuy nhiên, H liên kết với nguyên tử cacbon thiếu khả năng này. Các tương tác này rất mạnh, và hiđro trong nhóm OH có tính axit cao hơn do nguyên tử H thiếu điện tử; Vì vậy, hydro này tiếp tục ổn định cầu. Kết quả của những điều trên, axit fomic tồn tại dưới dạng chất lưỡng tính chứ không phải là một phân tử riêng lẻ.
Khi nhiệt độ giảm xuống, chất dimer định hướng các liên kết hydro của nó để tạo ra cấu trúc ổn định nhất với các chất dimer khác, dẫn đến chuỗi alpha và beta vô hạn của axit methanoic. Cấu trúc tinh thể này Nó phụ thuộc vào các biến vật lý tác động lên nó, chẳng hạn như áp suất và nhiệt độ.. Do đó, dây chuyền có thể chuyển đổi được. Nếu áp suất được tăng lên đến mức cực hạn, các chuỗi được nén đủ để được coi là một polyme kết tinh của axit fomic.
Tài sản
Chúng tôi sẽ tập trung vào việc mô tả các tính chất chính của axit fomic:
- axit methanoic là chất lỏng không màu ở nhiệt độ phòng, có mùi hăng nồng. Nó có trọng lượng phân tử là 46g / mol, nhiệt độ nóng chảy là 8,4ºC và nhiệt độ sôi là 100,8ºC, cao hơn so với nước.
- Có thể trộn lẫn với nước và các dung môi hữu cơ phân cực như ete, axeton, metanol và etanol.
- Ngược lại, trong các dung môi thơm như benzen và toluen, nó kém hòa tan vì axit fomic có ít nguyên tử cacbon trong cấu trúc của nó.
- Nó có pKa là 3,77, có tính axit mạnh hơn axit axetic, điều này có thể được giải thích là do nhóm metyl cung cấp mật độ điện tử cho nguyên tử cacbon bị oxy hóa bởi hai oxy. Điều này dẫn đến giảm nhẹ tính axit của các proton (CH3COOH, HCOOH).
- Một khi axit bị khử cacbon, được chuyển thành anion formate HCOO-, phân chia điện tích âm giữa hai nguyên tử oxy. Do đó, nó là một anion ổn định và là nguyên nhân tạo ra axit fomic cao.
Sử dụng axit formic
Ngành nông nghiệp và thực phẩm
Có hại như axit methanoic, nó được sử dụng với nồng độ vừa đủ làm chất bảo quản thực phẩm do tác dụng kháng khuẩn của nó. Vì lý do tương tự mà nó được sử dụng trong nông nghiệp, nó cũng có đặc tính diệt côn trùng. Nó cũng có tác dụng sát trùng cỏ và giúp ngăn ngừa khí đường ruột ở động vật trang trại.
Ngành dệt may và da giày
Nó được sử dụng trong ngành công nghiệp dệt để nhuộm và tinh chế hàng dệt và có lẽ là cách sử dụng axit này phổ biến nhất. Axit fomic được sử dụng để chế biến da và làm sạch vật liệu này bằng cách hành động tẩy dầu mỡ của nó. Sự thoái hóa axit fomic chuyển thành anion formate HCOO-, làm phân chia điện tích âm giữa hai nguyên tử oxy. Do đó, nó là một anion ổn định và là nguyên nhân tạo ra axit fomic cao.
An toàn đường bộ
Ngoài các mục đích sử dụng công nghiệp được chỉ định, các dẫn xuất axit formic (định dạng) được sử dụng trên các con đường mùa đông ở Thụy Sĩ và Áo để giảm nguy cơ tai nạn. Phương pháp điều trị này hiệu quả hơn so với sử dụng muối ăn.
Tôi hy vọng rằng với những thông tin này, bạn có thể hiểu thêm về axit formic, cấu trúc và công dụng của nó.