
În domeniul chimiei, energie de ionizare. Se referă la cantitatea minimă de energie necesară pentru a putea produce detașarea unui electron care a fost introdus într-un atom în faza gazoasă. Această energie este de obicei exprimată în unități de kilojuli pe mol. Este foarte important în multe domenii ale chimiei, deci este interesant de știut.
Prin urmare, vom dedica acest articol pentru a vă spune despre toate caracteristicile și importanța energiei de ionizare.
caracteristici cheie
Când ne referim energia necesară pentru a disloca un electron dintr-un atom de fază gazoasă Subliniem că această stare gazoasă este starea care este liberă de influența pe care atomii o pot exercita asupra lor. Amintim că într-un material care se află într-o stare gazoasă, este exclus orice tip de interacțiune intermoleculară, deoarece atomii sunt împrăștiați unul de celălalt. Mărimea energiei de ionizare este un parametru care servește la descrierea forței cu care se leagă un electron de atomul din care face parte.
Vor exista compuși în care are electronul o energie de ionizare mai mare și va însemna că are o rezistență mai mare a legăturii cu atomul. Adică, cu cât este mai mare energia de ionizare, cu atât va fi mai complicată detașarea electronului în cauză.
Potențial energetic de ionizare
Când începem să studiem energia de ionizare a unei substanțe, trebuie să cunoaștem potențialul său de ionizare. Nu este mai mult decât cantitatea minimă de energie care trebuie aplicată pentru a determina detașarea unui electron de învelișul exterior al atomului care se află în starea sa fundamentală. Mai mult, sarcina trebuie să fie neutră. Trebuie remarcat faptul că, atunci când vorbim despre potențialul de ionizare, se folosește un termen în care fiecare este folosit mai puțin. Acest lucru se datorează faptului că determinarea acestei proprietăți s-a bazat pe utilizarea unui potențial electrostatic la proba care urmează să fie studiată.
Prin utilizarea acestui potențial electrostatic s-au întâmplat mai multe lucruri: pe de o parte, ionizarea speciilor chimice a avut loc datorită acțiunii electrostatice. Pe de altă parte, s-a produs accelerarea procesului de detașare a electronului de îndepărtat. Pe măsură ce tehnicile spectroscopice au început să fie utilizate pentru a determina energia ionizării, numele potențialului a început să fie schimbat cu cel al energiei. De asemenea, se știe că proprietățile chimice ale atomilor sunt determinate de configurația electronilor prezenți la nivelul cel mai exterior al energiei. La aceste niveluri, electronii sunt mai departe de nucleu și pot oferi mai multe informații.
Toate acestea înseamnă că energia de ionizare a acestor specii care au electronii prezenți la nivelul energiei exterioare este direct legată de stabilitatea electronilor de valență.
Metode de determinare a energiei de ionizare
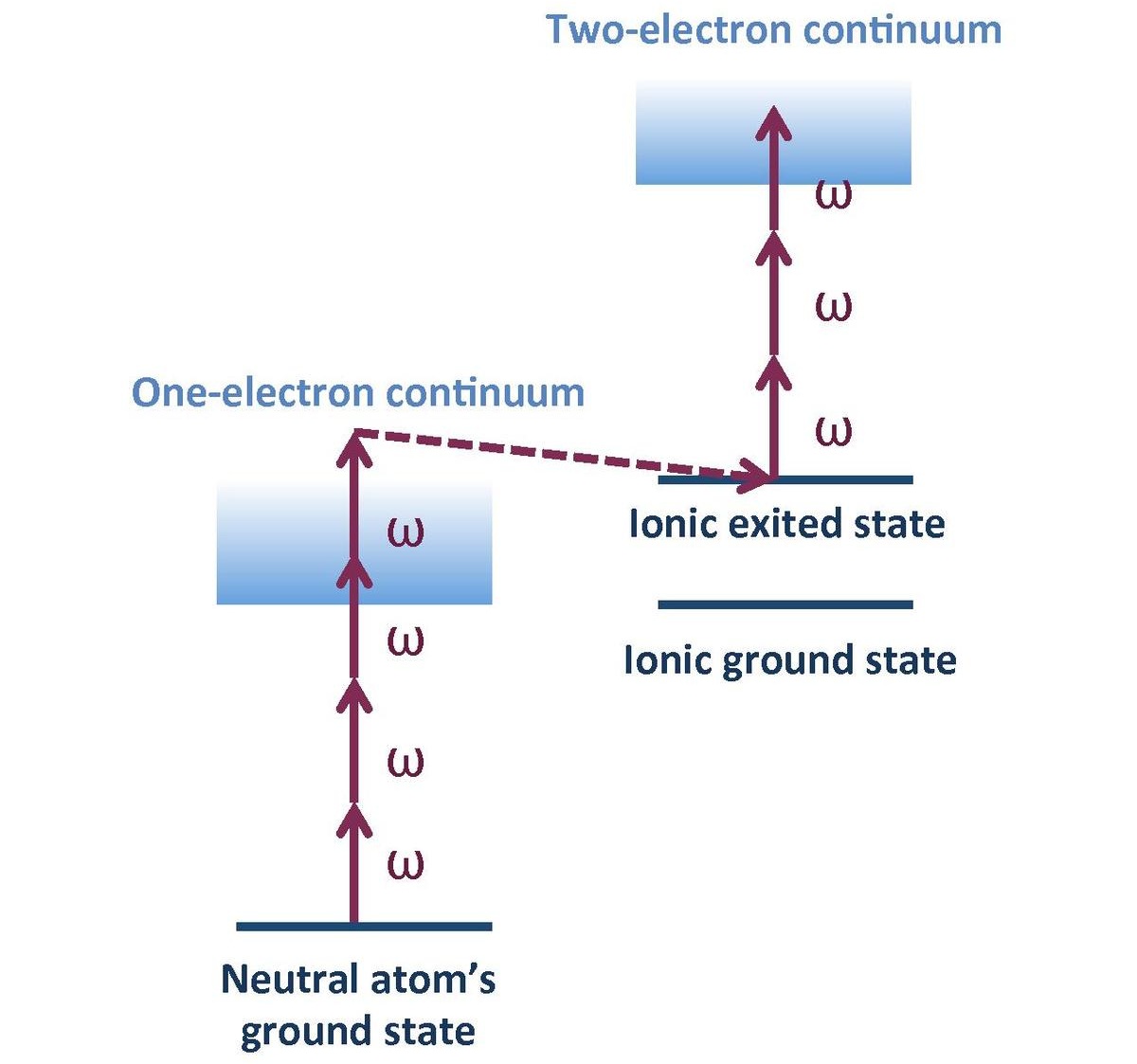
Există numeroase metode pentru a determina acest tip de energie. Metodele sunt date în principal prin procese de fotoemisiune. Majoritatea acestor procese se bazează pe determinarea energiei emise de electroni ca o consecință a aplicării efectului fotoelectric. Una dintre cele mai rapide metode de cuantificare a energiei de ionizare este spectroscopia atomică. Există, de asemenea, o altă metodă interesantă pentru a calcula acest tip de energie, care este spectroscopia fotoelectronică. În acest tip de metodă, se măsoară energiile cu care electronii sunt legați de atomi.
În acest sens, Se utilizează o metodă cunoscută sub numele de spectroscopie fotoelectronă ultravioletă, care are acronimul în limba engleză UPS. Această metodă constă într-o tehnică care utilizează excitația atomilor sau moleculelor prin aplicarea radiației ultraviolete. În acest fel, energia cu care electronii nivelului optim de energie externă sunt legați de nucleul atomului poate fi mai bine măsurată. Toate acestea se fac pentru a analiza tranzițiile energetice ale electronilor externi ai speciilor chimice studiate. De asemenea, este folosit pentru a studia caracteristicile legăturilor care se formează între ele.
O altă modalitate de cunoaștere a energiei de ionizare este prin intermediul metodei spectrului de copii fotoelectronice cu raze X. Folosește același principiu de excitație a electronilor stratului exterior și studiază diferențele în tipul de radiație care afectează spectacolele. , viteza cu care sunt expulzați electronii și rezoluția obținută.
Prima și a doua energie de ionizare
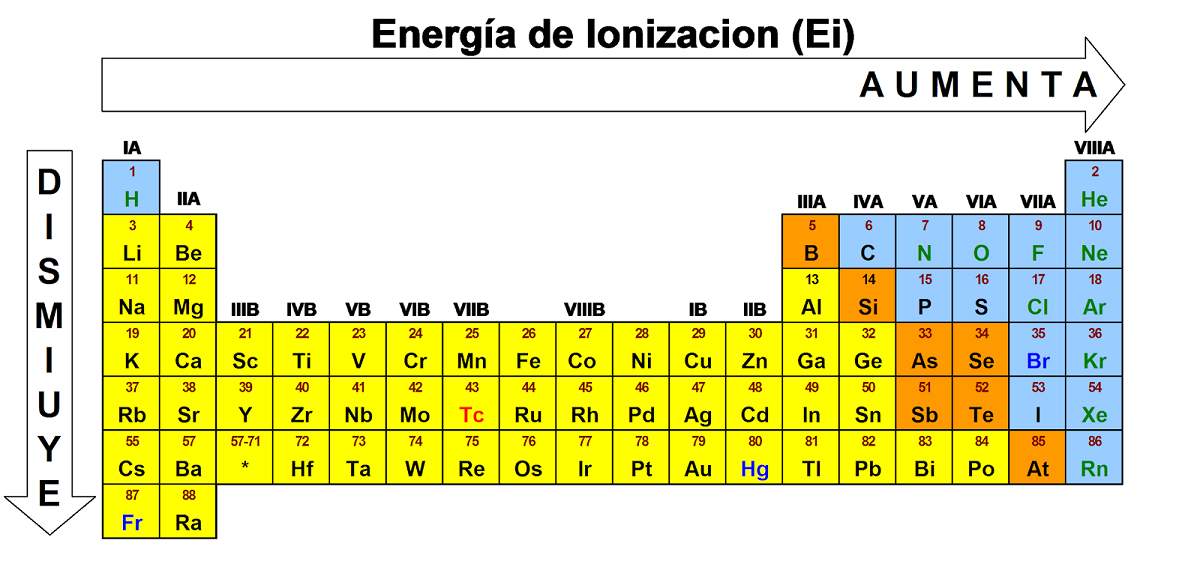
În cazul atomilor care au mai mult de un electron la nivelul cel mai exterior, constatăm că valoarea energiei necesare pentru îndepărtarea primului electron din atom se realizează printr-o reacție chimică endotermă. Atomii care au mai mult de un electron se numesc atomi polielectronici.. Reacția chimică este endotermă, întrucât încetează să mai furnizeze energie atomului pentru a putea obține un electron adăugat la cationul acestui element. Această valoare este cunoscută ca prima energie de ionizare. Toate elementele prezente în aceeași perioadă cresc proporțional cu creșterea numărului lor atomic.
Aceasta înseamnă că acestea scad de la dreapta la stânga într-o perioadă și de sus în jos în același grup existent în tabelul periodic. Dacă urmăm această definiție, gazele nobile au magnitudini mari în energiile lor de ionizare. Pe de altă parte, elementele care Acestea aparțin grupului de metale alcaline și alcalino-pământoase și au o valoare mai mică a acestei energii.
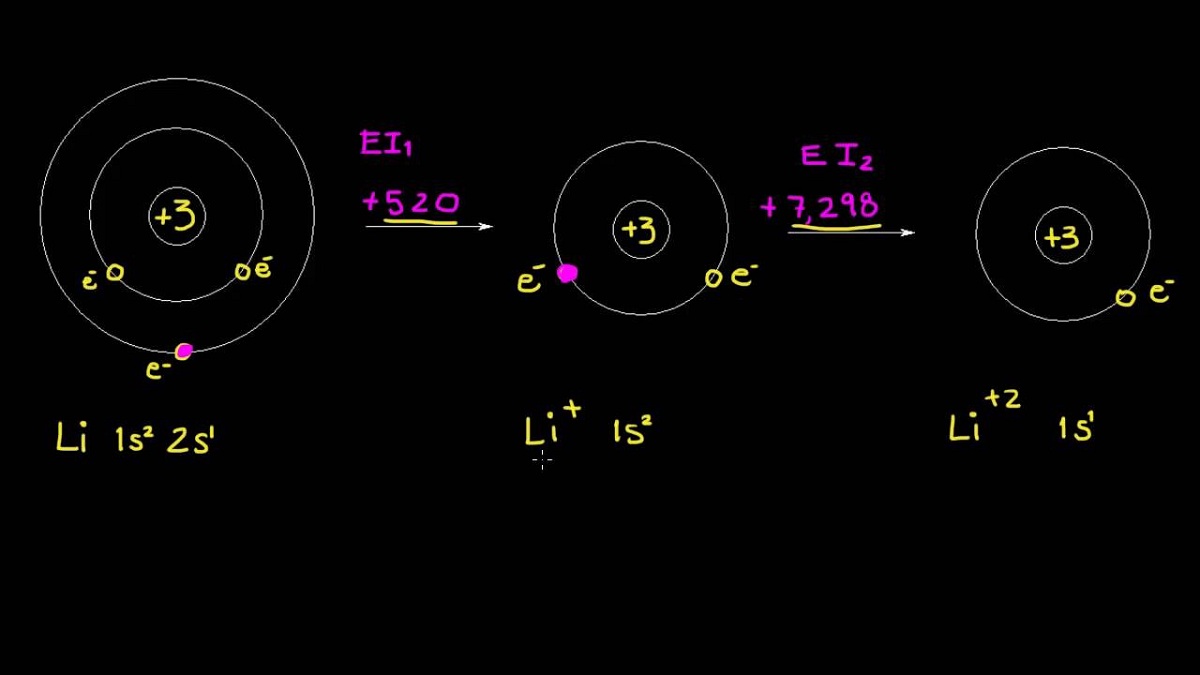
În același mod în care am descris prima energie, prin îndepărtarea unui al doilea electron din același atom, se obține a doua energie de ionizare. Pentru a calcula această energie, se menține aceeași schemă și se elimină următorii electroni. Din aceste informații se obține că detașarea electronului de un atom în starea sa fundamentală scade acest efect respingător pe care îl vedem existând printre electronii rămași. Această proprietate este cunoscută sub numele de încărcare nucleară și rămâne constantă. Este necesară o cantitate mai mare de energie pentru a rupe un alt electron al speciei ionice care are sarcina pozitivă.
Sper că cu aceste informații puteți afla mai multe despre energia de ionizare.