W dziedzinie chemii mamy do czynienia z reakcjami chemicznymi zachodzącymi między cząsteczkami i atomami. Dzisiaj porozmawiamy o hydroliza. Hydroliza to rodzaj reakcji chemicznej, która może zachodzić między nieorganicznymi i organicznymi cząsteczkami lub jonami. Główną cechą hydrolizy jest to, że obejmuje ona udział wody, dzięki czemu wiązania mogą zostać zerwane.
W tym artykule przedstawimy wszystkie cechy i znaczenie hydrolizy w chemii.
Co to jest hydroliza
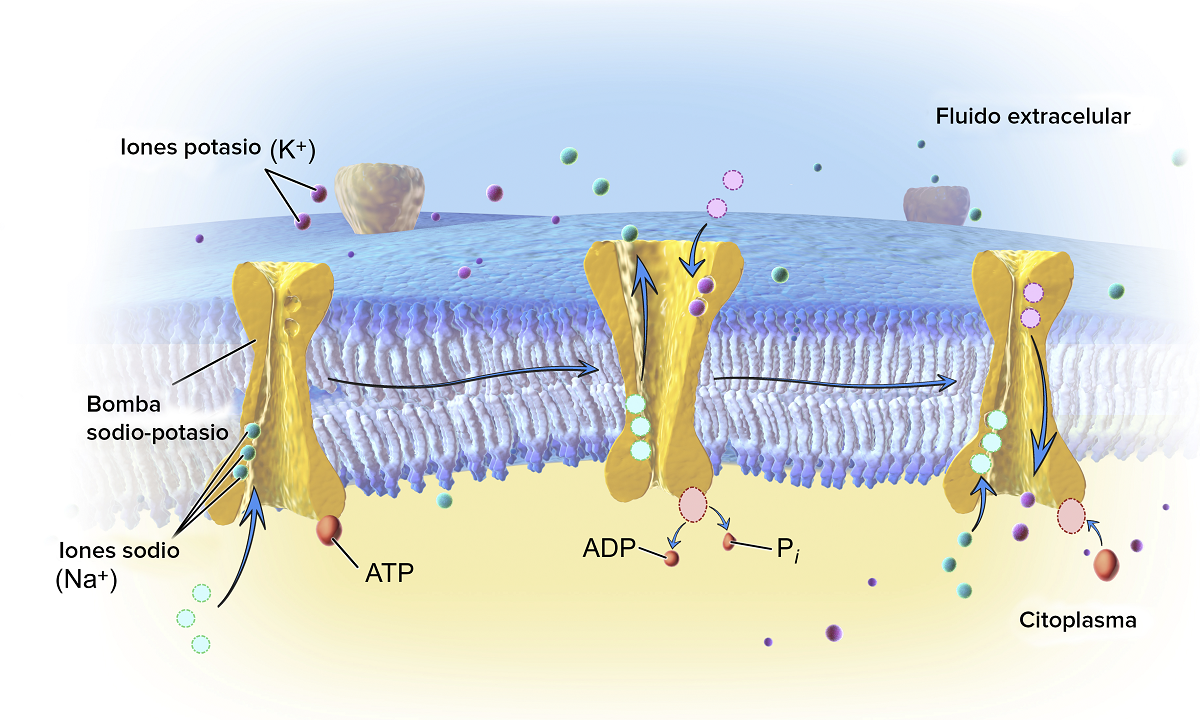
Mówimy o typie reakcji chemicznej, która może zachodzić między cząsteczkami organicznymi i nieorganicznymi. Podstawowym warunkiem jest to, że woda musi być zaangażowana, aby mogła zerwać wiązania tych cząsteczek. Słowo hydroliza pochodzi od greckiego hydro, co oznacza wodę i liza, co oznacza pęknięcie. W formie przetłumaczonej hydrolizę można by nazwać rozpadem wody. W tym przypadku mówimy o zerwaniu wiązań niektórych reagentów poprzez udział wody.
Cząsteczka wody składa się z dwóch atomów wodoru i jednego atomu tlenu. Dzięki tej kombinacji atomów powstaje równowaga między jonami soli słabych kwasów i zasad. Kwasy i zasady to pojęcia, które pojawiają się w ogólnych badaniach chemii i chemii analitycznej. Można powiedzieć, że hydroliza jest jedną z najprostszych reakcji chemicznych. Ogólne równanie hydrolizy jest następujące:
AB + H2O = AH + B-OH
Istnieje kilka przykładów hydrolizy, w których woda lub sama w sobie nie może zerwać pewnego wiązania kowalencyjnego. Pamiętamy, że wiązanie kowalencyjne to takie, w którym kilka cząsteczek o właściwościach niemetalicznych łączy się razem, tworząc kolejną nową cząsteczkę. Wiązanie, które je łączy, jest znane jako wiązanie kowalencyjne. Gdy sama woda nie jest w stanie zerwać tego wiązania, proces jest przyspieszany lub katalizowany przez zakwaszenie lub alkalizację ośrodka. Oznacza to, że w obecności jonów można katalizować hydrolizę. Chodzi o to, że istnieją enzymy zdolne do katalizowania chemicznej reakcji hydrolizy.
Główne cechy

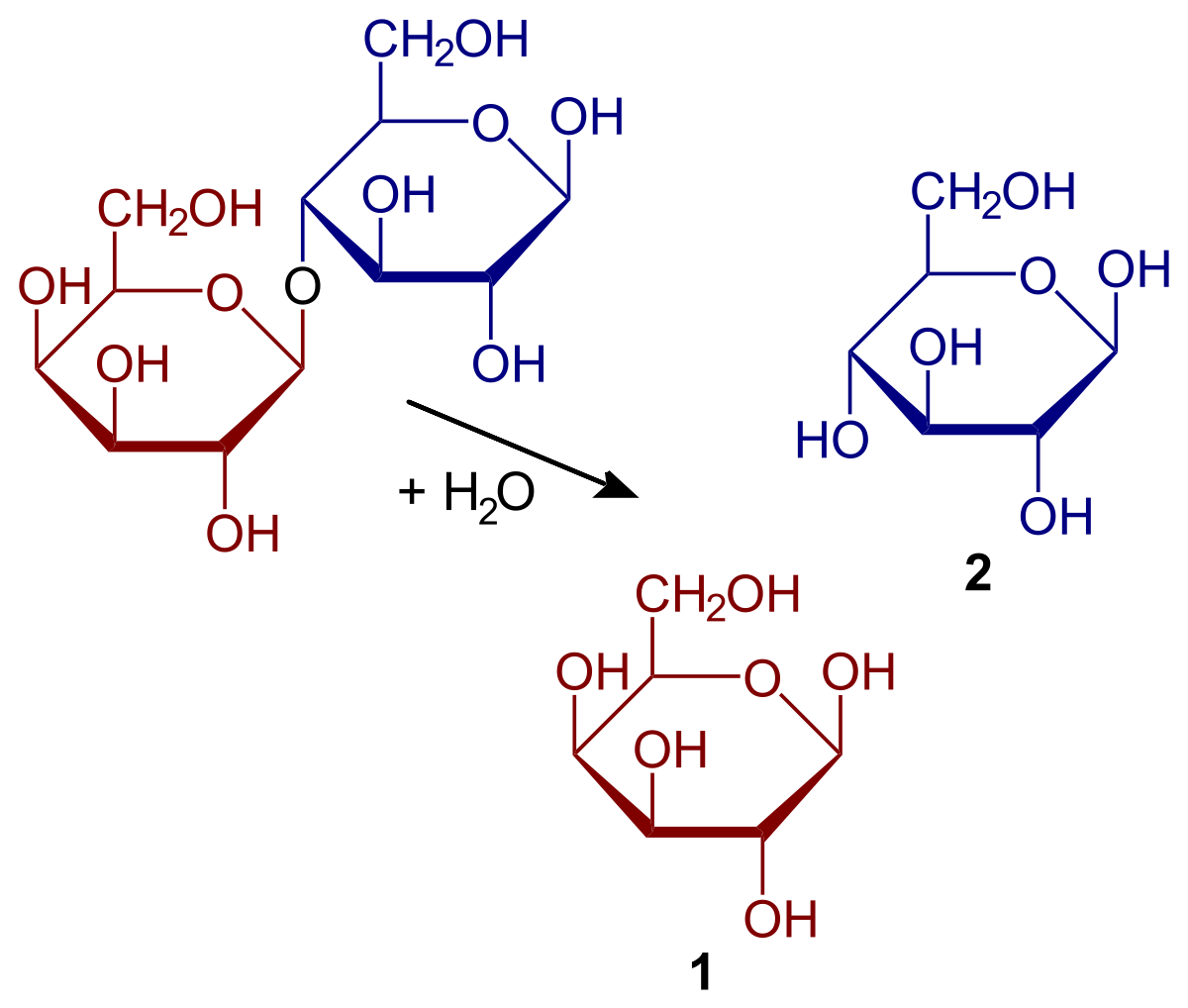
Zobaczmy, jakie są cechy i na czym polega hydroliza. Ten typ reakcji zajmuje szczególne miejsce, jeśli chodzi o biocząsteczki. I to dlatego, że wiązania, które utrzymują razem monomery cząsteczek, są podatne na hydrolizę w określonych warunkach. Oznacza to, że wiązania kowalencyjne, z którymi są połączone cząsteczki, mogą zostać zerwane w obecności wody. Przykładem tego są cukry. Cukry są zdolne do hydrolizy w celu rozbicia polisacharydów na monosacharydy. Dzieje się tak dzięki działaniu enzymów zwanych glukozydazami.
Należy wziąć pod uwagę, że to nie tylko cząsteczka jest substratem, który zrywa wiązanie. Sama woda również pęka i ostatecznie oddziela jony. Woda rozpada się na H + i OH–, gdzie H + kończy się na A, a OH– na B. W ten sposób AB reaguje z cząsteczką wody, tworząc dwa produkty, AH i B-OH.
Dlatego możemy powiedzieć, że hydroliza jest reakcją chemiczną przeciwną do kondensacji. Od kondensacji, dwa produkty łączą się, uwalniając małą cząsteczkę. Ta mała cząsteczka to woda. Wręcz przeciwnie, podczas hydrolizy cząsteczka jest zużywana, podczas gdy podczas kondensacji ta cząsteczka elektrolizy jest zużywana, uwalniana lub wytwarzana.
Aby ułatwić zrozumienie, ponownie wyjaśnimy przykład cukrów. Załóżmy, że AB jest dimerem sacharozy. W tym przypadku A oznacza glukozę, a B oznacza fruktozę. To wiązanie, które jest znane pod nazwą glikozydów, może być hydrolizowane, dając początek dwóm oddzielnym monosacharydom i roztworowi. To samo dzieje się z oligosacharydami i polisacharydami, jeśli enzymy są tymi, które działają w reakcjach.
Wiemy, że ta reakcja chemiczna ma tylko jeden kierunek. Oznacza to, że jest to rodzaj nieodwracalnej hydrolizy. Z drugiej strony istnieją reakcje hydrolizy, które są odwracalne po osiągnięciu równowagi.
Przykłady reakcji hydrolizy
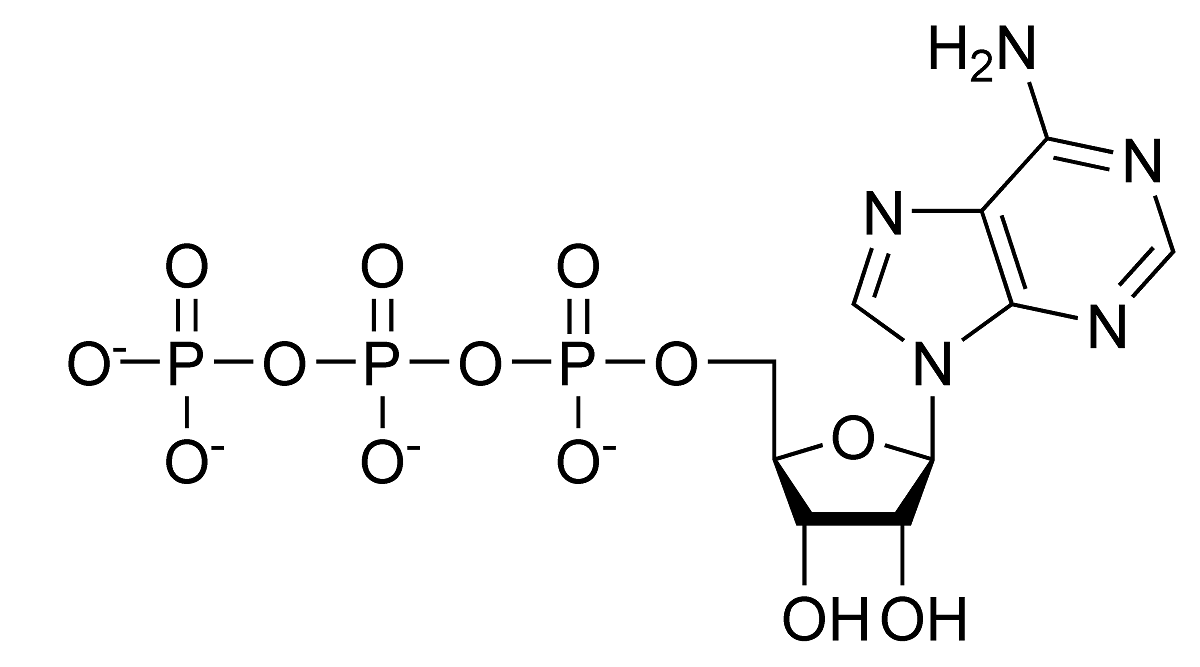
Zobaczmy, jakie są główne przykłady hydrolizy, które występują naturalnie. Przede wszystkim należy zobaczyć reakcję hydrolizy ATP. Wiemy, że ta cząsteczka ma stabilne wartości pH między 6.8 a 7.4. Jeśli jednak wartość pH wzrośnie i stanie się znacznie bardziej zasadowa, może ona samoistnie hydrolizować. U istot żywych hydroliza jest katalizowana przez enzymy znane pod nazwą ATPazy. Jest to rodzaj egzergonicznej reakcji chemicznej. Oznacza to, że entropia ADP jest większa niż ATP, więc zmiana energii swobodnej zachodzi w wyniku hydrolizy ATP. Ten rodzaj hydrolizy powoduje liczne reakcje endergiczne.
Reakcje sprzężone to inny rodzaj reakcji, w których zachodzi hydroliza. W niektórych przypadkach jest używany do konwersji związku A w związek B. Najbardziej znany przykład hydrolizy występuje naturalnie w wodzie. To tak, jakby jedna z cząsteczek wody mogła zostać rozbita na jony, a proton wodoru wiązał się z atomem tlenu drugiej cząsteczki wody. Daje to początek jonom hydroniowym. Można to określić nie tylko jako hydrolizę, jako autojonizację lub autoprotolizę wody.
Wreszcie kolejna z części, w której reakcje te są generowane w typowy sposób w białkach. Wiemy, że białka są stabilnymi cząsteczkami i do ich całkowitej hydrolizy wymagane są ekstremalne warunki. Pamiętamy, że białka składają się z aminokwasów. Jednak żywe istoty są wyposażone w arsenał enzymów, które umożliwiają hydrolizę białek do aminokwasów w dwunastnicy.
Mam nadzieję, że dzięki tym informacjom dowiesz się więcej o hydrolizie i jej właściwościach.