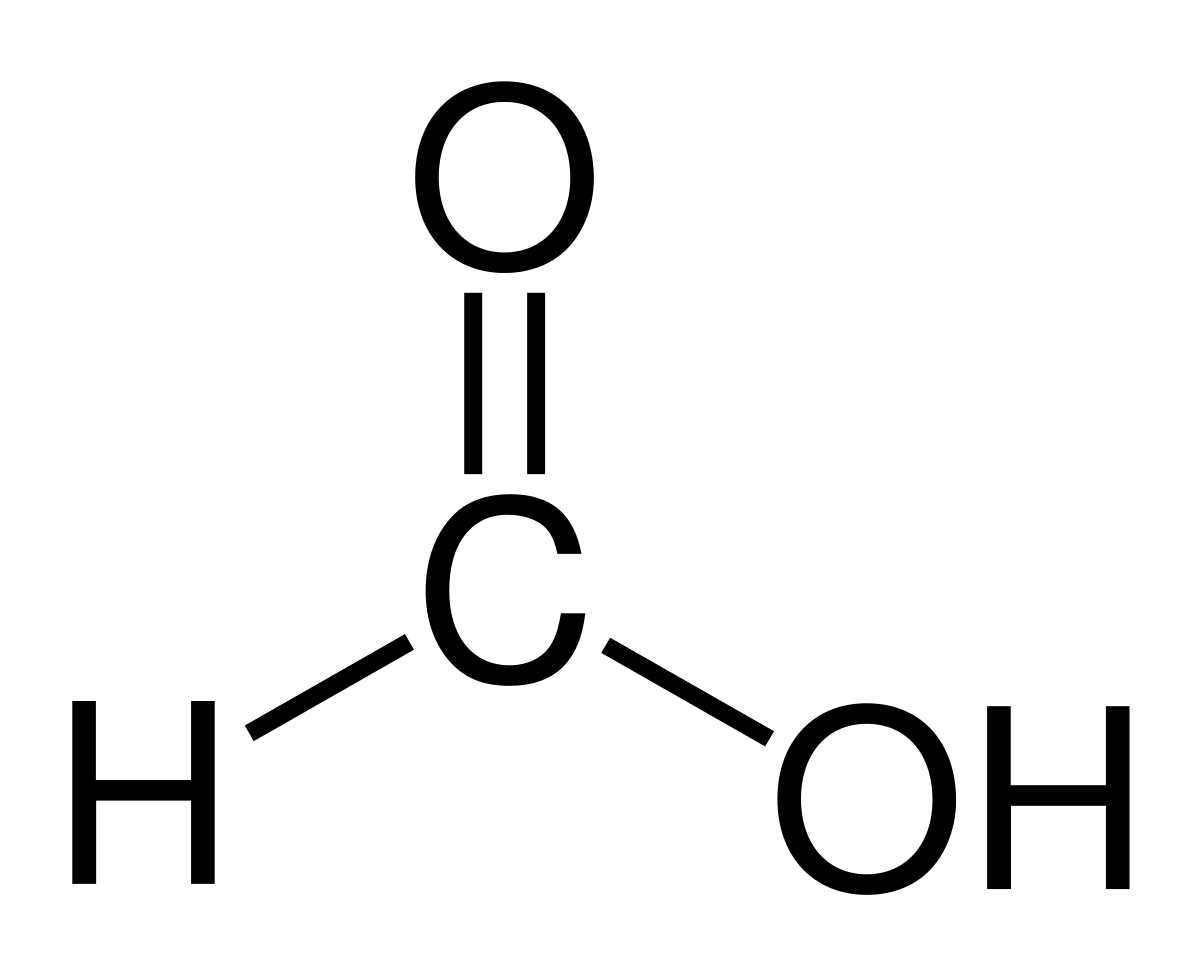
El mravlja kiselina o Metanska kiselina je najjednostavniji i najmanji spoj od svih organskih kiselina. Ima molekularnu formulu HCOOH sa samo jednim atomom vodika vezan za atom ugljika. Ime mu dolazi od riječi formica, što na latinskom znači mrav. To je prilično važan spoj u svijetu kemije i danas se široko koristi.
Iz tog razloga, ovaj ćemo članak posvetiti tome da vam ispričamo sve što trebate znati o mravljoj kiselini, njezinim karakteristikama i važnosti.
Glavne osobine
Prirodoslovci XNUMX. stoljeća otkrili su da određene vrste insekata (termicidi), kao npr mravi, termiti, pčele i kornjaši, luče ovaj spoj koji njihove ugrize čini bolnima. Osim toga, ovi insekti koriste ovaj spoj kao mehanizam napada, obrane i kemijske signalizacije.
Imaju otrovne žlijezde koje izbacuju ovu i druge kiseline, poput octene kiseline, iz tijela u obliku magle. Mravlja kiselina je jača od octene kiseline (CH3COOH); stoga će jednaka količina mravlje kiseline otopljene u vodi rezultirati otopinom s nižim pH.
engleski prirodoslovac John Ray postigao izolaciju ovog spoja 1671, izvađen iz velikog broja mrava. S druge strane, prvu uspješnu sintezu ovog spoja izveo je francuski kemičar i fizičar Joseph Gay-Lussac koristeći kao reagens cijanovodičnu kiselinu (HCN).
mravlje kiseline u prirodi

Mravlja kiselina može postojati na kopnenoj razini, kao komponenta biomase ili u atmosferi, sudjelujući u širokom rasponu kemijskih reakcija, čak se može naći i pod zemljom, u ulju ili u plinovitoj fazi na njezinoj površini.
U smislu biomase, kukci i biljke su glavni proizvođači ove kiseline. Kada fosilna goriva izgaraju, proizvode plinovitu mravlju kiselinu; stoga automobilski motori ovu kiselinu ispuštaju u atmosferu.
Međutim, na zemlji živi puno mrava, a proizvodnja mravlje kiseline između njih tisućama je puta veća od količine metanoične kiseline koju ljudska industrija proizvodi u jednoj godini. Šumski požari također su plinoviti izvor mravlje kiseline.
Gore, u složenom atmosferskom matriksu, odvijaju se fotokemijski procesi za sintezu mravlje kiseline. U ovom trenutku, mnogi hlapljivi organski spojevi (VOC) se razgrađuju pod djelovanjem UV zračenja ili se oksidiraju mehanizmom OH radikala. Bogata i složena atmosferska kemija je daleko glavni izvor metanoične kiseline na Zemlji.
Atomska struktura mravlje kiseline
Gornja slika prikazuje strukturu dimera plinovite faze mravlje kiseline. Bijele kuglice odgovaraju atomima vodika, crvene atomima kisika, a crne atomima ugljika.
U ovim molekulama se mogu vidjeti dvije skupine: hidroksil (-OH) i formil (-CH=O), koje su sposobne stvarati vodikove veze. Ove interakcije su tipa OHO, gdje je hidroksilna skupina H donor, a formilna skupina O donor.
Međutim, H vezan za atome ugljika nema tu sposobnost. Ove interakcije su vrlo jake, a vodik u OH skupini je kiseliji zbog H atoma s nedostatkom elektrona; Tako, ovaj vodik dodatno stabilizira most. Kao rezultat navedenog, mravlja kiselina postoji kao dimer, a ne kao pojedinačna molekula.
Kako temperatura pada, dimer usmjerava svoje vodikove veze kako bi stvorio najstabilniju strukturu s drugim dimerima, što rezultira beskonačnim alfa i beta lancima metanoične kiseline. Ova kristalna struktura Ovisi o fizičkim varijablama koje na njega djeluju, kao što su tlak i temperatura.. Stoga je lanac konvertibilan. Ako se tlak poveća do ekstremnih razina, lanci su dovoljno komprimirani da se smatraju kristalnim polimerom mravlje kiseline.
nekretnine
Usredotočit ćemo se na opisivanje glavnih svojstava mravlje kiseline:
- metanoična kiselina je bezbojna tekućina na sobnoj temperaturi jakog oštrog mirisa. Ima molekularnu težinu od 46 g/mol, talište od 8,4ºC i vrelište od 100,8ºC, više od vode.
- Može se miješati s vodom i polarnim organskim otapalima kao što su eter, aceton, metanol i etanol.
- Nasuprot tome, u aromatičnim otapalima kao što su benzen i toluen, slabo je topiv jer mravlja kiselina u svojoj strukturi ima malo atoma ugljika.
- Ima pKa od 3,77, koja je kiselija od octene kiseline, što se može objasniti jer metilna skupina daje elektronsku gustoću ugljikovom atomu oksidiranom s dva kisika. To rezultira blagim smanjenjem kiselosti protona (CH3COOH, HCOOH).
- Nakon što je kiselina deprotonirana, pretvara se u formatni anion HCOO-, koji delokalizira negativni naboj između dva atoma kisika. Stoga je stabilan anion i odgovoran je za visoku kiselost mravlje kiseline.
Upotreba mravlje kiseline
Prehrambena i poljoprivredna industrija
Štetna kao metanoična kiselina, koristi se u dovoljnim koncentracijama kao konzervans za hranu zbog svog antibakterijskog učinka. Iz istog razloga zbog kojeg se koristi u poljoprivredi, ima i insekticidna svojstva. Također ima antiseptički učinak na trave i pomaže u sprječavanju crijevnih plinova kod domaćih životinja.
Industrija tekstila i obuće
Koristi se u tekstilnoj industriji za bojanje i rafiniranje tekstila i vjerojatno je najčešća upotreba ove kiseline. Mravlja kiselina se koristi za obradu kože i depilaciju ovog materijala njegovo odmašćivanje. Deprotonacija mravlje kiseline pretvara se u formatni anion HCOO-, koji delokalizira negativni naboj između dva atoma kisika. Stoga je stabilan anion i odgovoran je za visoku kiselost mravlje kiseline.
Sigurnost ceste
Uz navedene industrijske namjene, derivati mravlje kiseline (format) koriste se na zimskim cestama u Švicarskoj i Austriji kako bi se smanjio rizik od nesreća. Ovaj tretman je učinkovitiji od upotrebe kuhinjske soli.
Nadam se da uz ove informacije možete saznati više o mravljoj kiselini, njezinoj strukturi i uporabi.