Wasser ist ein Element, das wir leben müssen und damit es Leben auf der Erde gibt, wie wir es heute kennen. Das Wassermolekül Es besteht aus zwei Wasserstoffatomen und einem Sauerstoffatom, die durch eine kovalente Bindung verbunden sind. Dies bedeutet, dass die beiden Wasserstoffatome und das Sauerstoffatom vereint sind, da sie Elektronen untereinander teilen. Die Formel für das Wassermolekül lautet H2O. Es gibt viele Eigenschaften, die das Wassermolekül hat, und dank ihm gibt es zahlreiche Prozesse, die zur Entwicklung des Lebens führen.
Aus diesem Grund widmen wir Ihnen in diesem Artikel alles, was Sie über das Wassermolekül wissen müssen.
Analyse des Wassermoleküls
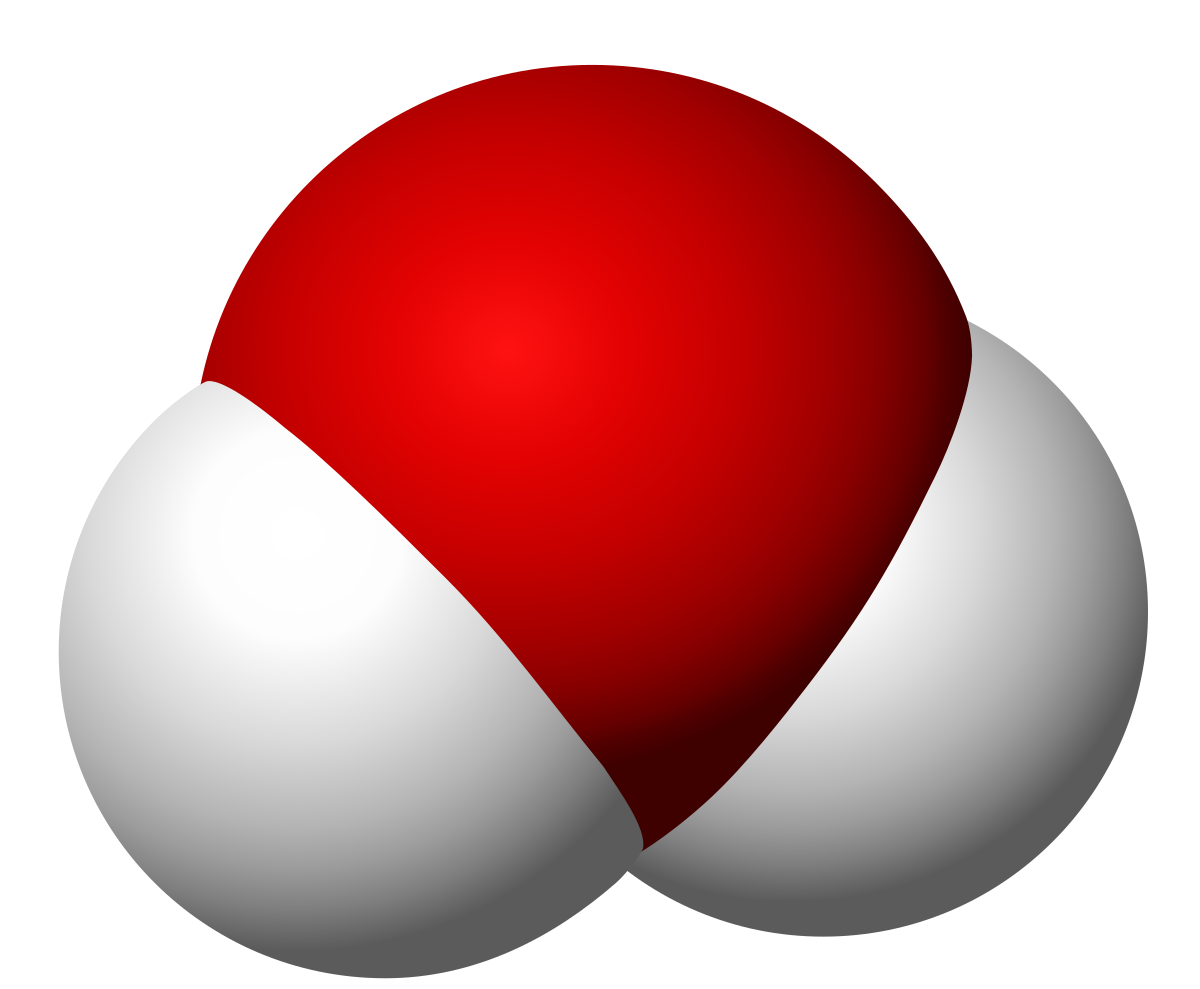
Wenn wir dieses Molekül analysieren, können wir sehen, dass der Bindungswinkel der kovalenten Bindung zwischen Wasserstoff und Sauerstoff bei 104.5 Grad beginnt. Dies kann durch spektroskopische und Röntgenanalyse erreicht werden. Der durchschnittliche Abstand zwischen Wasserstoff- und Sauerstoffatomen beträgt von 96.5 Uhr oder, was auch immer, 9.65 • 10-8 Millimeter.
Diese Entfernungen können nicht mit allem verglichen werden, was das menschliche Auge sehen kann. Die Anordnung der Elektronen im Wassermolekül kommuniziert die elektrische Asymmetrie, da zwischen Wasserstoff und Sauerstoff ein unterschiedliches Maß an Elektronegativität besteht. Wir nennen Elektronegativität zu die Fähigkeit eines Atoms, Elektronen anzuziehen, die in einer kovalenten Bindung geteilt werden. Wir erinnern uns, dass eine kovalente Bindung zwischen zwei nichtmetallischen Atomen hergestellt wird.
Da Sauerstoff mehr Elektronegativität als Wasserstoff aufweist, sind die Elektronen eher näher am Sauerstoffatom als am Wasserstoffatom. Dies liegt daran, dass Elektronen negativ geladen sind. Die Tatsache, dass die Elektronen hauptsächlich zu den Sauerstoffatomen gelangen, bewirkt, dass das Wasserstoffatom eine gewisse positive Ladung aufweist. Diese Ladung wird als positive Teilladung bezeichnet. Das von Sauerstoff wird die negative Teilladung genannt.
Der Unterschied zwischen positiven und negativen Elektronen, die nahe an beiden Atomen liegen, macht das Wassermolekül zu einem polaren Molekül. Das heißt, das Molekül hat einen Teil mit einem negativen Pol und einen anderen Teil mit einem positiven Pol. Obwohl das gesamte Molekül neutral ist, leiten sich aus diesem polaren Charakter alle seine physikochemischen und biologischen Eigenschaften ab.
Wechselwirkungen zwischen Molekülen
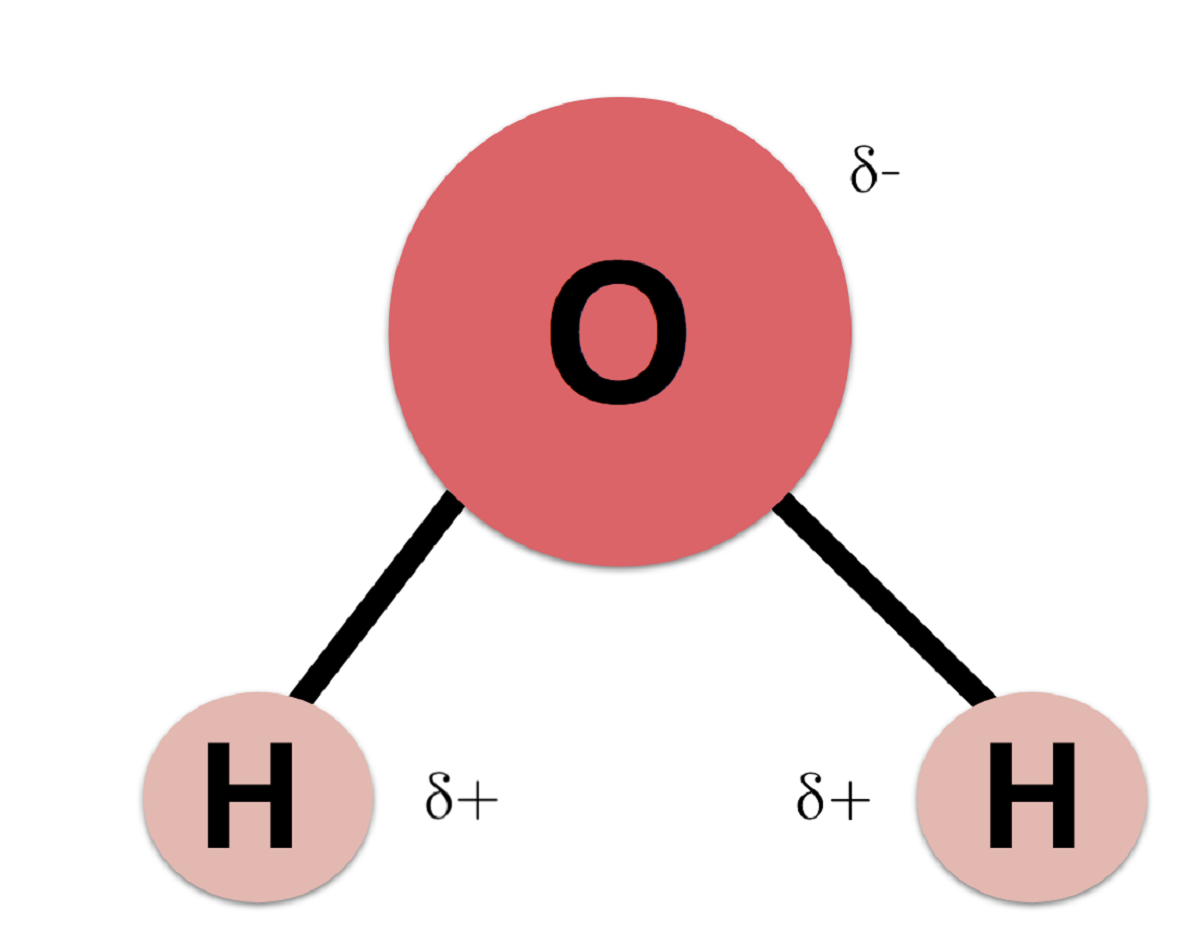
Wenn mehrere Wassermoleküle sehr nahe beieinander liegen, können sie getrennt eine Traktion zwischen den Sauerstoffatomen der Moleküle herstellen. Dies liegt daran, dass Sauerstoff eine negative Teilladung hat und einer der Wasserstoffatome eine positive Teilladung hat. Daher wird der positive Teil eines Wassermoleküls vom negativen Teil des anderen Wassermoleküls angezogen. Diese Art der Wechselwirkung zwischen Molekülen wird als Wasserstoffquelle bezeichnet. In diesen Molekülen passiert viel, da sie so geordnet sind, dass Jedes Wassermolekül kann sich mit 4 weiteren Molekülen verbinden. Diese Art der Wechselwirkung tritt mit Eis auf.
Die Bindungen zwischen den Wasserstoffatomen finden dank der Tatsache statt, dass es ein Atom mit einer negativen Teilladung und einen Wasserstoff mit einer positiven Teilladung gibt. Dies macht die Verbindungen nicht nur zum Wasser. Diese Wechselwirkungsbindungen treten auch in Stickstoff, Fluor und Wasserstoff in anderen Molekülen auf, die Proteine und DNA enthalten.
Mal sehen, was die physikochemischen Eigenschaften des Wassermoleküls sind. Unter diesen Eigenschaften und Merkmalen können wir die Kapazität und das Lösungsmittel hervorheben. Wir dürfen nicht vergessen, dass Wasser als universelles Lösungsmittel gilt. Ein weiteres Merkmal des Wassermoleküls ist seine hohe spezifische Wärme und seine Verdampfungswärme. Es hat auch eine hohe Kohäsion und Adhäsion, eine abnormale Dichte und fungiert als chemisches Reagenz.
Wenn wir die Eigenschaften von Wasser nutzen, sehen wir, dass es aufgrund seines polaren Charakters eine große Anzahl von Verbindungen in ihm dispergieren kann. Wie wir bereits erwähnt haben, ist das gesamte Molekül zwar neutral, aber die Tatsache, dass es einen positiven und einen negativen Teil hat, ist das, was Es gibt die physikochemischen Eigenschaften an, für die Wasser für das Leben so notwendig ist. So arbeitet es mit Salzen und anderen ionischen Substanzen, in denen das Wassermolekül seine Pole ausrichtet. Diese Ausrichtung der Pole ist als Funktion der Ladungen zweier Ionen gegeben, wobei der negative Pol auf der einen Seite und der positive Pol auf der anderen Seite angeordnet sind. Beispielsweise wirkt Wasser bei polaren Substanzen wie Ethanol auf ähnliche Weise. Es stellt einen Pol gegen einen anderen mit dem entgegengesetzten Vorzeichen der Substanz.
Eigenschaften des Wassermoleküls
Das Wassermolekül hat eine hohe spezifische Wärme. Diese spezifische Wärme ist nichts anderes als die Wärmemenge, die verabreicht werden muss ein Gramm Wasser, um seine Temperatur um ein Grad erhöhen zu können. Andererseits haben wir die Verdampfungswärme. Dies ist die Dampfmenge, die auf ein Gramm Flüssigkeit aufgebracht werden muss, damit sie auf ein Gramm Dampf übergehen kann. Wir wissen, dass das Wassermolekül dank der Brücken, die die Wasserstoffatome verbinden, eine hohe spezifische Wärme und Verdampfung aufweist. Das heißt, um die Wassertemperatur um ein Grad zu erhöhen, müssen alle Moleküle ihre Schwingung erhöhen. Dazu brechen sie die Wasserstoffbrückenbindungen auf, so dass sie ein Gramm flüssiges Wasser an ein Gramm Dampfwasser weitergeben können.
Die Tatsache, dass es einen hohen Wert an Verdampfungswärme hat, ist darauf zurückzuführen, dass es passieren kann. Ein weiteres Merkmal des Wassermoleküls ist die Kohäsion. Die Frage ist die Tendenz, dass zwei Moleküle vereint werden müssen. Auch dank der Wasserstoffbrücken des Wassermoleküls ist die Kohäsion hoch. Beitritt ist die Tendenz zweier verschiedener Moleküle, sich miteinander zu verbinden. Dadurch haftet das Wassermolekül stark an ionischen und polaren Verbindungen. Dies ist die Anwendung, die stattfindet, wenn Wasser an verschiedenen Oberflächen haftet.
Ich hoffe, dass Sie mit diesen Informationen mehr über das Wassermolekül erfahren können.