Inden for kemi har vi de kemiske reaktioner, der forekommer mellem molekyler og atomer. I dag skal vi tale om hydrolyse. Hydrolyse er en type kemisk reaktion, der kan forekomme mellem uorganiske og organiske molekyler eller ioner. Det vigtigste kendetegn ved hydrolyse er, at det involverer vanddeltagelse, så bindingerne kan brydes.
I denne artikel vil vi fortælle dig om alle egenskaber og vigtigheden af hydrolyse inden for kemi.
Hvad er hydrolyse
Vi taler om en type kemisk reaktion, der kan forekomme mellem både organiske og uorganiske molekyler. Den væsentlige betingelse er, at vand skal være involveret, så det kan bryde bindingerne af disse molekyler. Ordet hydrolyse kommer fra græsk hydro, som betyder vand og fra lysis, hvilket betyder brud. Oversat i form kunne hydrolyse være kendt som nedbrydning af vand. I dette tilfælde taler vi om at bryde båndene til nogle reaktanter gennem vandets deltagelse.
Vandmolekylet består af to brintatomer og et iltatomer. Takket være denne kombination af atomer dannes en ligevægt mellem ionerne af salte af svage syrer og baser. Syrer og baser er begreber, der vises i generelle studier af kemi og analytisk kemi. Hydrolyse kan siges at være en af de enkleste kemiske reaktioner derude. Den generelle ligning for en hydrolyse er som følger:
AB + H2O = AH + B-OH
Der er flere eksempler på hydrolyse, hvor vand eller i sig selv ikke kan bryde en bestemt kovalent binding. Vi husker, at en kovalent binding er en, hvori adskillige molekyler med ikke-metalliske egenskaber går sammen om at danne et nyt nyt molekyle. Bindingen, der forbinder dem, er kendt som en kovalent binding. Når vand alene ikke er i stand til at bryde denne binding, accelereres eller katalyseres processen ved forsuring eller alkalisering af mediet. I nærvær af ioner kan hydrolyse katalyseres. Og det er, at der er enzymer, der er i stand til at katalysere den kemiske reaktion ved hydrolyse.
Vigtigste funktioner

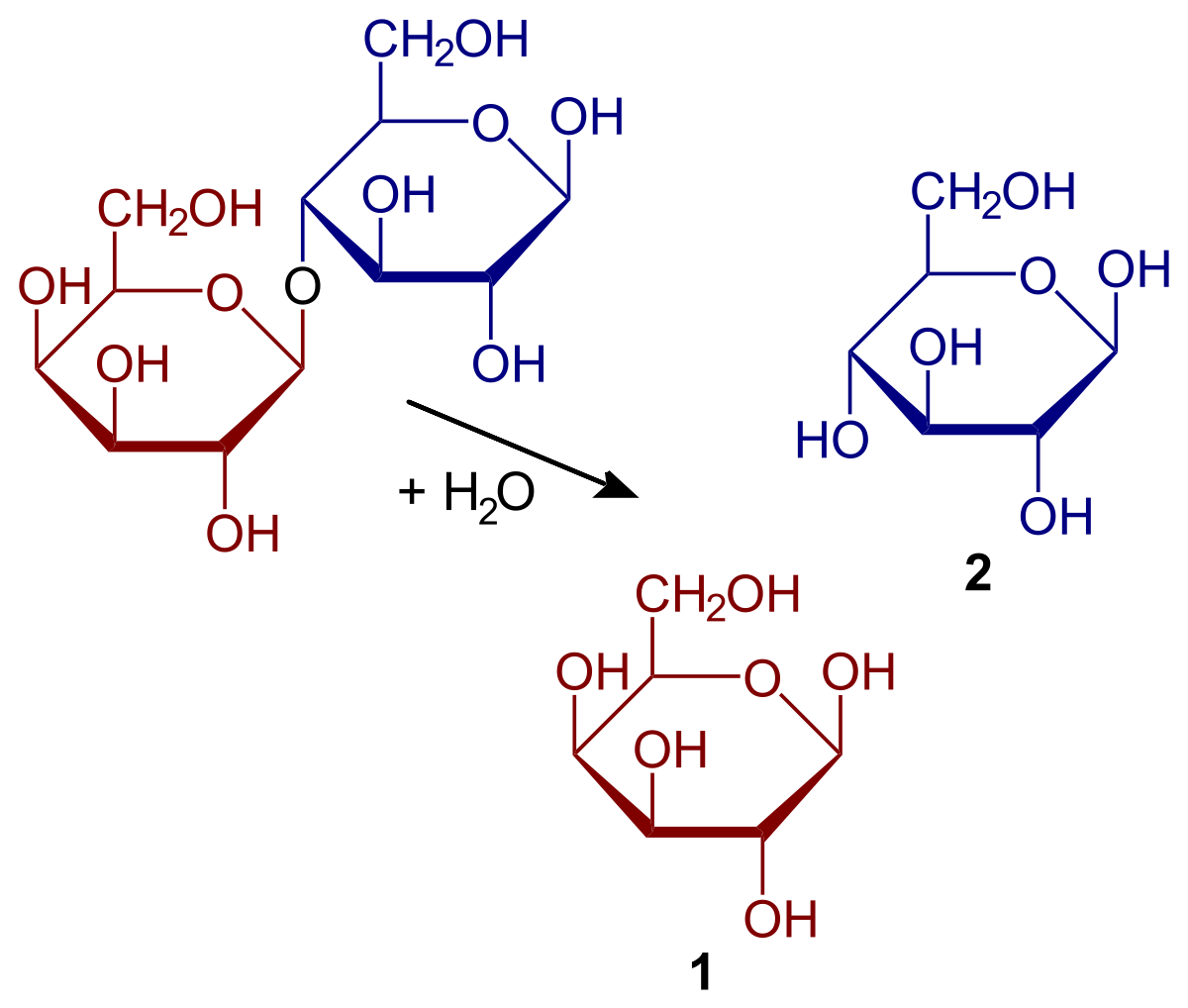
Lad os se, hvad karakteristika er, og hvad hydrolyse består af. Denne type reaktion indtager et særligt sted, når det kommer til biomolekyler. Og det er, at bindingerne, der holder molekylernes monomerer sammen, er modtagelige for hydrolysering under visse betingelser. Det vil sige, de kovalente bindinger, som molekylerne er bundet til, kan brydes i nærværelse af vand. Et eksempel på dette er sukker. Sukker er i stand til at hydrolysere for at nedbryde polysaccharider til monosaccharider. Dette sker takket være virkningen af enzymer kendt som glucosidaser.
Det skal tages i betragtning, at det ikke kun er molekylet et substrat, der bryder bindingen. Selve vandet bryder også og adskiller til sidst ionerne. Vand brister i H + og OH–, hvor H + slutter med A, og OH– med B. AB reagerer således med et vandmolekyle, hvilket giver anledning til to produkter, AH og B-OH.
Derfor kan vi sige, at hydrolyse er en kemisk reaktion i modstrid med kondens. Fra kondens, to produkter slutter sig ved at frigive et lille molekyle. Dette lille molekyle er vand. Tværtimod forbruges, ved hydrolyse, et molekyle, mens dette i kondensation forbruges, frigives eller produceres af dette elektrolysemolekyle.
For at gøre det meget lettere at forstå, vil vi forklare eksemplet på sukker igen. Lad os antage, at AB er en saccharose-dimer. I dette tilfælde repræsenterer A glucose og B repræsenterer fruktose. Denne binding i, som er kendt under det glykosidiske navn, kan hydrolyseres for at give anledning til to separate monosaccharider og opløsningen. Det samme sker med oligosaccharider og polysaccharider, hvis enzymerne er dem, der virker i reaktionerne.
Vi ved, at denne kemiske reaktion kun har én retning. Dette betyder, at det er en type irreversibel hydrolyse. På den anden side er der hydrolysereaktioner, der er reversible, når ligevægt er nået.
Eksempler på hydrolysereaktioner
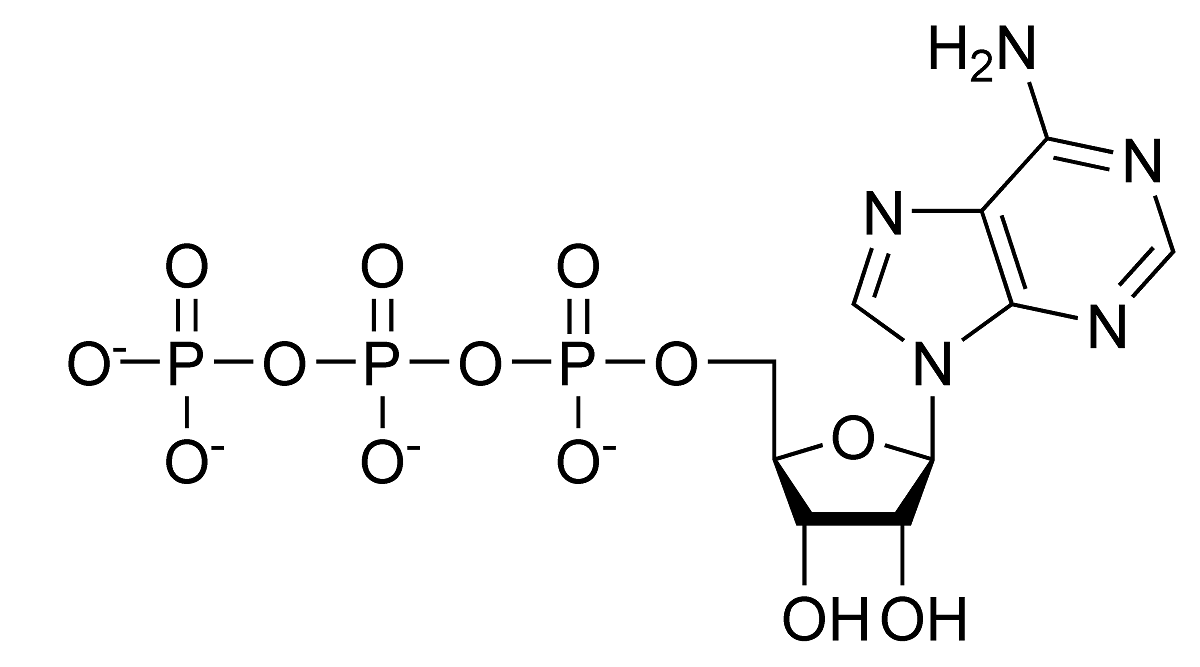
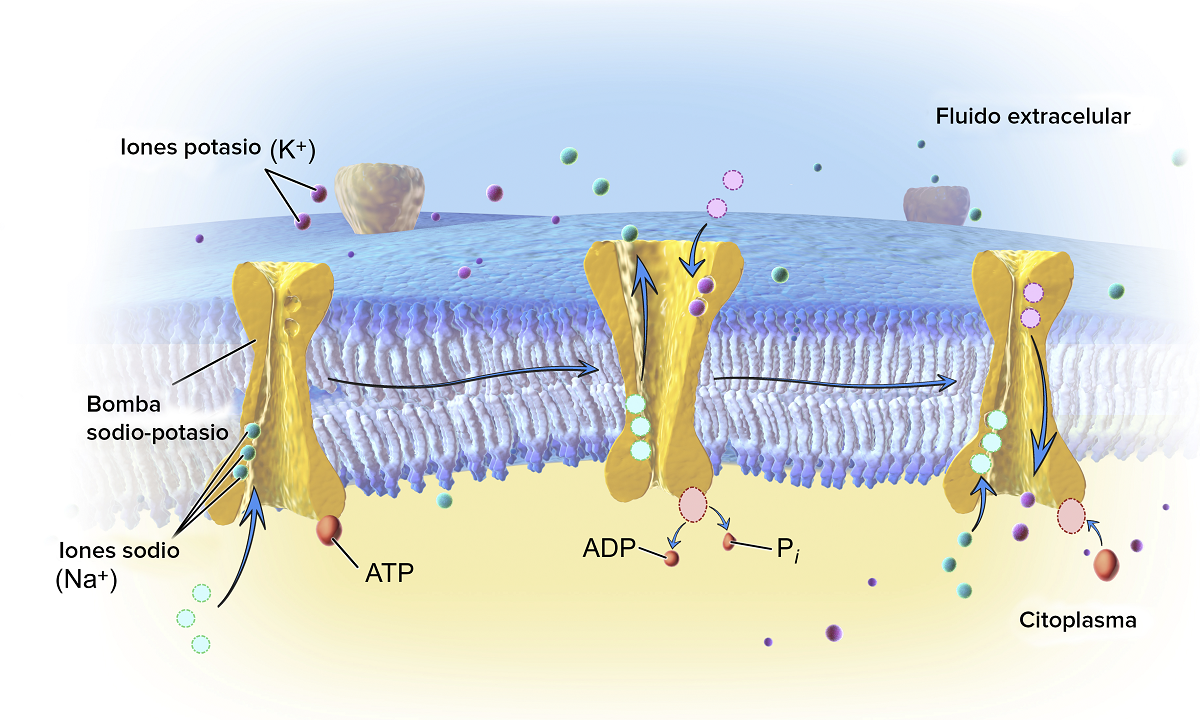
Lad os se, hvad der er de vigtigste eksempler på hydrolyse, der forekommer naturligt. Først og fremmest er at se hydrolysereaktionen af ATP. Vi ved, at dette molekyle har stabile pH-værdier mellem 6.8 og 7.4. Men hvis pH-værdierne stiger til at blive meget mere basiske, kan det hydrolysere spontant. Hos levende væsener katalyseres hydrolyse af enzymer kendt under navnet ATPases. Det er en type exergonisk kemisk reaktion. Dette betyder, at entropien af ADP er større end ATP, så den frie energivariation opstår ved hydrolyse af ATP. Denne type hydrolyse anvender adskillige endergoniske reaktioner.
Koblede reaktioner er en anden type reaktion, hvor der forekommer hydrolyse. I nogle tilfælde anvendes det til omdannelse af en forbindelse A til en forbindelse B. Det mest kendte eksempel på hydrolyse forekommer naturligt i vand. Det er som om et af vandmolekylerne kunne brydes i ioner, og hydrogenprotonen binder til iltatomet i det andet vandmolekyle. Dette giver anledning til hydroniumionen. Det kan betegnes mere end en hydrolyse som en autoionisering eller autoprotolyse af vand.
Endelig en anden af de dele, hvor disse reaktioner genereres på en almindelig måde i proteiner. Vi ved, at proteiner er stabile molekyler, og for at opnå deres fuldstændige hydrolyse kræves ekstreme forhold. Vi husker, at proteiner består af aminosyrer. Imidlertid er levende væsener udstyret med et arsenal af enzymer, der tillader hydrolyse af proteiner til aminosyrer i tolvfingertarmen.
Jeg håber, at du med disse oplysninger kan lære mere om hydrolyse og dens egenskaber.