Voda je živel, který potřebujeme k životu ak životu na Zemi, jak jej známe dnes. The molekula vody Skládá se ze dvou atomů vodíku a jednoho atomu kyslíku spojených kovalentní vazbou. To znamená, že dva atomy vodíku a atom kyslíku jsou spojeny díky tomu, že mezi sebou sdílejí elektrony. Vzorec molekuly vody je H2O. Molekula vody má mnoho vlastností a díky ní existuje řada procesů, které vedou k rozvoji života.
Proto se budeme věnovat tomuto článku, abychom vám řekli vše, co potřebujete vědět o molekule vody.
Analýza molekuly vody
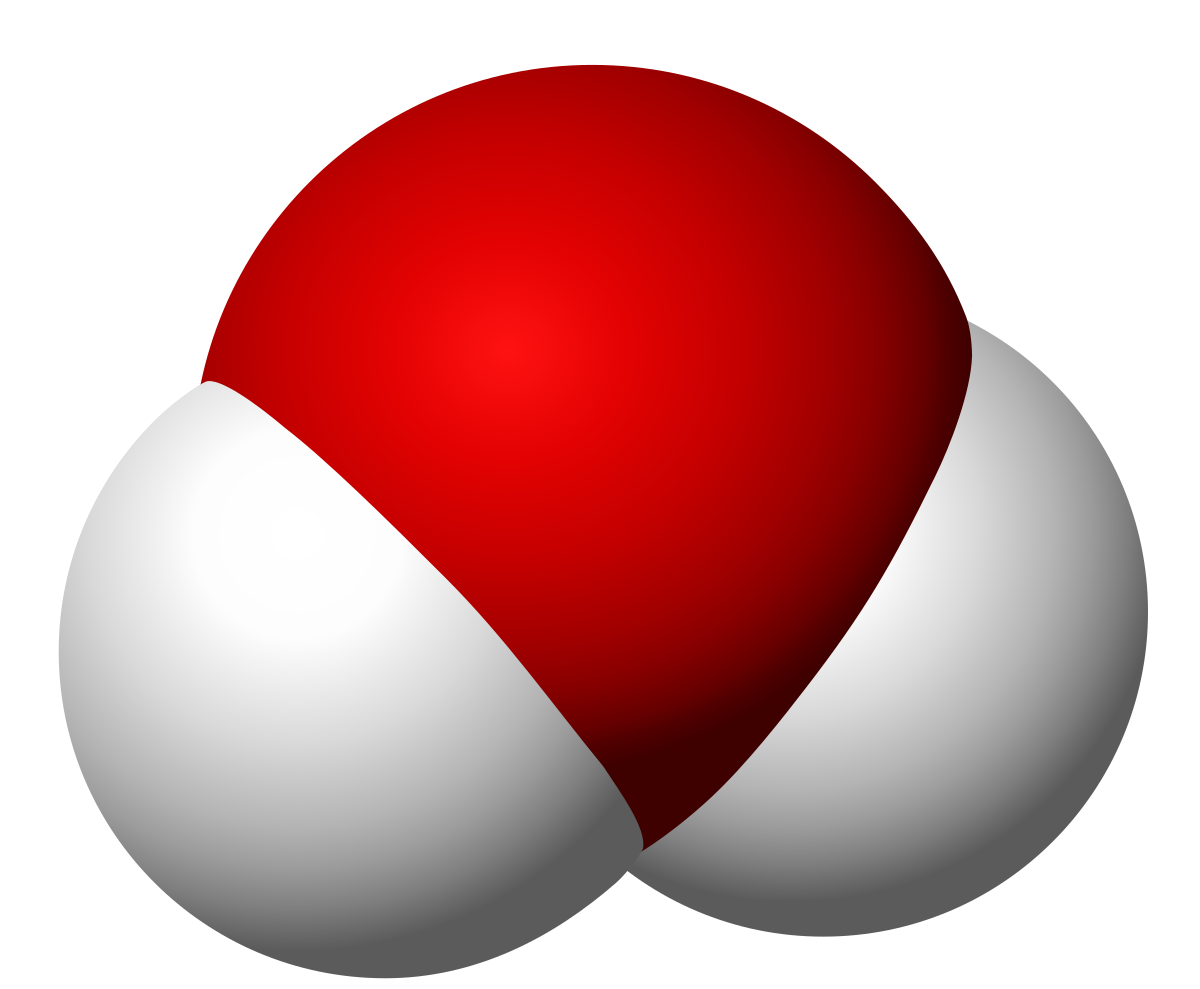
Pokud analyzujeme tuto molekulu, můžeme vidět, že úhel připojení kovalentní vazby mezi vodíkem a kyslíkem začíná od 104.5 stupňů. Toho lze dosáhnout spektroskopickou a rentgenovou analýzou. Průměrná vzdálenost mezi atomy vodíku a kyslíku je 96.5 hod. nebo, co je stejné, 9.65 • 10–8 milimetrů.
Tyto vzdálenosti nelze srovnávat s ničím, co může lidské oko vidět. Uspořádání elektronů v molekule vody komunikuje elektrickou asymetrii, protože mezi vodíkem a kyslíkem je jiná úroveň elektronegativity. Voláme elektronegativitu schopnost atomu přitahovat elektrony, které jsou sdílené v kovalentní vazbě. Pamatujeme si, že kovalentní vazba je vazba, která je vytvořena mezi dvěma nekovovými atomy.
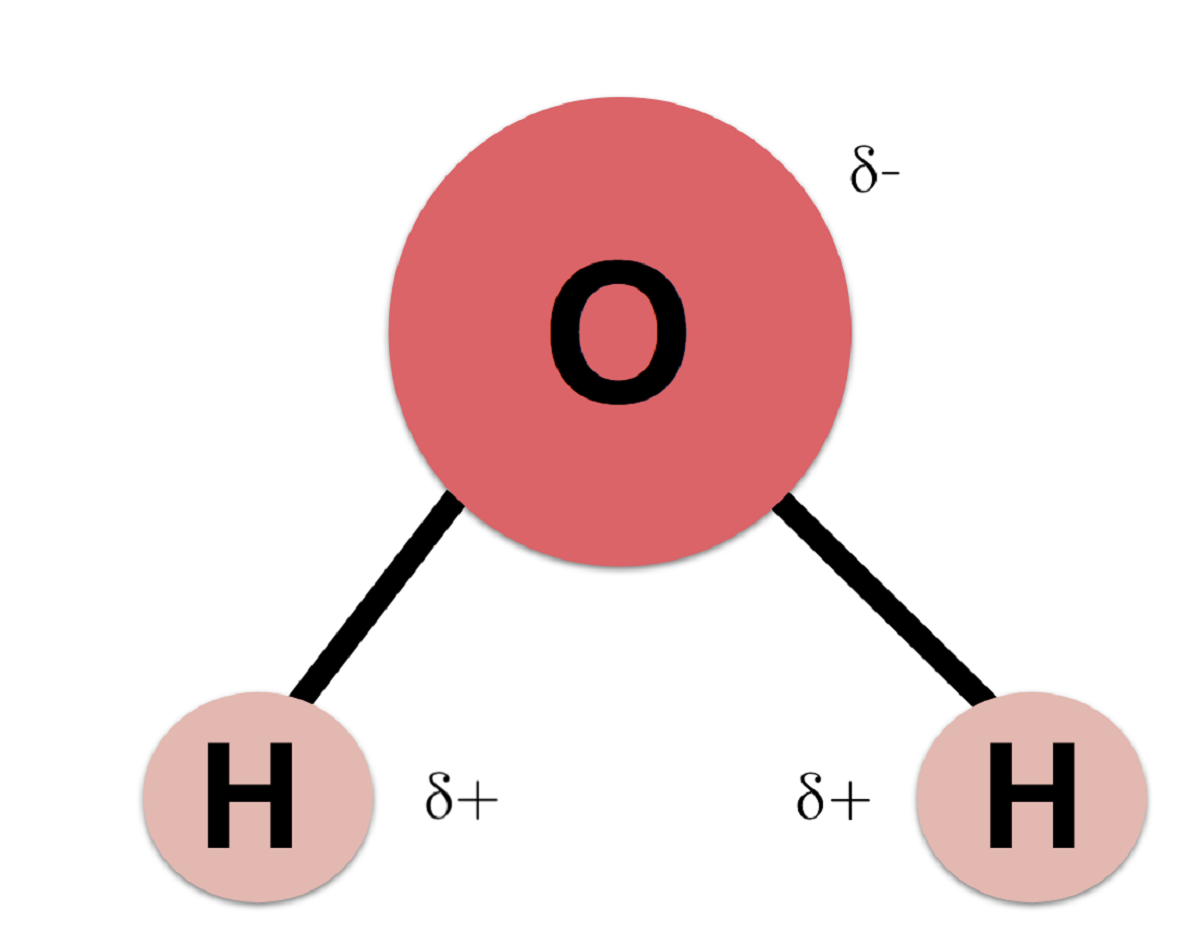
Vzhledem k tomu, že kyslík má větší elektronegativitu než vodík, je pravděpodobné, že elektrony jsou blíže atomu kyslíku než vodíku. Je to proto, že elektrony jsou záporně nabité. Skutečnost, že elektrony jdou většinou k atomům kyslíku, způsobuje, že atom vodíku má určitý kladný náboj. Tento náboj se nazývá kladný částečný náboj. Kyslíku se říká záporný částečný náboj.
Rozdíl mezi kladnými a zápornými elektrony, které jsou blízko obou atomů, činí z molekuly vody polární molekulu. To znamená, že molekula má část se záporným pólem a další část s kladným pólem. Přestože je celá molekula neutrální, jsou od ní odvozeny všechny její fyzikálně-chemické a biologické vlastnosti.
Interakce mezi molekulami
Když je několik molekul vody velmi blízko u sebe, jsou schopny samostatně navázat trakci mezi atomy kyslíku molekul. Je to proto, že kyslík má záporný částečný náboj a jeden z vodíků má kladný částečný náboj. Proto je pozitivní část jedné molekuly vody přitahována k negativní části druhé molekuly vody. Tento typ interakce mezi molekulami se nazývá zdroj vodíku. V těchto molekulách se toho hodně děje, protože jsou uspořádány takovým způsobem každá molekula vody je schopná se spojit s dalšími 4 molekulami. K tomuto typu interakce dochází s ledem.
Vazby mezi vodíky probíhají díky tomu, že existuje atom se záporným částečným nábojem a vodík s kladným částečným nábojem. Díky tomu nejsou odkazy jedinečné pro vodu. Tyto interakční vazby se také vyskytují v dusíku, fluoru a vodíku v jiných molekulách, které obsahují proteiny a DNA.
Podívejme se, jaké jsou fyzikálně-chemické vlastnosti molekuly vody. Mezi těmito vlastnostmi a vlastnostmi můžeme vyzdvihnout kapacitu a rozpouštědlo. Nesmíme zapomínat, že voda je považována za univerzální rozpouštědlo. Další charakteristikou molekuly vody je její vysoké měrné teplo a její odpařovací teplo. Má také velkou soudržnost a adhezi, abnormální hustotu a funguje jako chemické činidlo.
Použijeme-li vlastnosti vody, zjistíme, že je díky svému polárnímu charakteru schopna v ní rozptýlit velké množství sloučenin. Jak jsme již zmínili dříve, i když je celá molekula neutrální, skutečnost, že má pozitivní část a negativní část, je co Poskytuje fyzikálně-chemické vlastnosti, pro které je voda tak nezbytná pro život. Pracuje tedy se solemi a jinými iontovými látkami, ve kterých molekula vody orientuje své póly. Tato orientace pólů nastává jako funkce nábojů dvou iontů, kladení záporného pólu na jednu stranu a kladného pólu na druhou. Například u polárních látek, jako je ethanol, působí voda podobným způsobem. Je proti jednomu pólu proti druhému s opačným znamením látky.
Vlastnosti molekuly vody
Molekula vody má vysoké specifické teplo. Toto specifické teplo není nic jiného než množství tepla, kterému je třeba podat gram vody, aby mohl zvýšit svoji teplotu o jeden stupeň. Na druhou stranu máme výparné teplo. Jedná se o množství páry, které musí být aplikováno na gram kapaliny, aby mohla přejít na gram páry. Víme, že molekula vody má vysoké specifické teplo a odpařování díky můstkům, které spojují atomy vodíku. To znamená, že aby se zvýšila teplota vody o jeden stupeň, musí všechny molekuly zvýšit své vibrace. K tomu rozbijí vodíkové vazby, aby mohli projít gramem kapalné vody na gram parní vody.
Skutečnost, že má vysokou hodnotu odpařovacího tepla, je způsobena tím, že může projít. Další charakteristikou molekuly vody je soudržnost. Otázkou je tendence, že dvě molekuly musí být spojeny. Díky vodíkovým vazbám molekuly vody je vysoká soudržnost. Přistoupení je tendence dvou různých molekul vzájemně se spojovat. Díky tomu má molekula vody vysokou adhezi ke sloučeninám, které jsou iontové a polární. K této aplikaci dochází, když se stane, že voda ulpívá na různých površích.
Doufám, že s těmito informacemi se dozvíte více o molekule vody.