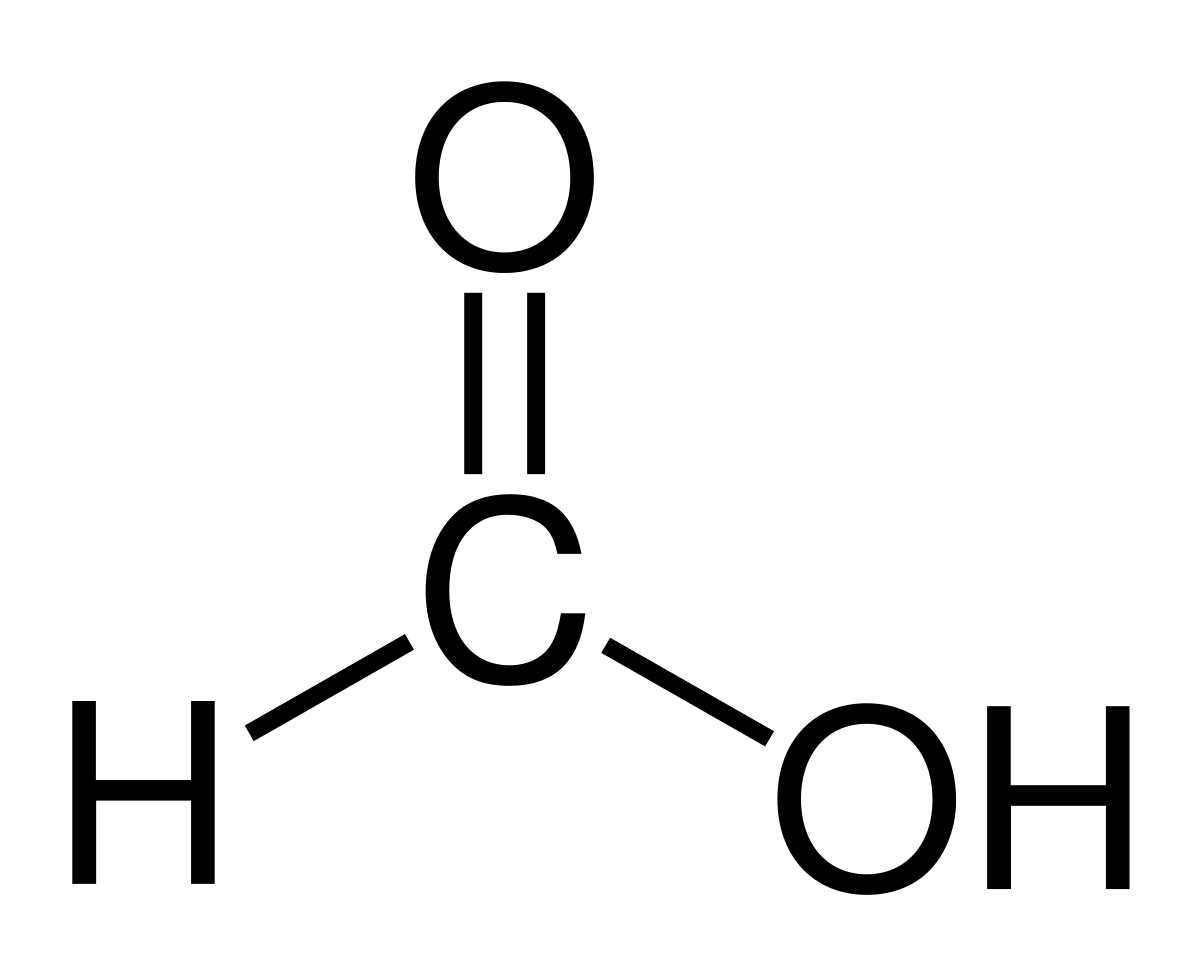
El ácido fórmico o ácido metanoico es el compuesto más simple y pequeño de todos los ácidos orgánicos. Tiene la fórmula molecular HCOOH con solo un átomo de hidrógeno unido a un átomo de carbono. Su nombre proviene de la palabra formica, que significa hormiga en latín. Se trata de un compuesto bastante importante en el mundo de la química y muy utilizado en la actualidad.
Por ello, vamos a dedicar este artículo a contarte todo lo que debes saber sobre el ácido fórmico, sus características e importancia.
Características principales
Los naturalistas del siglo XV descubrieron que ciertos tipos de insectos (termicidas), como hormigas, termitas, abejas y escarabajos, secretan este compuesto que hace que sus picaduras sean dolorosas. Además, estos insectos utilizan este compuesto como mecanismo de ataque, defensa y señalización química.
Tienen glándulas tóxicas que expulsan este y otros ácidos, como el ácido acético, del cuerpo en forma de niebla. El ácido fórmico es más fuerte que el ácido acético (CH3COOH); por lo tanto, una cantidad igual de ácido fórmico disuelta en agua dará como resultado una solución con un pH más bajo.
El naturalista inglés John Ray logró el aislamiento de este compuesto en 1671, extraído de un gran número de hormigas. Por otro lado, la primera síntesis exitosa de este compuesto fue realizada por el químico y físico francés Joseph Gay-Lussac usando ácido cianhídrico (HCN) como reactivo.
Ácido fórmico en la naturaleza

El ácido fórmico puede existir a niveles terrestres, como componente de la biomasa o en la atmósfera, participando en una amplia gama de reacciones químicas, incluso puede encontrarse bajo tierra, en el petróleo o en fase gaseosa en su superficie.
En términos de biomasa, los insectos y las plantas son los principales productores de este ácido. Cuando los combustibles fósiles se queman, producen ácido fórmico gaseoso; por lo tanto, los motores de los automóviles liberan este ácido a la atmósfera.
Sin embargo, hay una gran cantidad de hormigas viviendo en la tierra, y la producción de ácido fórmico entre ellas es miles de veces mayor que la cantidad de ácido metanoico producido por la industria humana en un año. Asimismo, los incendios forestales son una fuente gaseosa de ácido fórmico.
Más arriba, en la compleja matriz atmosférica, tienen lugar procesos fotoquímicos para la síntesis de ácido fórmico. En este punto, muchos compuestos orgánicos volátiles (COV) se degradan bajo la acción de la radiación UV o se oxidan por el mecanismo de radicales OH. La rica y compleja química atmosférica es, con mucho, la principal fuente de ácido metanoico en la Tierra.
Estructura atómica del ácido fórmico
La figura anterior muestra la estructura del dímero en fase gaseosa del ácido fórmico. Las esferas blancas corresponden a átomos de hidrógeno, las rojas a átomos de oxígeno y las negras a átomos de carbono.
Se pueden ver dos grupos en estas moléculas: hidroxilo (-OH) y formilo (-CH=O), los cuales son capaces de formar enlaces de hidrógeno. Estas interacciones son del tipo O-H-O, donde el grupo hidroxilo es el donante de H y el grupo formilo es el donante de O.
Sin embargo, el H unido a átomos de carbono carece de esta capacidad. Estas interacciones son muy fuertes y el hidrógeno en el grupo OH es más ácido debido al átomo de H deficiente en electrones; por lo tanto, este hidrógeno estabiliza aún más el puente. Como resultado de lo anterior, el ácido fórmico existe en forma de dímero y no como molécula individual.
A medida que baja la temperatura, el dímero orienta sus enlaces de hidrógeno para crear la estructura más estable con otros dímeros, lo que da como resultado infinitas cadenas alfa y beta de ácido metanoico. Esta estructura cristalina depende de las variables físicas que actúan sobre ella como la presión y la temperatura. Por lo tanto, la cadena es convertible. Si la presión aumenta a niveles extremos, las cadenas se comprimen lo suficiente como para ser consideradas un polímero cristalino de ácido fórmico.
Propiedades
Vamos a centrarnos en describir cuáles son las propiedades principales del ácido fórmico:
- El ácido metanoico es un líquido incoloro a temperatura ambiente con un fuerte olor acre. Tiene un peso molecular de 46g/mol, un punto de fusión de 8,4ºC y un punto de ebullición de 100,8ºC, superior al del agua.
- Miscible con agua y disolventes orgánicos polares como éter, acetona, metanol y etanol.
- Por el contrario, en disolventes aromáticos como el benceno y el tolueno, es poco soluble porque el ácido fórmico tiene pocos átomos de carbono en su estructura.
- Tiene un pKa de 3,77, que es más ácido que el ácido acético, lo que puede explicarse porque el grupo metilo aporta densidad electrónica al átomo de carbono oxidado por dos oxígenos. Esto da como resultado una ligera disminución en la acidez de los protones (CH3COOH, HCOOH).
- Una vez que el ácido se desprotona, se convierte en el anión formiato HCOO-, que deslocaliza la carga negativa entre los dos átomos de oxígeno. Por lo tanto, es un anión estable y es responsable de la alta acidez del ácido fórmico.
Usos del ácido fórmico
La industria de los alimentos y agricultura
Tan nocivo como el ácido metanoico, se utiliza en concentraciones suficientes como conservante de alimentos debido a su efecto antibacteriano. Por la misma razón que se usa en la agricultura, también tiene propiedades insecticidas. También tiene un efecto antiséptico en los pastos y ayuda a prevenir los gases intestinales en los animales de cría.
La industria textil y del calzado
Se utiliza en la industria textil para teñir y refinar textiles y es probablemente el uso más común de este ácido. El ácido fórmico se utiliza para el procesamiento del cuero y el depilado de este material por su acción desengrasante. La desprotonación del ácido fórmico se convierte en el anión formiato HCOO-, que deslocaliza la carga negativa entre los dos átomos de oxígeno. Por lo tanto, es un anión estable y es responsable de la alta acidez del ácido fórmico.
Seguridad vial
Además de los usos industriales especificados, los derivados del ácido fórmico (formato) se utilizan en carreteras de invierno en Suiza y Austria para reducir el riesgo de accidentes. Este tratamiento es más efectivo que usar sal de mesa.
Espero que con esta información puedan conocer más sobre el ácido fórmico, su estructura y sus usos.